Clear Sky Science · it
Un circuito basalo-prefrontale-talamo definito a livello molecolare regola le dimensioni sensoriali e affettive del dolore nei topi maschi
Perché questo circuito cerebrale è importante per il dolore
Il dolore è più di una puntura acuta o di un dolore sordo; comprende anche una componente emotiva e può rimodellare il nostro umore e comportamento per anni. Molti pazienti con dolore cronico ottengono poco beneficio dagli attuali farmaci e spesso affrontano effetti collaterali significativi. Questo studio su topi maschi scopre un circuito cerebrale definito con precisione che aiuta il cervello a modulare il dolore, sia in termini di intensità percettiva sia di disagio emotivo. Mappando e controllando questo percorso, il lavoro indica nuove modalità più mirate per alleviare il dolore cronico senza fare affidamento esclusivo sui tradizionali analgesici.
Un’autostrada nascosta dal cervello cognitivo al centro del dolore
I ricercatori si sono concentrati sulla corteccia prefrontale mediale, una regione anteriore del cervello coinvolta nel processo decisionale, nelle emozioni e nel controllo del dolore, e sul talamo, un centro di rilè profondo che modula sia l’intensità sia l’unpleasantness del dolore. Hanno scoperto che un gruppo specifico di cellule nella corteccia prefrontale mediale, contrassegnate da un gene chiamato Foxp2, costituisce una via di uscita importante verso il talamo. Queste cellule si trovano principalmente nello strato corticale più profondo e inviano lunghi assoni a nuclei talamici particolari, trascurando in gran parte altri bersagli tipici della corteccia prefrontale. Usando metodi di tracciamento e mappature cerebrali globali, il team ha mostrato che i neuroni marcati da Foxp2 si connettono fortemente a tre regioni talamiche note per influenzare l’elaborazione del dolore: il nucleo parataeniale, il talamo mediodorsale e il talamo ventromediale. 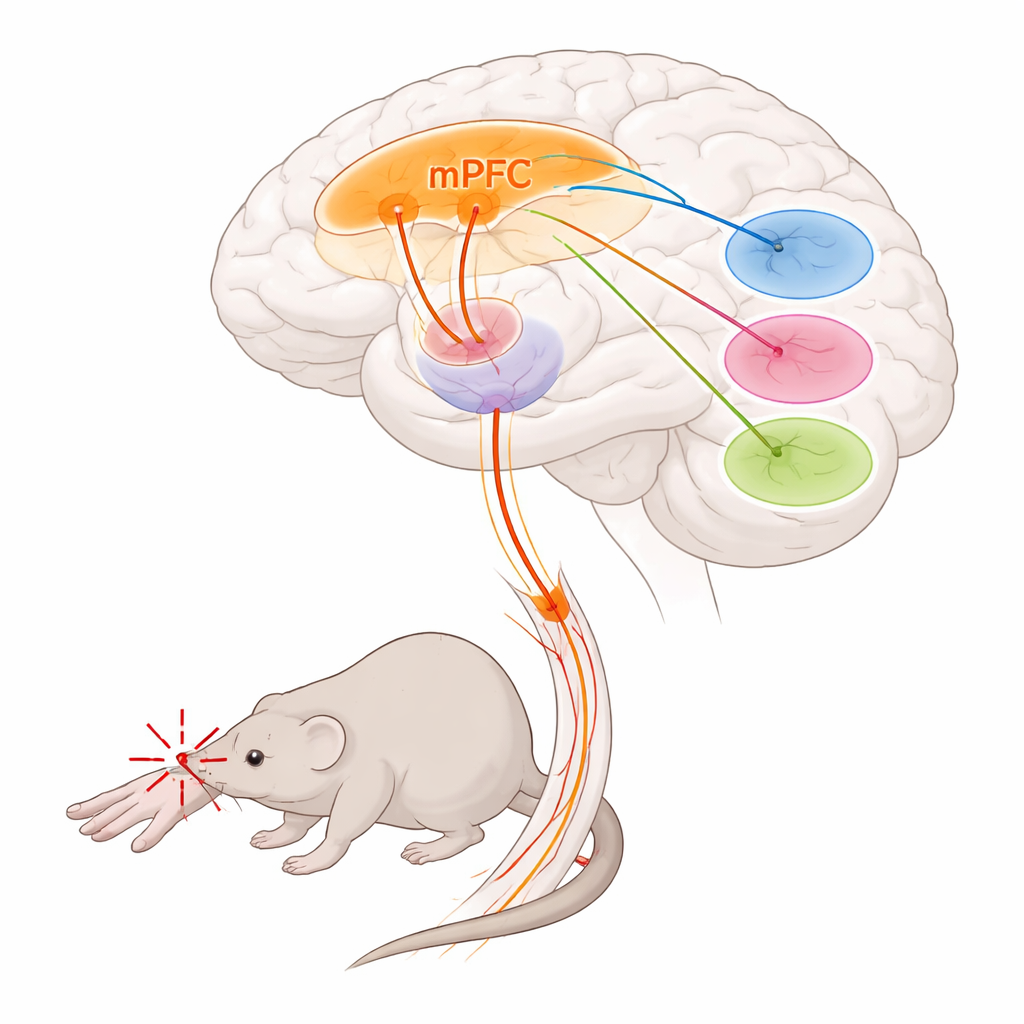
Quando il dolore colpisce, un centro di controllo chiave si zittisce
Per vedere come si comporta questo percorso durante il dolore, gli scienziati hanno impiantato piccole lenti sopra la corteccia prefrontale mediale e hanno registrato l’attività di singoli neuroni marcati da Foxp2 in topi svegli. Durante brevi pizzicotti meccanici, dolore chimico indotto dalla formalina e dolore infiammatorio prolungato, queste cellule si sono costantemente indebolite: la maggior parte mostrava meno raffiche di attività durante gli episodi dolorosi e nei giorni successivi all’infortunio infiammatorio. Questo spegnimento non era sottile; in alcune condizioni più di un terzo fino a quasi la metà delle cellule divenne nettamente meno attiva. La scoperta suggerisce che gli stati di dolore acuto e cronico possono, in parte, riflettere il silenziamento di un sistema frenante prefrontale naturale che altrimenti aiuterebbe a contenere il dolore.
Accendere e spegnere il circuito rimodella il dolore
Il gruppo ha poi chiesto se questo spegnimento fosse solo un effetto collaterale del dolore o un suo motore. Usando strumenti genetici, hanno bloccato a lungo termine l’output dei neuroni marcati da Foxp2 oppure ne hanno potenziato brevemente l’attività. L’inattivazione persistente ha reso i topi più sensibili al tatto e al calore, indicando che questo percorso normalmente limita i segnali dolorifici in arrivo. Al contrario, l’attivazione a breve termine ha aumentato la soglia per gli stimoli dolorosi, ridotto il leccamento nella fase tardiva nel test della formalina (una misura del dolore infiammatorio in corso) e ha fatto preferire ai topi gli ambienti in cui il circuito era stato attivato, segnalando sollievo dal carico emotivo del dolore. Illuminando rami specifici del percorso, i ricercatori hanno mostrato che le proiezioni verso il talamo parataeniale riducono sia la sensibilità fisica sia le risposte di coping, mentre le proiezioni verso il talamo mediodorsale e ventromediale modulano principalmente le dimensioni emotive e comportamentali. Nel complesso, questi risultati rivelano uno schema di wiring finemente suddiviso in cui diversi rami della stessa popolazione prefrontale controllano aspetti differenti dell’esperienza del dolore.
Taratura chimica: un potenziamento colinergico per il sollievo dal dolore
Cosa controlla questi neuroni prefrontali coinvolti nel sollievo dal dolore? Esperimenti di tracciamento hanno scoperto forti input da una regione colinergica del prosencefalo basale chiamata banda diagonale orizzontale. Molte delle cellule che inviano segnali da quest’area verso i neuroni marcati da Foxp2 utilizzano l’acetilcolina, un mediatore coinvolto nell’attenzione e nell’arousal. L’attivazione di questa proiezione colinergica ha ridotto la sensibilità meccanica e i comportamenti di coping e ha attenuato l’ipersensibilità infiammatoria, sebbene non abbia spostato in modo netto il tono emotivo negativo del dolore. Sul versante recettoriale, i neuroni marcati da Foxp2 risultarono arricchiti per un particolare tipo di recettore per l’acetilcolina, noto come recettore nicotinico α4β2. La somministrazione diretta di un agonista selettivo α4β2 nella corteccia prefrontale mediale ha reso i topi meno sensibili al calore e al tatto dolorosi, anche in stati infiammatori cronici, e ha aumentato l’attività dei neuroni marcati da Foxp2. Il blocco di questi neuroni ha eliminato il beneficio del farmaco, dimostrando che questo recettore allevia il dolore specificamente eccitando questo tipo cellulare. 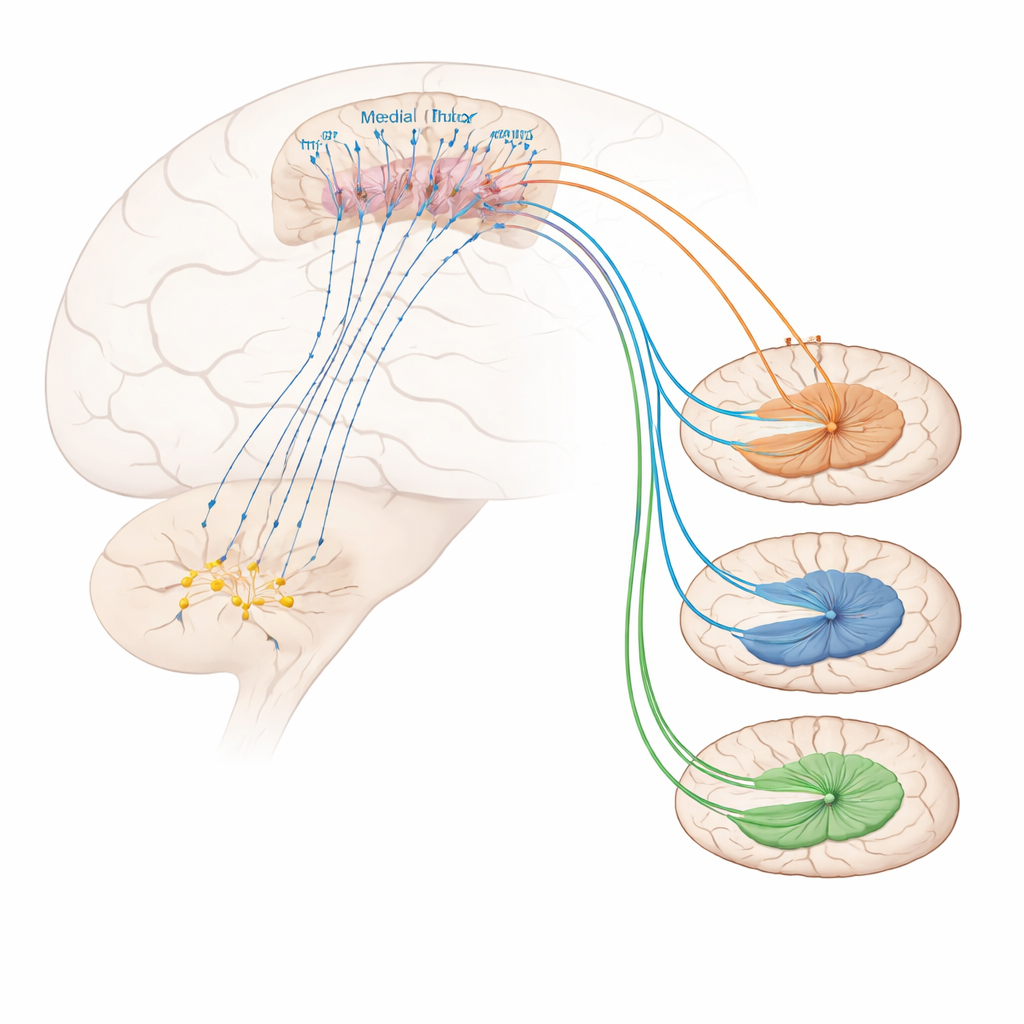
Cosa significa per il futuro trattamento del dolore
In termini pratici, lo studio identifica un percorso preciso in tre tappe: una regione colinergica “accenditrice” nel prosencefalo basale, un insieme specializzato di cellule di controllo nella corteccia prefrontale mediale e hub di rilè distinti nel talamo che governano separatamente quanto forte il dolore si percepisce, quanto è spiacevole dal punto di vista emotivo e come reagiamo. Il dolore sembra abbassare l’attività di questo circuito; riattivarlo, sia mediante stimolazione diretta sia mirando i suoi recettori per l’acetilcolina, attenua sia il dolore fisico sia il disagio associato al dolore infiammatorio nei topi maschi. Pur rimanendo molto lavoro per tradurre questi risultati agli esseri umani e ad altre forme di dolore cronico, i risultati evidenziano una strategia promettente: invece di anestetizzare tutta la sensazione, i trattamenti futuri potrebbero ripristinare o sintonizzare i circuiti cerebrali endogeni di sollievo dal dolore per terapie a lungo termine più efficaci e potenzialmente più sicure.
Citazione: Xie, G., Liu, Y., Qi, X. et al. A molecularly defined basalo-prefrontal-thalamic circuit regulates sensory and affective dimensions of pain in male mice. Nat Commun 17, 2134 (2026). https://doi.org/10.1038/s41467-026-69001-2
Parole chiave: dolore cronico, corteccia prefrontale mediale, talamo, segnalazione colinergica, recettori nicotinici