Clear Sky Science · it
Modifica covalente di un acido glutammico ispirata alla tecnologia HaloTag
Trasformare gli “ancoraggi” proteici in bersagli farmacologici
Molti farmaci oncologici moderni funzionano agganciandosi a proteine all’interno delle nostre cellule. Tuttavia alcune delle proteine più importanti non offrono maniglie facili per i medicinali. Questo studio introduce un ingegnoso trucco chimico, ispirato a uno strumento di laboratorio molto diffuso chiamato HaloTag, per fissarsi su un punto normalmente difficile da raggiungere in una proteina che regola segnali di crescita rilevanti per il cancro. Il lavoro potrebbe aprire nuove strade verso farmaci che spengono in modo più duraturo le vie che guidano i tumori.
Perché la maggior parte dei farmaci covalenti mira allo stesso sito
Negli ultimi anni i cosiddetti farmaci covalenti mirati sono diventati una classe di medicinali promettente. Portano un gruppo chimico debolmente reattivo che forma un legame permanente con un amminoacido specifico di una proteina, bloccando il farmaco al suo posto. Quasi tutti questi farmaci prendono di mira la cisteina, un amminoacido relativamente raro ma altamente reattivo. Per contrasto, altri due amminoacidi, l’aspartato e il glutammato, sono molto più comuni e spesso cruciali per la forma e la funzione di una proteina, ma i loro gruppi carbossilato acidi sono molto meno reattivi nell’ambiente acquoso cellulare. Questo li rende difficili da modificare in modo selettivo, e prima di questo lavoro esistevano solo pochi esempi riusciti di farmaci covalenti che prendessero di mira glutammato o aspartato.
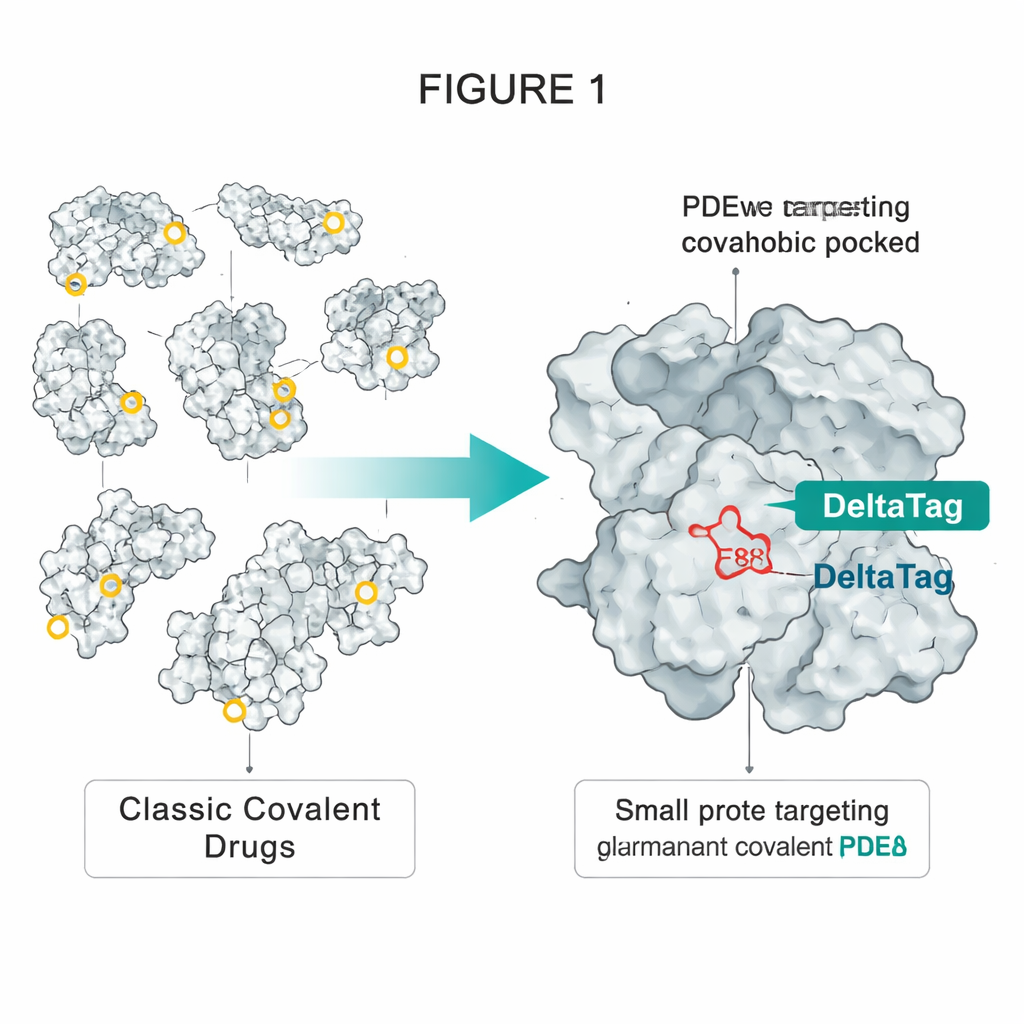
Prendere in prestito un trucco dalla tecnologia HaloTag
Gli autori hanno tratto ispirazione da HaloTag, una proteina ingegnerizzata ampiamente utilizzata che può essere marcata in modo permanente con coloranti fluorescenti. In HaloTag, un aspartato posizionato appositamente, in profondità in una tasca idrofobica, reagisce con una catena cloroalcano semplice presente sul colorante, formando un legame estere stabile. Il gruppo ha notato che un’altra proteina, PDEδ, possiede una tasca idrofobica simile che contiene un singolo glutammato accessibile, chiamato E88. PDEδ trasporta proteine di segnalazione lipidate come la piccola GTPasi Rheb attraverso la cellula, aiutandole a raggiungere le membrane dove complessi promotori della crescita come mTORC1 vengono attivati. Inibitori non covalenti di PDEδ sviluppati in precedenza potevano bloccare questo trasporto, ma il loro effetto era limitato perché un’altra proteina, Arl2, può rimuoverli dalla tasca nel tempo.
Progettare DeltaTag per fissarsi al glutammato
Per superare questo problema dello “sgancio”, i ricercatori sono partiti da un noto bloccante ad alta affinità di PDEδ e hanno riprogettato uno dei suoi sostituenti per portare un "warhead" haloalcano simile a quelli usati nei ligandi HaloTag. Attraverso diverse iterazioni di ottimizzazione strutturale guidate dalle strutture cristalline della proteina, sono giunti a un composto chiamato DeltaTag. La sua caratteristica chiave è un gruppo fenetil bromuro posizionato in modo che, una volta che la molecola si inserisce nella tasca lipidica di PDEδ, il bromuro sia allineato con precisione per reagire con E88. Misure biofisiche e strutture cristallografiche ad alta risoluzione hanno confermato che DeltaTag forma un legame estere covalente specificamente con questo glutammato e che altri amminoacidi potenzialmente più reattivi su PDEδ restano intatti. Il composto è sufficientemente reattivo da marcare efficacemente la proteina, ma abbastanza stabile in acqua e in presenza del principale antiossidante solforato della cellula, il glutatione, da evitare danni diffusi e indiscriminati.
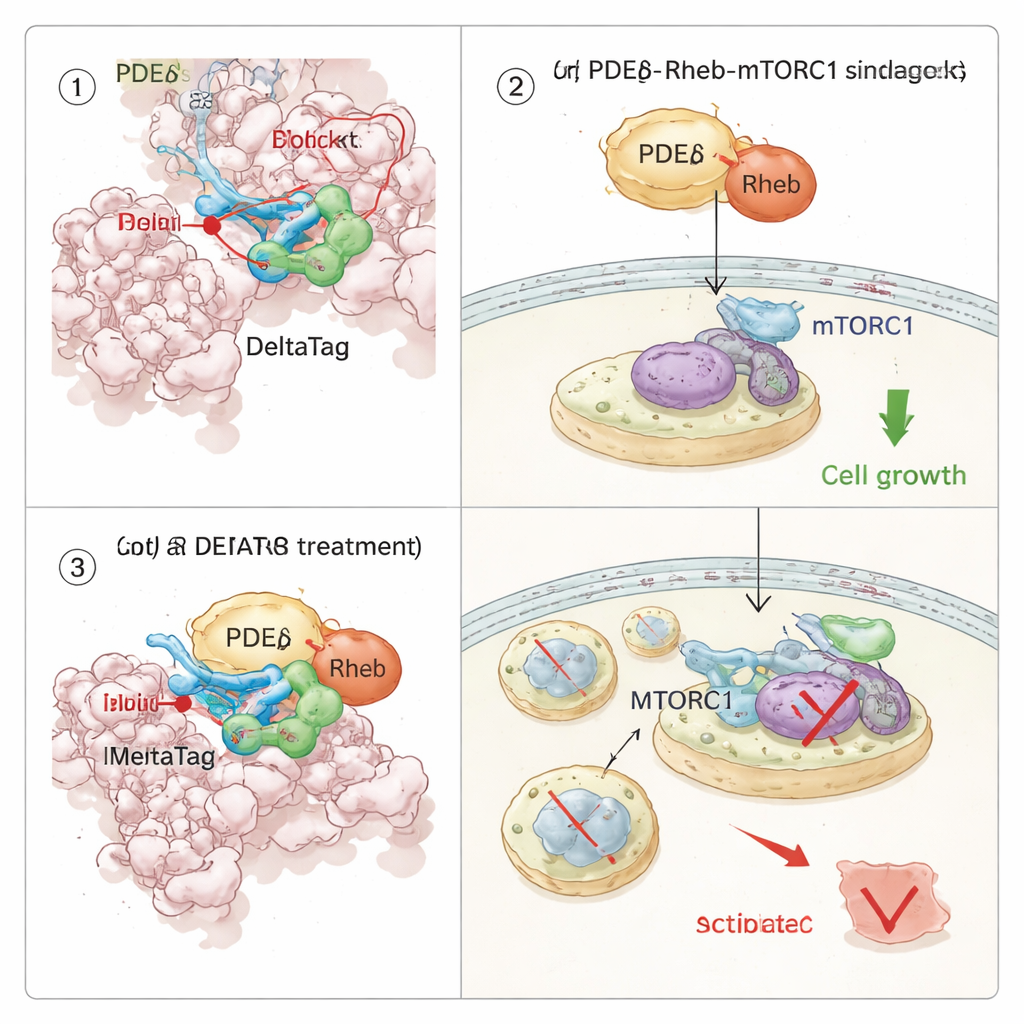
Riconfigurare una via di crescita dentro le cellule tumorali
Poiché PDEδ accompagna Rheb, e Rheb a sua volta attiva la via di crescita mTORC1, il team ha indagato come l’inibizione covalente di PDEδ si ripercuotesse sulla segnalazione cellulare. Utilizzando profili di stabilità termica su migliaia di proteine, hanno mostrato che DeltaTag si lega selettivamente a PDEδ negli estratti cellulari e altera proteine collegate all’asse Rheb–mTOR. In esperimenti di imaging in cellule vive, DeltaTag ha fatto sì che Rheb si spostasse da un pattern diffuso nell’interno cellulare verso membrane interne più raggruppate, coerente con l’interruzione del suo normale trasporto. La fosfoproteomica globale e i western blot mirati hanno rivelato che l’attività di mTORC1, seguita tramite la fosforilazione di una proteina ribosomale chiamata S6, è diminuita nel tempo, mentre segnali compensatori in vie correlate sono aumentati. È importante che, in diverse linee cellulari tumorali umane guidate da KRAS mutante e dipendenti da una forte segnalazione mTOR, DeltaTag abbia rallentato la proliferazione cellulare più efficacemente rispetto a inibitori reversibili strettamente correlati, e il suo effetto è stato più debole in cellule prive di PDEδ, a sostegno dell’azione principalmente on‑target.
Aprire una porta a nuovi tipi di bersagli farmacologici
Questo lavoro dimostra che è possibile costruire piccole molecole che formano un legame permanente e altamente specifico con un singolo glutammato sepolto in una tasca idrofobica di una proteina, usando una chimica haloalcano relativamente semplice presa in prestito da HaloTag. Nel sistema modello PDEδ, quel legame covalente produce un blocco più duraturo di una via di crescita rilevante per il cancro rispetto ai precedenti farmaci reversibili. Più in generale, la stessa logica di progettazione potrebbe essere applicata ad altre proteine che presentano cavità idrofobiche ma mancano dei consueti amminoacidi “reattivi”, purché espongano un glutammato o un aspartato posizionato strategicamente. Con ulteriori ottimizzazioni, inibitori covalenti mirati al glutammato come DeltaTag potrebbero diventare strumenti utili per la biologia chimica e, in ultima analisi, candidati per nuove terapie che affrontano proteine attualmente difficili da colpire con farmaci.
Citazione: Zhang, R., Liu, J., Gasper, R. et al. Covalent modification of a glutamic acid inspired by HaloTag technology. Nat Commun 17, 1257 (2026). https://doi.org/10.1038/s41467-026-68999-9
Parole chiave: inibitori covalenti, mirare il glutammato, PDEδ, segnalazione mTOR, progettazione di farmaci antitumorali