Clear Sky Science · it
Ingegnerizzare cellule sintetiche con domini intramembrana che possiedono distinte asimmetrie di doppio strato
Perché contano le piccole bolle sintetiche
Ogni cellula vivente è avvolta da una membrana che si comporta come una pelle intelligente e flessibile. Questa pelle non è uniforme: il lato interno e quello esterno, e persino differenti zone lungo la sua superficie, possono avere composizioni e forme molto diverse. Queste differenze aiutano le cellule a inviare segnali, legare proteine e persino dividersi. Tuttavia è stato sorprendentemente difficile costruire membrane modello semplici e controllabili che catturino questa complessità. Questo studio introduce un modo pratico per realizzare “cellule sintetiche” delle dimensioni cellulari le cui membrane sono asimmetriche su entrambi i foglietti e lateralmente segmentate in regioni distinte — aprendo una strada a modelli cellulari più realistici e allo studio di come i pattern di membrana guidino gemmazione e divisione. 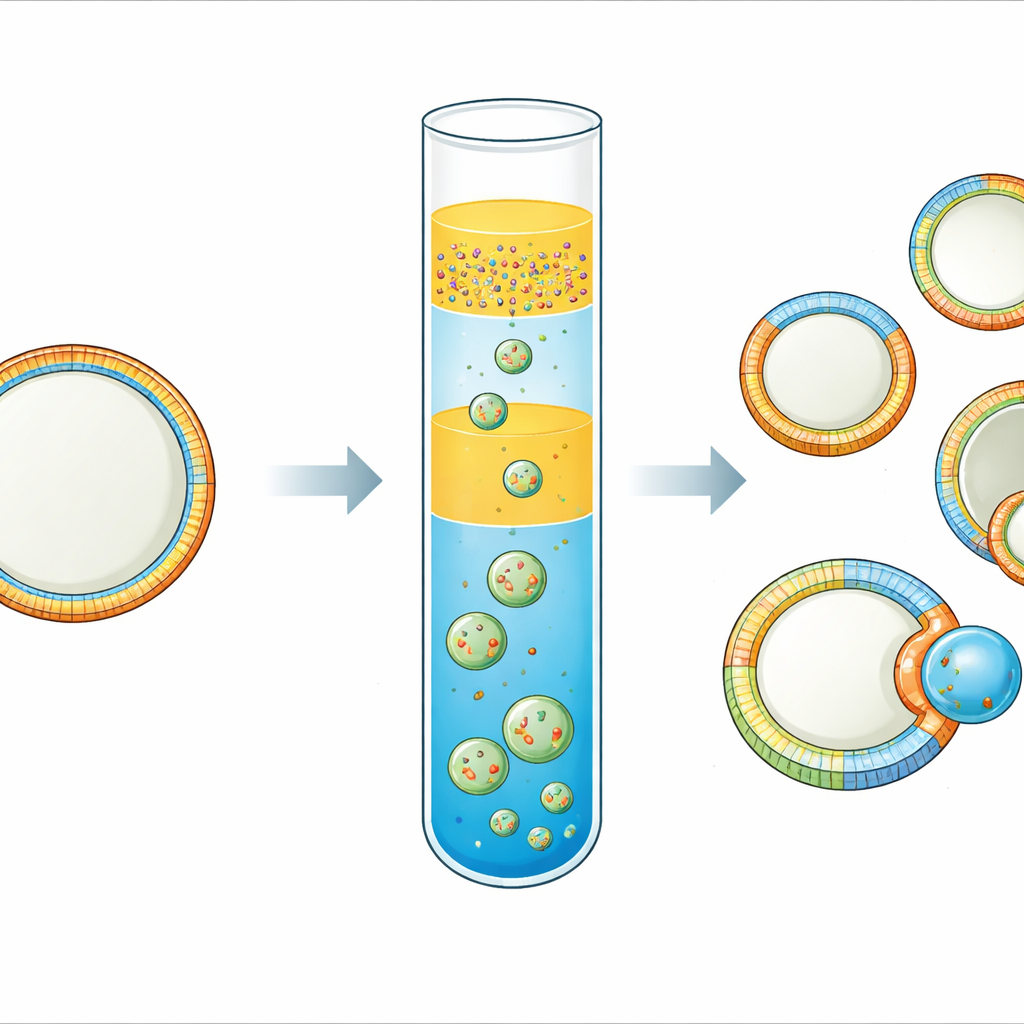
Costruire migliori imitazioni cellulari
Le membrane delle cellule reali sono asimmetriche: il lato interno è ricco di lipidi carichi negativamente che attraggono proteine di segnalazione, mentre il lato esterno porta lipidi diversi che mediano il riconoscimento cellula–cellula. Molti metodi di laboratorio possono generare vescicole giganti — sfere cave di molecole simili ai lipidi — ma i loro due foglietti finiscono di solito per essere uguali e l’interno è difficile da raggiungere. Altri approcci che creano asimmetria richiedono spesso dispositivi complessi, lipidi speciali o lasciano le vescicole attaccate a una superficie. Gli autori si sono proposti di creare vescicole autosufficienti e di dimensione cellulare che combinino un elevato incapsulamento di biomolecole con un’asimmetria robusta e regolabile, più simile a quella di una cellula vivente.
Una ricetta a tre strati per membrane asimmetriche
Il gruppo ha perfezionato una tecnica di “emulsione invertita”, in cui minuscole gocce d’acqua ricoperte di lipidi vengono spinte attraverso un’interfaccia olio–acqua per formare vescicole. La loro innovazione chiave è un allestimento con tre strati di olio. In basso si trova un olio contenente i lipidi destinati al foglietto esterno della membrana. Sopra questo, viene posto un sottile strato di olio-spaziatore privo di lipidi, e sopra ancora un’emulsione di gocce d’acqua circondate da un secondo olio che porta i lipidi per il foglietto interno. Durante un breve passaggio di centrifugazione, le gocce attraversano lo spaziatore e lo strato inferiore, acquisendo un secondo rivestimento lipidico e chiudendosi in vescicole. Scegliendo due oli di diversa densità e includendo lo spaziatore si limita nettamente il mescolamento tra i serbatoi lipidici, così i foglietti interno ed esterno mantengono composizioni distinte.
Verificare che i due lati rimangano diversi
Per verificare che avessero veramente foglietti differenti, i ricercatori hanno usato sia letture chimiche sia test basati su proteine. In una serie di esperimenti hanno aggiunto un lipide fluorescente in un solo foglietto e poi esposto le vescicole a una sostanza chimica nella soluzione esterna che annulla la fluorescenza ma non può attraversare la membrana. Quando il lipide fluorescente era sul lato esterno, il segnale diminuiva quasi completamente; quando era sul lato interno cambiava di poco, mostrando che la maggior parte dei lipidi marcati restava dove previsto. In un secondo insieme di esperimenti hanno posto lipidi che legano proteine specifiche — come lipidi marcati con biotina per lo streptavidina o teste speciali per una proteina fluorescente verde con tag His — in un solo foglietto. Le proteine aggiunte al compartimento opposto (interno o esterno) si legavano solo quando il lipide corrispondente era sullo stesso lato della membrana, confermando sia una forte asimmetria sia la funzione proteica preservata.
Creare zattere e osservare la gemmazione delle membrane
Le membrane cellulari reali contengono anche “zattere”: piccole zone arricchite in specifici lipidi come colesterolo e sfingomielina, che possono clusterizzare proteine e influenzare la forma. Ottenere una tale separazione di fase con il metodo a emulsione invertita era stato difficile perché il colesterolo tendeva a rimanere disciolto nell’olio invece di unirsi alla membrana. Usando lo squalene nello strato di olio inferiore, che trattiene il colesterolo meno saldamente rispetto al comune olio minerale, gli autori sono riusciti a formare in modo riproducibile vescicole le cui membrane si separavano in regioni liquide ordinate e liquide disordinate coesistenti, molto simili alle zattere. Hanno poi combinato questo pattern laterale con l’asimmetria dei foglietti: un dominio portava un ligando sul foglietto interno che legava streptavidina all’interno, mentre un altro dominio portava glicolipidi che legavano la tossina del colera all’esterno. 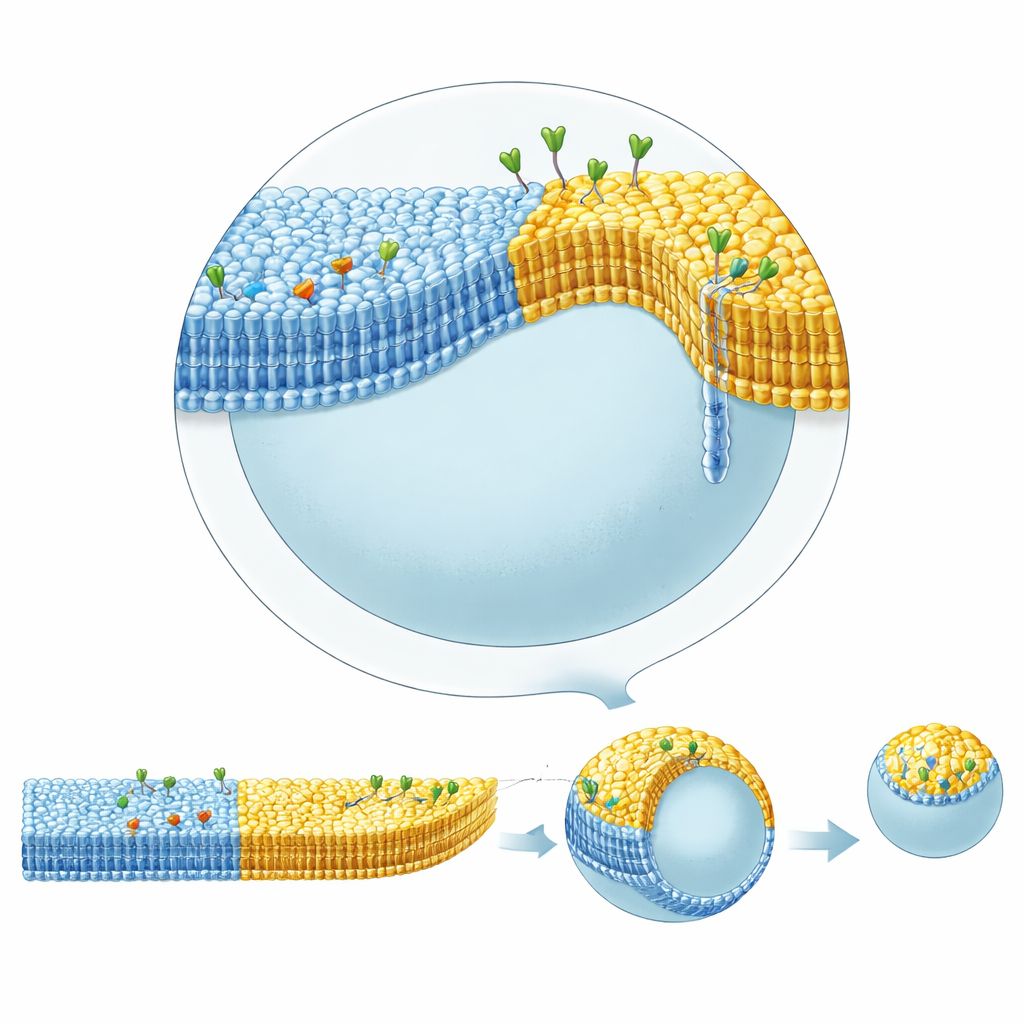
Come proteine e pattern guidano i cambiamenti di forma
Queste vescicole complesse mostrarono dinamiche di forma sorprendenti. Quando la tossina del colera si legava ai glicolipidi nel dominio ordinato sul lato esterno, quel dominio si protendeva verso l’esterno formando una gemma curva collegata da un collo stretto e, sotto una lieve deflazione osmotica, poteva staccarsi interamente come una vescicola figlia. Questa gemmazione non richiedeva molecole energetiche come l’ATP né macchine specializzate per la divisione; nasceva esclusivamente dall’interazione tra composizione lipidica, confini di dominio e legame proteico asimmetrico. Aumentando la quantità di streptavidina legata sul lato interno del dominio disordinato, il gruppo è stato in grado di contrastare la curvatura verso l’esterno del dominio ordinato e ripristinare gradualmente una forma più sferica. Un’analisi geometrica dettagliata dei contorni delle vescicole ha mostrato che la curvatura della membrana salta al confine tra i domini, e che i colli stretti che si formano durante la gemmazione devono resistere a forze di almeno decine di piconewton — quantificando come la struttura dei domini e l’affollamento proteico possano modellare meccanicamente le membrane.
Cosa significa tutto ciò per le future cellule sintetiche
In termini pratici, gli autori hanno sviluppato una ricetta per creare bolle morbide delle dimensioni di una cellula le cui pelli sono patternate e doppio-laterali in modo molto simile alle membrane cellulari reali. Poiché il metodo è relativamente semplice, funziona con molti lipidi diversi e permette di intrappolare proteine e altre grandi molecole all’interno, apre la strada alla costruzione di cellule artificiali più realistiche dal basso verso l’alto. Tali cellule sintetiche potrebbero aiutare gli scienziati a dissezionare come i pattern di membrana controllano segnalazione, traffico e divisione, e potrebbero infine essere impiegate come vettori intelligenti per farmaci che cambiano forma o si dividono su richiesta all’interno del corpo.
Citazione: Yandrapalli, N., Seemann, T., Lipowsky, R. et al. Engineering synthetic cells with intramembrane domains possessing distinct bilayer asymmetries. Nat Commun 17, 2620 (2026). https://doi.org/10.1038/s41467-026-68997-x
Parole chiave: cellule sintetiche, membrane lipidiche, asimmetria della membrana, separazione di fase, gemmazione della membrana