Clear Sky Science · it
Piattaforma nanodisco per glicoproteine virali per l’analisi dei vaccini
Trasformare le proteine virali in bersagli misurabili
I vaccini moderni si basano sempre più su versioni ingegnerizzate con precisione delle proteine che rivestono la superficie dei virus. Queste proteine sono i principali bersagli per gli anticorpi protettivi, tuttavia sono notoriamente difficili da studiare nella loro forma naturale legata alla membrana. Questo articolo descrive una nuova piattaforma di laboratorio che inserisce glicoproteine virali a lunghezza intera in minuscoli frammenti lipidici piatti chiamati nanodischi. Questa configurazione consente agli scienziati di misurare quanto i candidati vaccinali imitino i virus reali, come gli anticorpi vi si legano e come riprogettare questi vaccini per ottenere una protezione migliore.
Perché ricreare la superficie virale è importante
Molte delle proteine virali più rilevanti sono ancorate in una membrana lipidica, proprio come avviene su un virus vero. Gli approcci tradizionali in laboratorio rimuovono la parte di membrana per rendere queste proteine più facili da produrre e purificare in soluzione. Ma quella scorciatoia elimina regioni vicine alla membrana che ospitano bersagli anticorpali particolarmente preziosi, incluso un segmento dell’HIV noto come regione esterna prossima alla membrana (MPER). Queste regioni prossime alla membrana possono apparire e comportarsi in modo diverso quando non sono immerse in un ambiente lipidico realistico, il che significa che frammenti proteici solubili possono offrire un quadro incompleto o fuorviante di come un vaccino si comporterà nell’organismo.
Costruire una piattaforma nanodisco versatile
I ricercatori hanno messo a punto una procedura snella di cinque giorni per prelevare glicoproteine di superficie virali a lunghezza intera da cellule umane, mantenere intatti i loro segmenti transmembrana naturali e reinserirli in un disco lipidico controllato. Hanno prima espresso glicoproteine ingegnerizzate di HIV ed Ebola sulle superfici cellulari, quindi le hanno estratte delicatamente con detergente e catturate su una matrice di purificazione. Mentre le proteine erano ancora legate, hanno aggiunto lipidi definiti e una proteina scaffold a cintura che si auto-assembla in una piccola membrana a forma di disco. Con la rimozione del detergente, le proteine virali si sono sistemate in questi nanodischi. Le preparazioni risultanti erano altamente pure, stabili per mesi in frigorifero e presentavano rivestimenti gliccanici (zuccheri) molto simili a quelli presenti sui picchi virali nativi. 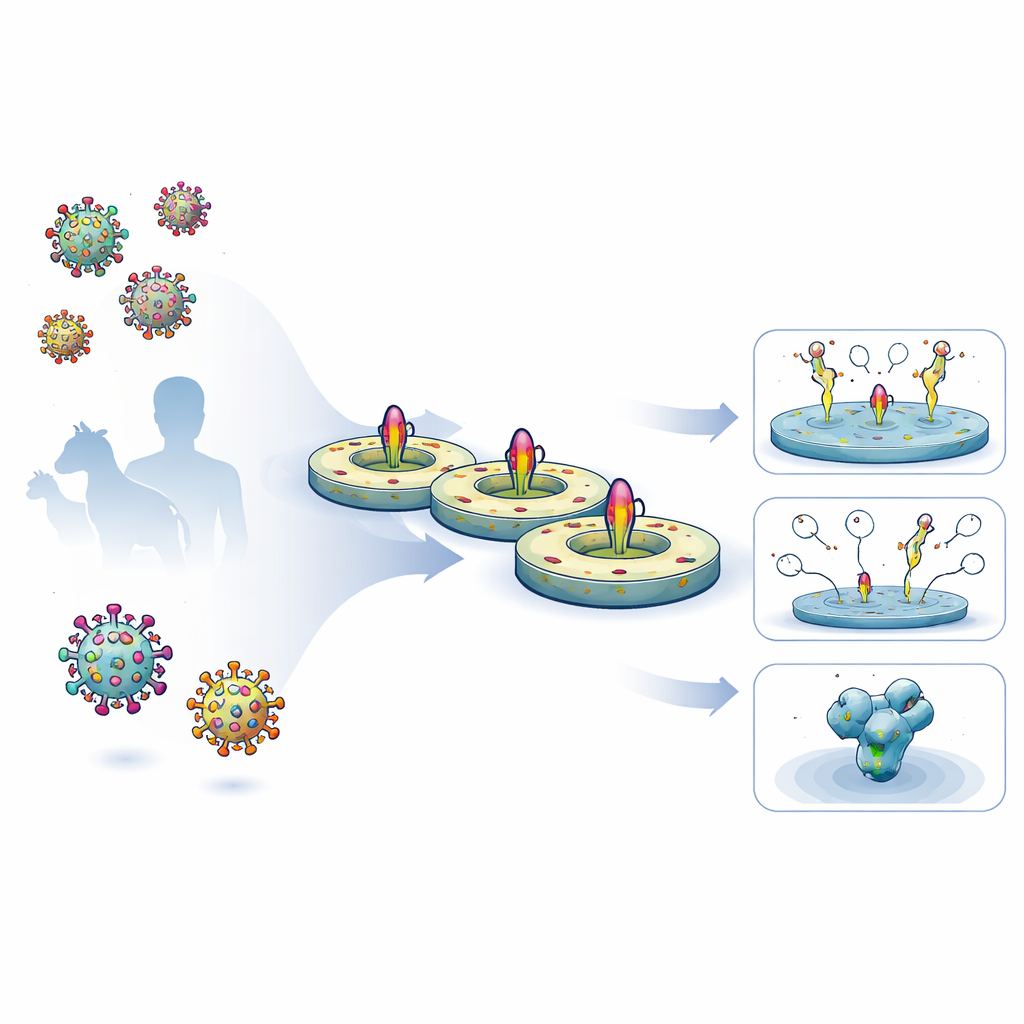
Misurare il legame degli anticorpi e le risposte immunitarie
Con le proteine incapsulate nei nanodischi, il gruppo ha testato quanto diversi anticorpi potessero legarsi usando varie configurazioni di risonanza plasmonica di superficie (SPR), una tecnica che monitora il legame in tempo reale. Utilizzando nanodischi HIV progettati per esporre la regione MPER, hanno mostrato che un potente anticorpo neutralizzante ampio chiamato 10E8 si legava circa 70 volte più strettamente al costrutto ingegnerizzato rispetto a un design precedente, principalmente perché si dissociava molto più lentamente. Mutazioni di controllo che interrompevano la regione MPER eliminarono del tutto il legame di 10E8, confermando che la piattaforma può riportare con sensibilità come le modifiche di design influenzino epitopi chiave. Gli stessi nanodischi hanno funzionato come sonde in citometria a flusso, aiutando a isolare cellule B da topi e scimmie immunizzati che riconoscevano la forma transmembrana completa della proteina HIV, comprese parti assenti dalle sonde solubili standard. 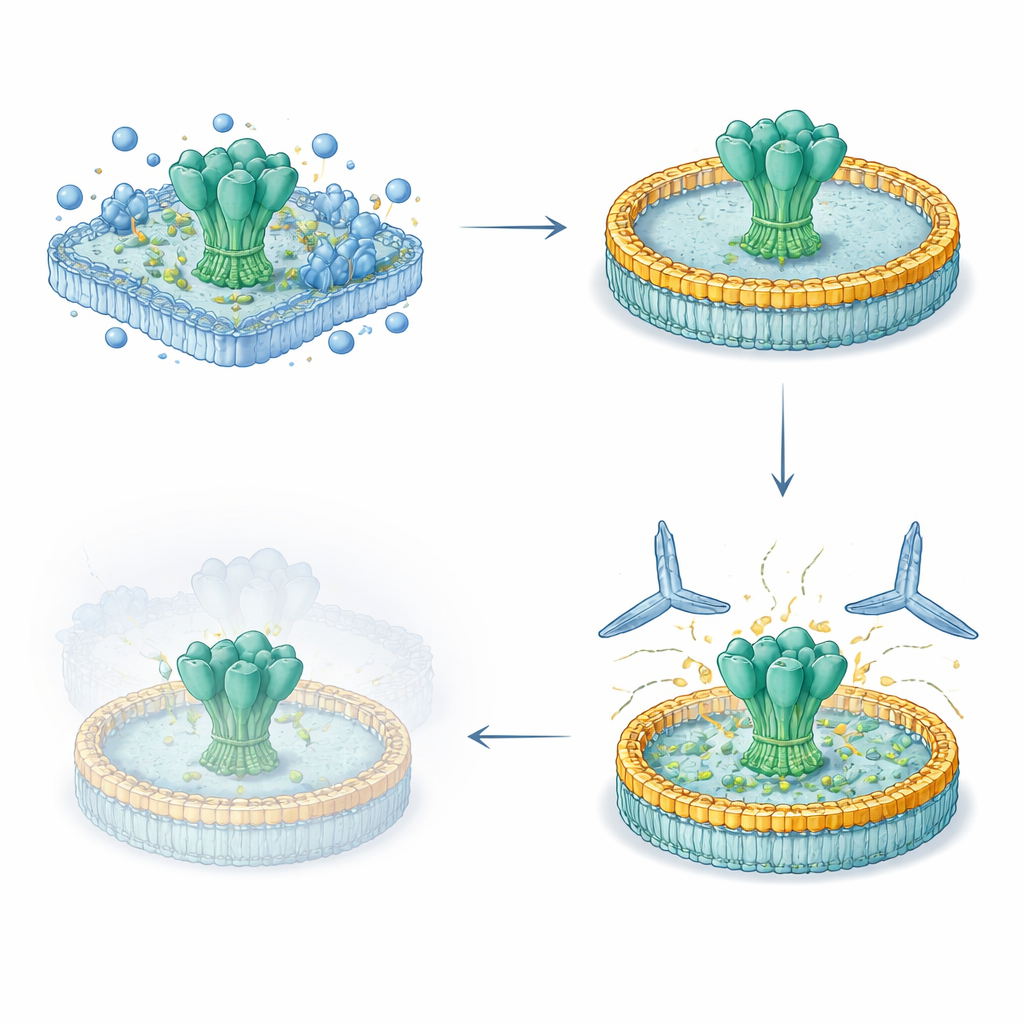
Osservare il bersaglio completo a livello atomico
Per comprendere esattamente come gli anticorpi riconoscano l’MPER nel suo contesto nativo, gli autori hanno usato la microscopia elettronica criofrenata per immaginare i nanodischi HIV ingegnerizzati legati a tre diversi anticorpi neutralizzanti ampi. Hanno ottenuto una struttura a 3,5 angstrom di un anticorpo, 10E8, impegnato con il segmento MPER mentre il resto del picco HIV rimaneva ancorato nel disco lipidico. Ciò ha rivelato una rete continua di contatti tra 10E8 e sia l’MPER sia porzioni vicine della proteina esterna, inclusa una tasca profonda alla giunzione tra due subunità. Confrontando questa struttura con immagini precedenti di 10E8 legato solo a un breve peptide, il gruppo ha mostrato che l’ambiente di membrana e il picco a lunghezza intera consentono contatti supplementari e movimenti dinamici invisibili in modelli più semplici, e che specifici aminoacidi nel virus influenzano fortemente quanto facilmente 10E8 può neutralizzarlo.
Usi ampi per vaccini più intelligenti
In termini pratici, questa piattaforma nanodisco offre ai progettisti di vaccini un modo per valutare candidati vaccinali transmembrana con gli stessi potenti strumenti analitici a lungo riservati ai frammenti proteici solubili. Funziona su virus diversi, supporta misurazioni dettagliate dei legami, consente l’ordinamento e il sequenziamento precisi delle cellule B indotte dal vaccino e produce strutture ad alta risoluzione che catturano epitopi realistici prossimi alla membrana. Per il lettore non specialista, la conclusione è che gli scienziati dispongono ora di un banco di prova più verosimile per le proteine di superficie virali, capace di mostrare quali progetti vaccinali somigliano e si comportano davvero come il virus reale e come modificarli per ottenere risposte anticorpali più forti e più ampie. Questo dovrebbe accelerare lo sviluppo di vaccini di nuova generazione non solo per l’HIV ma per molti altri virus rivestiti.
Citazione: Rantalainen, K., Liguori, A., Ozorowski, G. et al. Virus glycoprotein nanodisc platform for vaccine analytics. Nat Commun 17, 2561 (2026). https://doi.org/10.1038/s41467-026-68985-1
Parole chiave: nanodischi, vaccini HIV, glicoproteine virali, anticorpi neutralizzanti ampi, crio-ME