Clear Sky Science · it
Footprinting radicale nel sangue intero dei mammiferi
Osservare le proteine in azione nel sangue reale
Le proteine nel nostro sangue cambiano continuamente forma mentre svolgono funzioni vitali come combattere le infezioni, trasportare il ferro e rispondere alle malattie. Fino ad ora, la maggior parte degli strumenti per esaminare questi piccoli spostamenti conformazionali ha funzionato solo su campioni semplificati in laboratorio o su cellule isolate. Questo studio dimostra, per la prima volta, che gli scienziati possono leggere la forma delle proteine direttamente nel sangue mammifero intatto, aprendo la strada a osservare i processi patologici così come avvengono realmente nell’organismo.
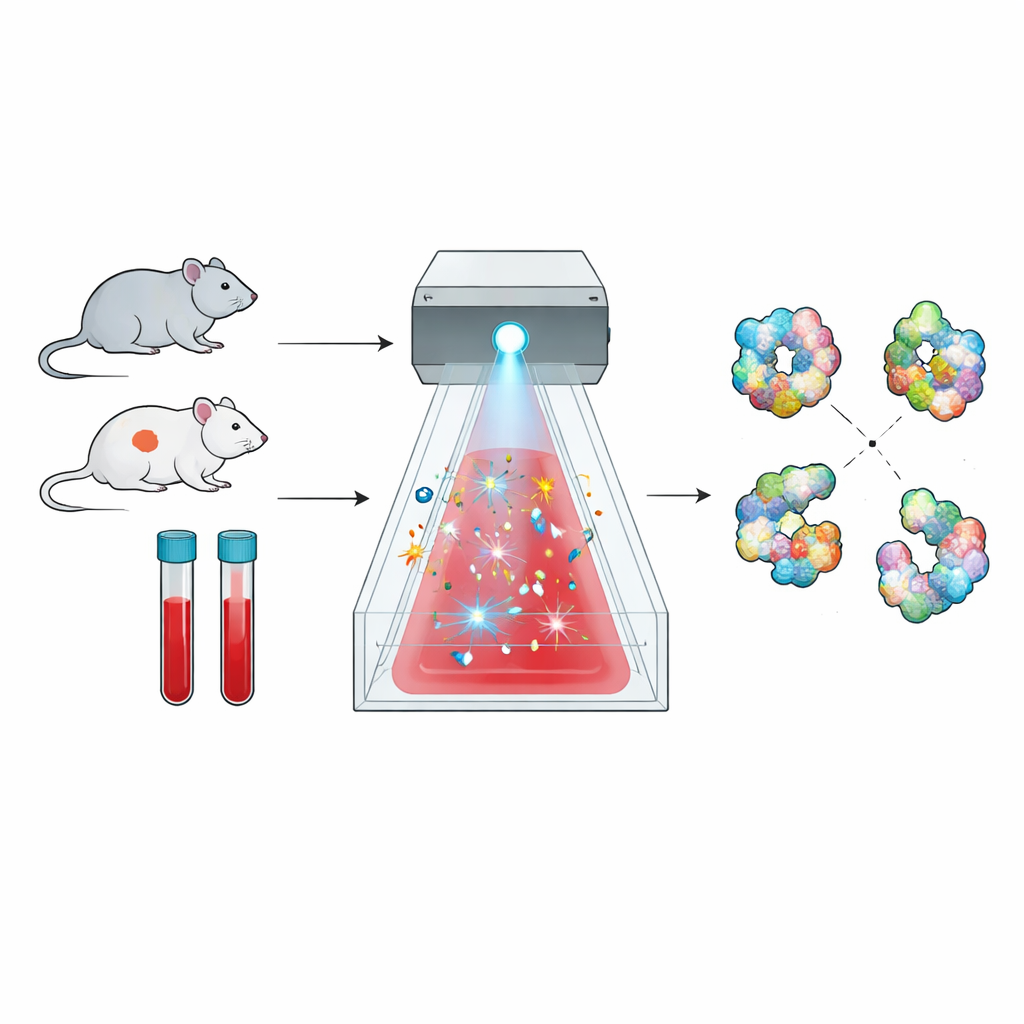
Un nuovo modo per mappare le forme delle proteine
Le proteine non sono perle rigide; si ripiegano in strutture tridimensionali complesse, e tali forme determinano la loro funzione. Il metodo esplorato qui, chiamato radical protein footprinting, sfrutta questo principio. Brevi impulsi di molecole altamente reattive agiscono come un “flash fotografico” chimico, colpendo solo le parti di una proteina esposte al liquido circostante. Successivamente, la spettrometria di massa viene usata per contare dove si sono verificati quegli attacchi chimici, producendo una sorta di mappa superficiale, o impronta, della struttura di ciascuna proteina. Le differenze in quell’impronta tra stati sani e patologici rivelano spostamenti sottili nel ripiegamento della proteina o nelle sue interazioni con partner molecolari.
Far funzionare la tecnica nel sangue intero
Applicare questo approccio direttamente al sangue è stata una sfida di lunga data. Il sangue assorbe fortemente la luce ultravioletta ed è ricco di enzimi, come la catalasi, che distruggono rapidamente i comuni reagenti che generano radicali prima che possano marcare le proteine. I ricercatori hanno risolto il problema passando al persolfato di sodio, che può essere scisso da un brillante flash di luce a banda larga in potenti radicali solfato. Utilizzando un sistema commerciale chiamato FOX, hanno dimostrato che il persolfato può essere attivato in modo affidabile e che una lettura di dosimetria incorporata può tracciare quanti radicali vengono prodotti, permettendo un controllo accurato dell’“esposizione” ricevuta da ciascun campione.
Proteggere le cellule catturando i dettagli
Poiché questo metodo è pensato per studiare le proteine in uno stato prossimo a quello naturale, era cruciale che le cellule del sangue non venissero distrutte. Test sul sangue di topo hanno mostrato che l’aggiunta di persolfato concentrato provocava solo cambiamenti lievi e reversibili nella forma dei globuli rossi e meno del due percento di lisi cellulare, simili a quanto osservato con soluzioni saline semplici. Il team ha inoltre messo a punto una miscela di “quench” migliorata che assorbe rapidamente le specie reattive residue, evitando danni spurii da reazioni laterali più lente dopo il flash. Insieme, questi perfezionamenti hanno permesso di marcare le proteine nel sangue di topo intatto preservando la struttura cellulare e mantenendo molto basso il rumore di fondo.
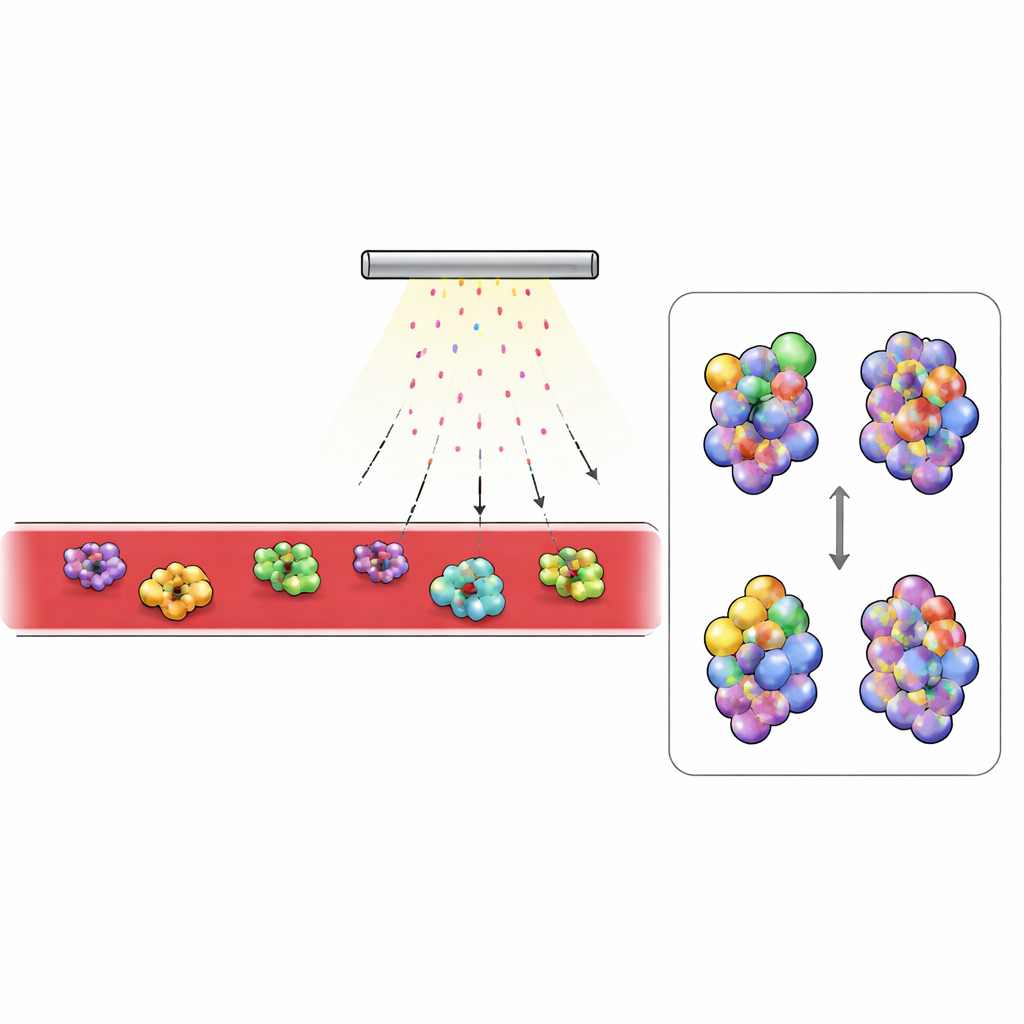
Cosa cambia nel sangue diabetico
Con questa piattaforma a disposizione, i ricercatori hanno confrontato il sangue di topi sani e di un modello comune di diabete di tipo 2. Si sono concentrati sulle proteine più abbondanti rilevate, in particolare quelle circolanti all’esterno delle cellule. Le proteine extracellulari hanno mostrato un’impregnazione molto più intensa rispetto a quelle intracellulari, riflettendo la penetrazione limitata del persolfato negli interni cellulari. Due proteine ematiche sono emerse in modo particolare: il complemento C3, un componente chiave del sistema immunitario, e la transferrina, che trasporta il ferro. Nei topi diabetici, le regioni di C3 che si seppelliscono quando la proteina passa alla sua forma attiva sono risultate meno marcate, mentre regioni normalmente nascoste risultavano più esposte. Questo pattern corrisponde al cambiamento strutturale noto quando C3 viene convertito nel suo frammento attivo, C3b, e analisi ematiche hanno confermato che gli animali diabetici avevano molto più C3 attivato. Nella transferrina, le aree vicino al sito di legame del ferro risultavano più protette nel sangue diabetico, coerente con una maggiore quantità di ferro legata dalla proteina. Misure indipendenti hanno mostrato un ferro sierico più elevato e una frazione maggiore di transferrina saturata di ferro nei topi diabetici.
Perché questo è importante per la salute e la medicina
Per un non specialista, il messaggio essenziale è che gli autori hanno creato un modo per “percepire” le forme di molte proteine contemporaneamente direttamente nel sangue reale, e poi usare quei modelli conformazionali per dedurre come la malattia stia modificando la chimica del corpo. In questo modello murino di diabete di tipo 2, il metodo mette in luce una segnalazione del complemento iperattivata e un carico di ferro maggiore sulla transferrina — cambiamenti che i test classici potrebbero non rilevare o mostrare solo in modo indiretto. Poiché l’approccio funziona con piccoli campioni di sangue e utilizza una sorgente luminosa standardizzata, potrebbe alla fine aiutare a identificare segnali strutturali precoci di malattia, monitorare il comportamento di farmaci biologici nel flusso sanguigno e guidare la progettazione di terapie più efficaci.
Citazione: Zhao, M., Tobin, L., Misra, S.K. et al. Radical footprinting in mammalian whole blood. Nat Commun 17, 2470 (2026). https://doi.org/10.1038/s41467-026-68982-4
Parole chiave: proteomica strutturale, proteine ematiche, diabete di tipo 2, sistema del complemento, metabolismo del ferro