Clear Sky Science · it
Variazioni nel terminale C delle proteine influenzano la proteostasi
Come il terminale delle proteine influisce sulla salute
Ogni proteina nelle nostre cellule termina con una piccola “coda” di appena pochi blocchi costitutivi. Queste code possono sembrare un dettaglio, ma questo studio mostra che decidono silenziosamente quali proteine rimangono e quali vengono rimosse rapidamente. Poiché i livelli proteici sono alla base del cancro, delle malattie genetiche e della risposta cellulare allo stress, comprendere queste code offre nuovi modi per interpretare il rischio di malattia e persino progettare futuri trattamenti.
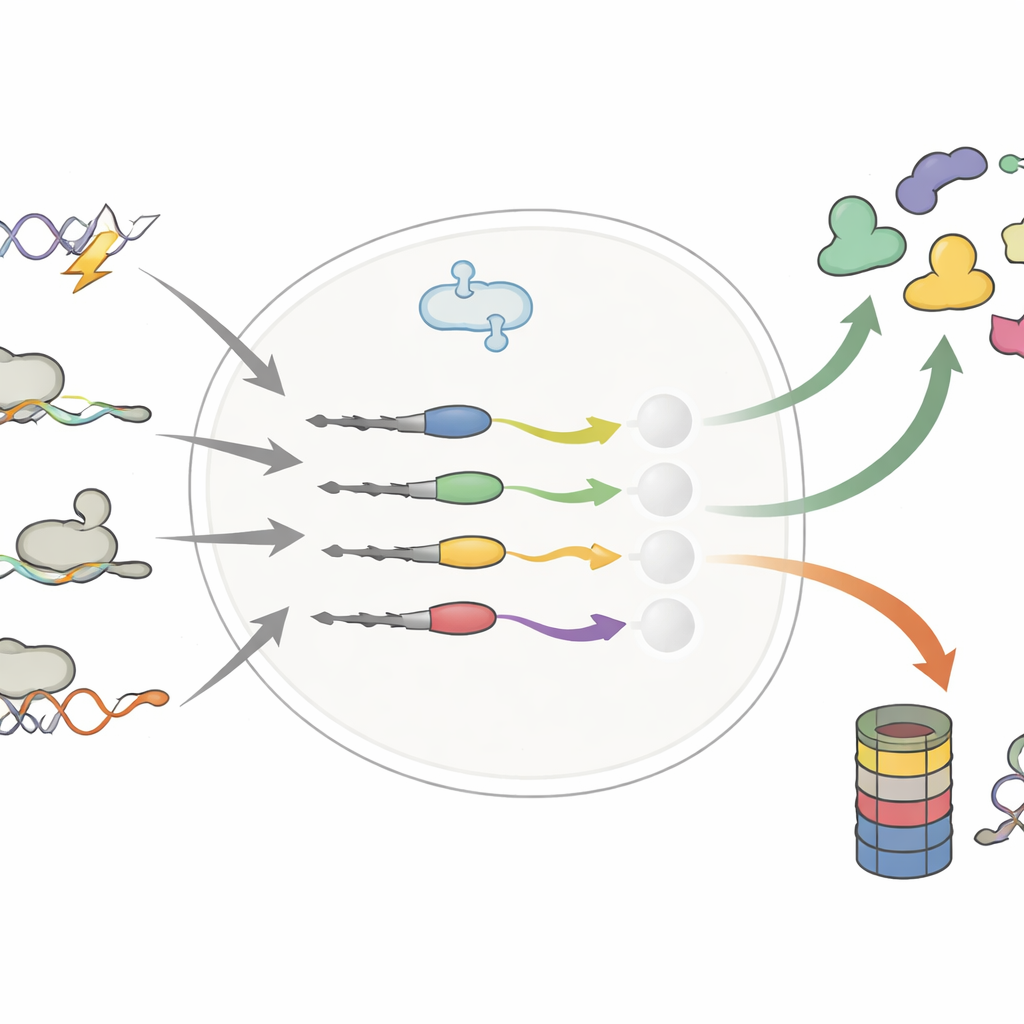
Piccoli cambiamenti alla coda, grandi variazioni nella durata
Gli autori si sono concentrati sull’estremità delle proteine — il C-terminale — dove anche poche aggiunte o sostituzioni di blocchi costitutivi possono comparire a seguito di mutazioni del DNA, splicing alternativo dell’RNA o quando i ribosomi leggono oltre il normale segnale di stop. Studi precedenti suggerivano che tali code “erronee” agissero soprattutto come etichette di smaltimento, inviando le proteine difettose al trituratore della cellula. Confrontando sistematicamente migliaia di code normali e alterate, questo studio ribalta quella visione semplicistica. Il gruppo dimostra che le code alterate possono sia accorciare sia allungare la vita di una proteina, a volte stabilizzando oncoproteine o destabilizzando fattori oncosoppressori.
Quando gli errori genetici aiutano o danneggiano le proteine
Una sorgente principale di cambiamenti della coda sono le mutazioni nonstop, che cancellano un normale segnale di stop così che il ribosoma procede in una porzione di RNA che normalmente resta silente. I ricercatori hanno testato oltre 3.000 varianti nonstop legate a malattie usando un reporter a doppio colore che misura quanto ciascuna coda protegge o indebolisce una proteina modello. In media le code mutate rendevano ancora le proteine meno stabili rispetto alle controparti normali, ma una frazione considerevole ha fatto l’opposto: circa una mutazione nonstop su dieci stabilizzava le proteine, mentre quasi un terzo le destabilizzava. Questi cambiamenti hanno interessato oncoproteine e oncosoppressori noti, implicando che mutazioni apparentemente sottili possono in realtà sbilanciare la crescita e la morte cellulare.
Varietà incorporata da splicing e readthrough
Non tutte le differenze di coda sono incidentali. I nostri geni producono abitualmente più versioni proteiche tramite splicing alternativo e readthrough programmato del codone di stop. Analizzando cataloghi genici umani, gli autori hanno scoperto che quasi due terzi dei geni producono proteine con più di un design di coda, e molte differiscono solo negli ultimi pochi blocchi costitutivi. Testando esempi selezionati, hanno mostrato che queste versioni quasi identiche spesso hanno emivite chiaramente diverse. Alcune code generate dal readthrough rendevano le proteine più stabili, altre meno. Ciò suggerisce che le cellule usano deliberatamente la variazione delle code come una manopola di regolazione fine, adattando quanto a lungo forme proteiche specifiche persistono in tessuti o condizioni diverse.
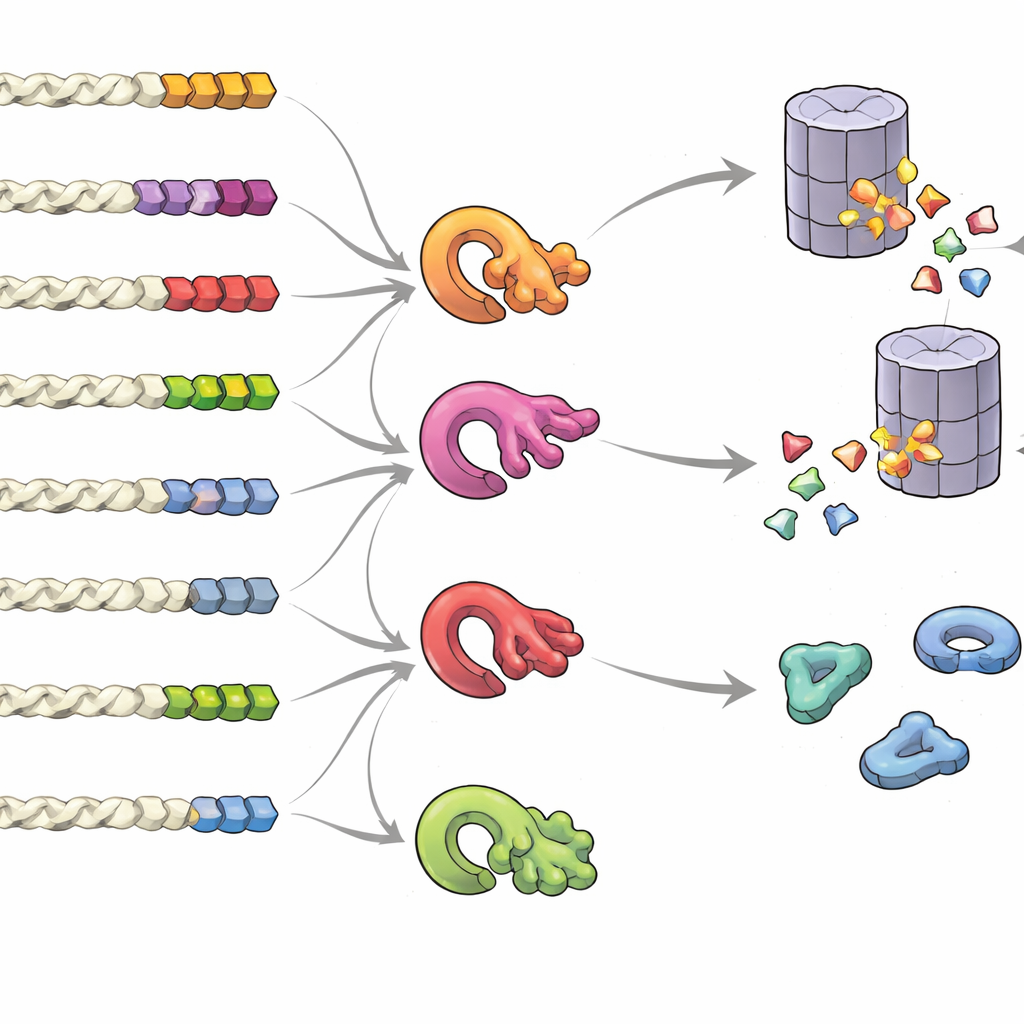
Cosa rende una coda segnale “conservami” o “buttami”
Per capire quali caratteristiche di una coda influenzano il destino proteico, il gruppo ha creato librerie di code casuali e ne ha misurato l’impatto in bulk. Hanno scoperto che non è un singolo “motivo” fisso ma la composizione complessiva, la posizione e il raggruppamento di certi blocchi costitutivi a fare la differenza. Le code ricche di componenti piccole o idrofobiche, o delle più rare cisteina e triptofano, tendevano a favorire la degradazione, specialmente quando questi residui erano raggruppati. Al contrario, code arricchite in residui acidi favorivano la stabilità. Osservando molte specie, le code proteiche normali mostravano chiare tracce di pressione evolutiva per evitare schemi rischiosi, mentre le code derivate da readthrough o frameshift — soggette a errori — erano sbilanciate verso composizioni destabilizzanti. Il gruppo ha anche scoperto che più enzimi di controllo qualità — diverse ligasi dell’ubiquitina — si specializzano nel riconoscere distinti pattern idrofobici delle code, formando una rete intricata che decide quali proteine vengono distrutte.
Perché questo è importante per medicina e biotecnologia
Il lavoro riformula le code proteiche da semplici terminali passivi a regolatori attivi dell’abbondanza proteica. Per un lettore non specialistico, questo significa che molte malattie possono derivare non solo da proteine difettose ma anche da sottili cambiamenti nella durata di vita delle proteine, guidati da piccole differenze alle loro estremità. Avverte inoltre che terapie che promuovono intenzionalmente il readthrough dei segnali di stop, impiegate per trattare alcune malattie genetiche, potrebbero modificare involontariamente le emivite di molte proteine normali. Allo stesso tempo, i risultati suggeriscono nuove strategie potenti: ingegnerizzando sequenze terminali o inducendo le cellule a preferire particolari forme splice o eventi di readthrough, gli scienziati potrebbero un giorno modulare i livelli proteici verso l’alto o verso il basso con notevole precisione.
Citazione: Chu, CY., Hsu, SY., Yeh, CW. et al. Protein C-terminal variations impact proteostasis. Nat Commun 17, 2288 (2026). https://doi.org/10.1038/s41467-026-68979-z
Parole chiave: stabilità proteica, coda C-terminale, degradazione delle proteine, mutazioni genetiche, proteostasi