Clear Sky Science · it
VSIG10L è un determinante chiave dell’omeostasi esofagea e della predisposizione ereditaria all’esofago di Barrett
Perché questo conta per chi soffre di bruciore di stomaco
Il bruciore di stomaco cronico è comune, ma solo una piccola parte delle persone sviluppa l’esofago di Barrett, una condizione che può evolvere in cancro esofageo. Questo studio pone una domanda semplice ma importante: perché alcune famiglie sono molto più predisposte all’esofago di Barrett rispetto ad altre? Tracciando un singolo gene e osservando come modella il rivestimento dell’esofago in uomini e topi, i ricercatori rivelano un anello mancante tra rischio ereditario, danno da reflusso e la capacità dell’organismo di mantenere l’esofago sano.
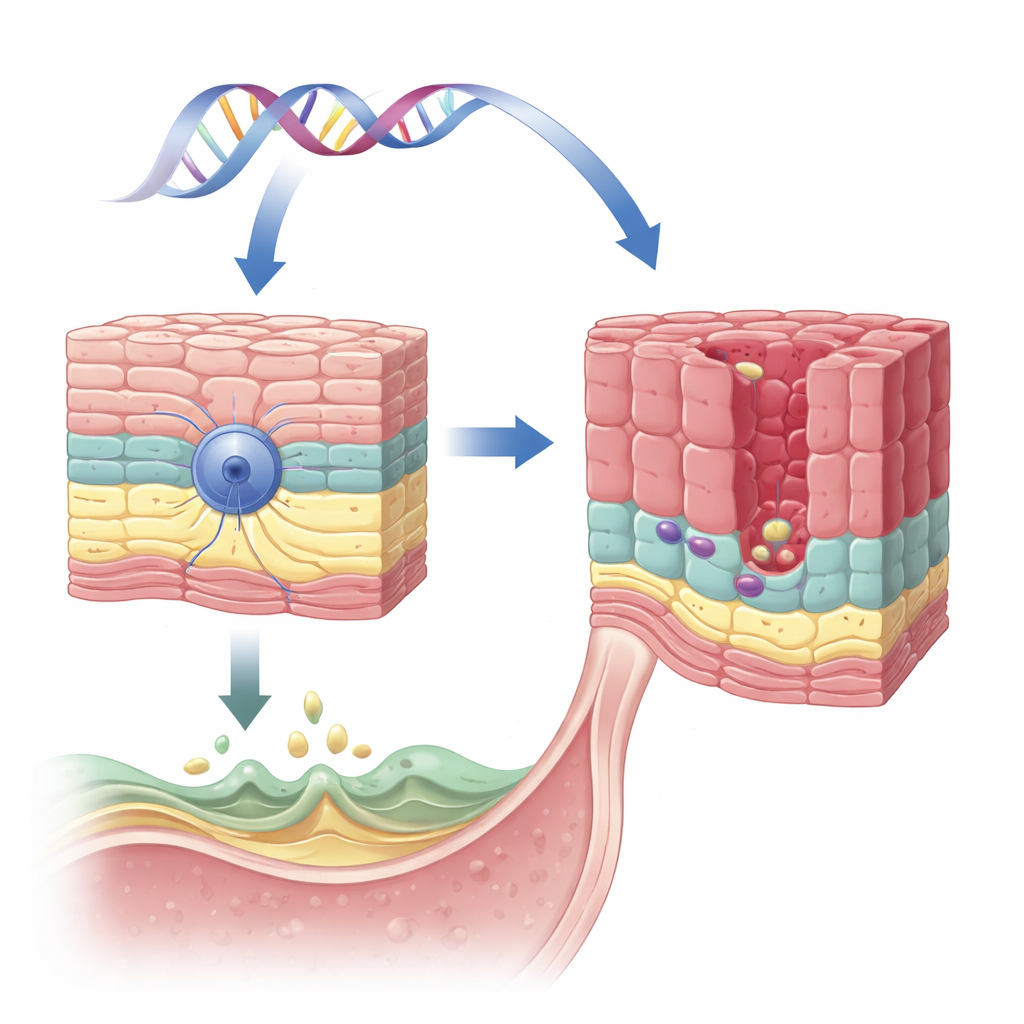
Un gene protettivo nel rivestimento esofageo
Il team si è concentrato su un gene chiamato VSIG10L, precedentemente segnalato in una grande famiglia con molti membri affetti da esofago di Barrett e da tumori correlati. VSIG10L è attivo negli strati superiori delle cellule piatte (squamose) che rivestono l’esofago, ma non nelle cellule basali più profonde e con caratteristiche staminali. Utilizzando un metodo sensibile di rilevazione dell’RNA nei tessuti umani, suino e murino, oltre a colture tridimensionali di cellule esofagee umane, i ricercatori hanno mostrato che VSIG10L è costantemente espresso solo nelle cellule “in maturazione” appena sopra lo strato basale. Questo pattern suggerisce che VSIG10L aiuti le cellule squamose a completare i passaggi finali della loro maturazione e a formare una barriera stabile.
Mutazioni ereditarie che indeboliscono la barriera
Sequenziando il gene VSIG10L in 684 persone provenienti da 302 famiglie con esofago di Barrett e cancro esofageo, gli investigatori hanno individuato diverse varianti rare e dannose. Per testare l’effetto di queste varianti, hanno creato organoidi esofagei derivati da cellule staminali umane di un paziente portatore di una di queste mutazioni. Rispetto agli organoidi di un donatore sano, gli organoidi mutati non sono riusciti a costruire la normale struttura squamosa stratificata. Invece, spesso hanno formato strutture anomale a forma di ghiandola, composte da cellule rimaste in uno stato basale e immaturo, contrassegnato da una proteina chiamata p63. Questa distorsione della stratificazione e della maturazione normale rispecchia i primi passaggi ritenuti precedere l’esofago di Barrett nei pazienti.
Modelli murini che riproducono la malattia umana
Per andare oltre le colture cellulari, il team ha creato topi portatori sia di una copia precisa della mutazione familiare umana in VSIG10L sia di una perdita completa del gene. Nei topi sani, il gene corrispondente Vsig10l è nuovamente attivo solo nelle cellule squamose soprabasali. Al microscopio elettronico, i topi mutanti hanno mostrato una marcata perdita di desmosomi—i piccoli “rivet” che fissano le cellule adiacenti—in questi strati. Le mappe di attività genica dallo stomaco squamoso, una regione murina che assomiglia all’esofago inferiore, hanno rivelato un’ampia alterazione dei programmi strutturali e di differenziazione. Quando i topi sono stati nutriti con una dieta contenente l’acido biliare deossicolico, a imitazione del reflusso cronico, il 70–100% degli animali mutanti Vsig10l ha sviluppato estese chiazze mucinose simili al Barrett alla giunzione squamosa–colonnare, mentre i topi wild-type hanno sviluppato solo lesioni piccole e limitate.
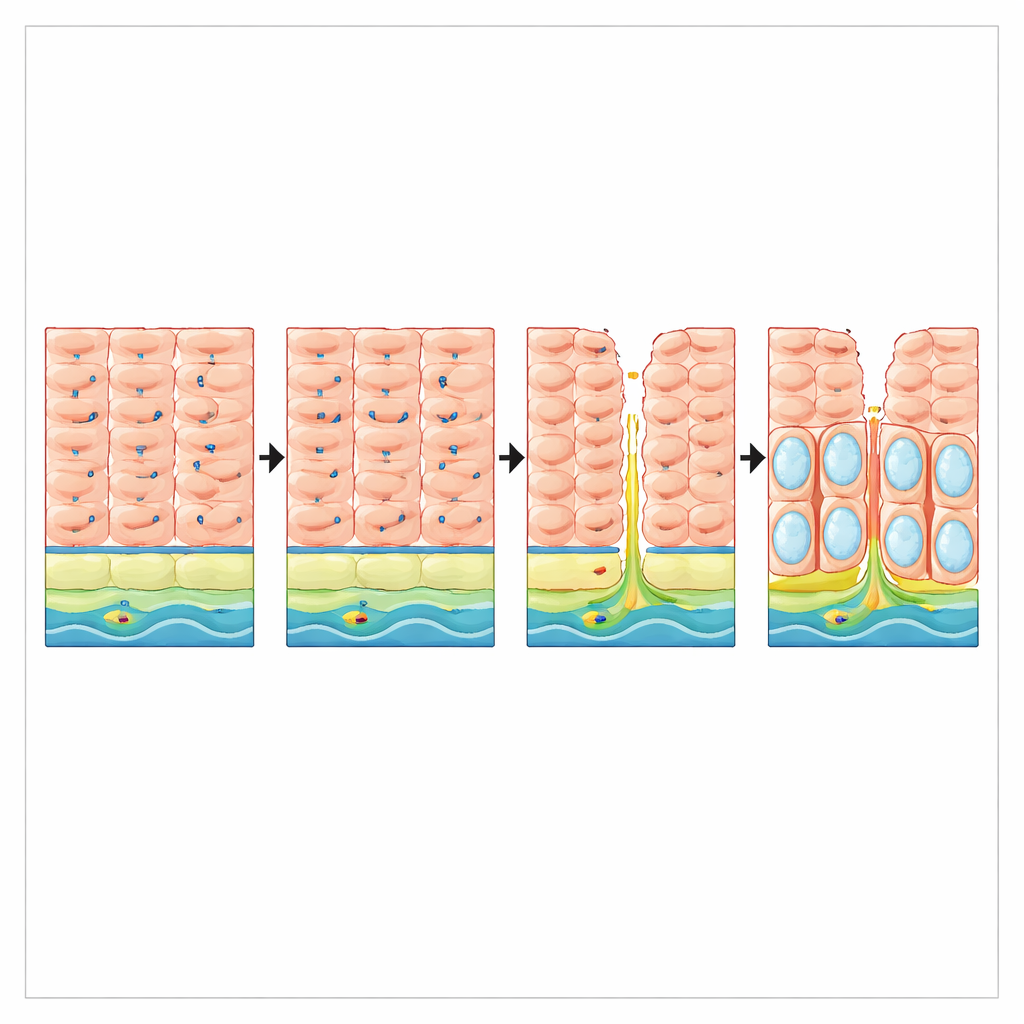
Danno da reflusso e perdita di protezione nei pazienti
I ricercatori si sono poi chiesti se il reflusso potesse disturbare VSIG10L negli esseri umani. In biopsie di pazienti con malattia da reflusso gastroesofageo di lunga durata ma senza esofago di Barrett, i livelli di RNA di VSIG10L erano circa tre volte più bassi rispetto alle persone senza reflusso, nonostante il marcatore basale delle cellule squamose TP63 non risultasse modificato. Nelle sezioni tissutali, il rivestimento esofageo sano mostrava una chiara banda di cellule positive per VSIG10L sopra lo strato basale. Al contrario, la mucosa danneggiata da reflusso presentava un’espansione di cellule di tipo basale ricche di p63 e una quasi completa perdita del gradiente di differenziazione positivo per VSIG10L. Questi risultati suggeriscono che il reflusso cronico erode non solo l’integrità fisica del rivestimento ma anche il programma genico che ne mantiene il rinnovamento ordinato.
Mettere insieme i pezzi
Nel loro insieme, i risultati sostengono un modello semplice: VSIG10L è un guardiano chiave della barriera squamosa esofagea. Difetti ereditari in questo gene, o la sua soppressione acquisita tramite reflusso cronico, portano a una scarsa maturazione del rivestimento, a un numero ridotto di ancoraggi cellula–cellula e a una superficie più permeabile. In questo stato vulnerabile, l’esposizione ripetuta ad acido e bile favorisce una guarigione anomala a carattere ghiandolare invece della restaurazione del rivestimento squamoso originale, predisponendo allo sviluppo dell’esofago di Barrett. Per pazienti e famiglie, questa ricerca indica la strada verso futuri test genetici in grado di segnalare chi è a più alto rischio e verso nuove terapie mirate a preservare o ripristinare la funzione di VSIG10L, con l’obiettivo a lungo termine di prevenire l’esofago di Barrett e la sua progressione a cancro.
Citazione: Ravillah, D., Singh, S., Katabathula, R.M. et al. VSIG10L is a major determinant of esophageal homeostasis and inherited predisposition to Barrett’s esophagus. Nat Commun 17, 2167 (2026). https://doi.org/10.1038/s41467-026-68975-3
Parole chiave: esofago di Barrett, reflusso gastroesofageo, predisposizione genetica, omeostasi epiteliale, rischio di cancro esofageo