Clear Sky Science · it
Sfruttare l’allosteria della fucosiltransferasi umana 8 con un inibitore covalente per sopprimere la fucosilazione core
Perché bloccare un piccolo zucchero può essere importante per il cancro
Le nostre cellule decorano costantemente le proteine con minuscole catene zuccherine che modulano finemente il funzionamento di quelle proteine. Un particolare segnale zuccherino, chiamato fucosilazione core, favorisce la crescita tumorale, la diffusione, l’evasione del sistema immunitario e persino la resistenza ai farmaci oncologici moderni. Questo articolo descrive come gli scienziati abbiano individuato un punto di controllo nascosto sull’enzima umano che aggiunge questo zucchero e messo a punto una nuova molecola a bassa tossicità che si lega a quel punto di controllo per spegnere l’enzima. Il loro lavoro apre una nuova strada per farmaci che riorientano sottilmente gli zuccheri di superficie cellulare invece di attaccare direttamente DNA o proteine.
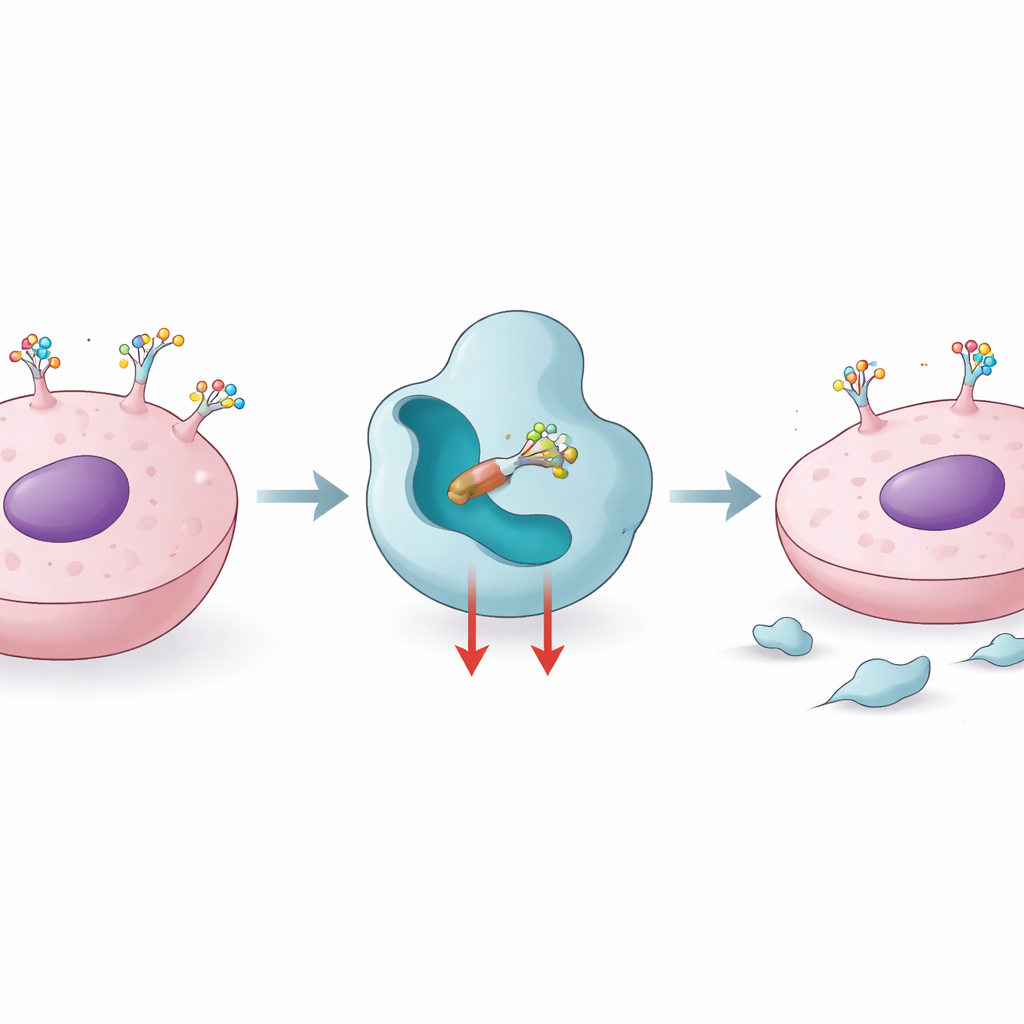
Come le cellule usano tag zuccherini per modellare la malattia
Le proteine che escono dalla “fabbrica” intracellulare attraversano una sorta di linea di finitura molecolare dove le catene zuccherine vengono aggiunte e modificate. La fucosilazione core è uno di questi passaggi finali, eseguito da un enzima chiamato FUT8, che aggiunge una singola unità di fucosio in una posizione chiave su molti glicani legati alle proteine. Quando i livelli di FUT8 aumentano, questo marchio zuccherino diventa più comune su molecole che controllano la crescita cellulare, il movimento e il riconoscimento immunitario. Studi hanno collegato un’elevata attività di FUT8 a melanoma aggressivi, carcinoma mammario triplo negativo, cancro del polmone e resistenza a farmaci mirati e ad alcune terapie con anticorpi. Bloccare FUT8 può rimuovere dalla superficie cellulare alcune proteine che funzionano come freni immunitari, come PD‑1, rendendo i tumori più visibili al sistema immunitario: per questo FUT8 è un bersaglio interessante per l’immunoterapia oncologica e per migliorare farmaci biologici.
La necessità di bloccanti più intelligenti e selettivi
Progettare farmaci contro FUT8 è stato difficile perché molti enzimi correlati utilizzano lo stesso combustibile zuccherino di base. Gli inibitori precedenti spesso imitavano quel combustibile, causando una soppressione ampia e non selettiva di molte vie di fucosilazione e effetti collaterali indesiderati, inclusi problemi di coagulazione che hanno interrotto una sperimentazione clinica. Gli autori hanno ragionato che una strategia migliore sarebbe stata evitare il sito attivo principale molto affollato e cercare invece un sito «remoto» unico su FUT8 che potesse agire come interruttore di controllo. Utilizzando uno screening ad alto rendimento che monitorava l’attività enzimatica, hanno esaminato oltre seimila composti e individuato alcune molecole a catena che rallentavano FUT8 riducendo al contempo l’invasione delle cellule tumorali in coltura.
Scoprire una tasca di controllo nascosta
Con la cristallografia a raggi X, il team ha risolto le strutture tridimensionali di FUT8 legata a due di questi inibitori. Con loro sorpresa, nessuno dei due composti si trovava nella posizione abituale dove si legano il donatore e l’accettore dello zucchero. Invece, entrambi si inserivano in una lunga tasca a forma di canale tra due grandi lobi dell’enzima, vicina ma distinta dal centro attivo. Il legame in questo sito spostava certi anelli e amminoacidi chiave, in particolare elementi che normalmente aiutano a trattenere il donatore di zucchero. Simulazioni al computer hanno mostrato che quando la tasca era occupata, il movimento complessivo e il paesaggio energetico di FUT8 cambiavano, favorendo conformazioni poco efficienti nel catalizzare la reazione. In altre parole, gli inibitori agivano allostericamente: premevano un pulsante distante che provocava il disallineamento delle parti operative dell’enzima.
Trasformare una molecola hit in uno strumento covalente preciso
Con questa mappa strutturale, i ricercatori hanno cercato molecole che non solo potessero occupare la tasca ma anche formare un legame permanente con una lisina vicina (K216) che naturalmente si sposta verso il canale. Hanno scoperto che un reagente chiamato SSO, che porta un estere N‑idrossisuccinimmide reattivo, si legava nello stesso solco e formava un legame covalente con K216, bloccando l’enzima in uno stato inattivo. Sulla base delle caratteristiche comuni di SSO e del loro primo hit NH125, hanno unito frammenti di entrambi per creare una nuova molecola chiamata CAIF. Le strutture cristalline hanno confermato che CAIF si snoda lungo il canale, si inserisce tra residui idrofobici e forma un legame covalente con K216. Questo progetto ha aumentato l’inibizione di FUT8 di diversi ordini di grandezza rispetto ai composti parentali, risparmiando al contempo enzimi strettamente correlati e sottolineando la forma unica della tasca allosterica di FUT8.
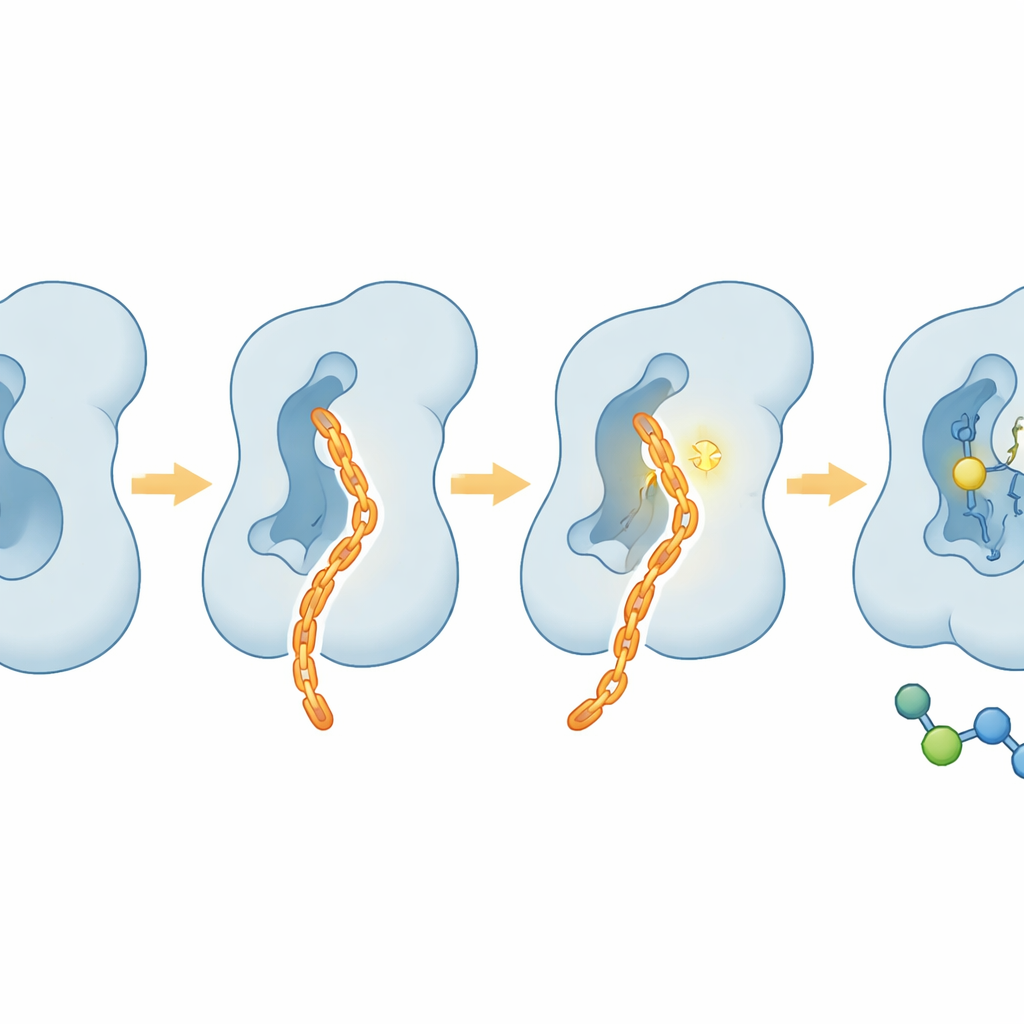
Dolce per le cellule, duro sul comportamento tumorale
Oltre alle provette, il team ha valutato il comportamento di CAIF nelle cellule viventi. In diverse linee cellulari umane, CAIF ha mostrato tossicità minima anche a dosi elevate, suggerendo che non avvelena ampiamente i macchinari cellulari. Eppure ha ridotto marcatamente la fucosilazione core sulla superficie cellulare, come rivelato da coloranti leganti gli zuccheri, e lo ha fatto con molta maggiore selettività per FUT8 rispetto ai precedenti inibitori non specifici. Nei saggi di invasione cellulare, CAIF ha superato un comune bloccante a base di zuccheri nel limitare la capacità delle cellule tumorali di migrare attraverso una matrice, un marchio della potenziale metastasi. Questi effetti sono coerenti con il ruolo noto di FUT8 nell’aumentare invasività ed evasione immunitaria piuttosto che nel guidare direttamente la divisione cellulare.
Cosa significa questo per i futuri trattamenti contro il cancro
Questo studio non sostiene che CAIF sia pronto per diventare un farmaco. Piuttosto dimostra che FUT8 contiene una tasca allosterica precedentemente sconosciuta e sfruttabile farmacologicamente, che può essere mirata con molecole sagomate in modo preciso che formano un legame durevole con una singola lisina. Sfruttando questo sito, i ricercatori possono modulare selettivamente un enzima che modifica gli zuccheri e si trova all’incrocio della progressione tumorale, dell’evasione immunitaria e della resistenza ai farmaci, lasciando in gran parte intatti gli enzimi correlati. Il lavoro offre un progetto per la progettazione di inibitori di nuova generazione che rimodellano i pattern zuccherini rilevanti per la malattia sulle proteine e che potrebbero, in ultima analisi, ampliare gli strumenti disponibili per l’immunoterapia oncologica e il miglioramento degli anticorpi terapeutici.
Citazione: Jiang, J., He, D., Ke, M. et al. Exploiting human fucosyltransferase 8 allostery with a covalent inhibitor for core fucosylation suppression. Nat Commun 17, 2607 (2026). https://doi.org/10.1038/s41467-026-68971-7
Parole chiave: Inibizione FUT8, fucosilazione core, inibitori allosterici covalenti, glicosilazione nel cancro, progettazione di farmaci per glicosiltransferasi