Clear Sky Science · it
FANCD2 limita la progressione delle forcelle e previene la fragilità alle origini precoci durante la ri-replicazione
Quando le copie del DNA escono leggermente dal copione
Ogni volta che una cellula si divide, deve copiare l'intero patrimonio di DNA esattamente una sola volta. Se parti di quel patrimonio vengono copiate due volte, o copiate in modo frettoloso e approssimativo, il risultato può essere cromosomi spezzati e mutazioni che alimentano il cancro. Questo studio esamina cosa accade quando i meccanismi di salvaguardia contro turni di copia extra cominciano a fallire, rivelando come una proteina di riparo chiamata FANCD2 intervenga per impedire che cellule con un comportamento scorretto moderato scivolino nel caos genomico completo.
Parapetti per una copia pulita
I nostri cromosomi vengono duplicati da migliaia di punti di partenza, o “origini”, che vengono autorizzati e poi attivati in una sequenza temporale accurata. Una piccola proteina chiamata Geminin normalmente aiuta a garantire che ogni origine si attivi una sola volta per ciclo cellulare. Quando Geminin viene persa o indebolita, alcune origini possono riattivarsi su DNA già copiato, una situazione nota come ri-replicazione. Le cellule tumorali, che spesso sovraproducono fattori di licensing, sono particolarmente soggette a questo problema. Gli autori hanno prima utilizzato uno screening genetico ad alto contenuto in cellule umane predisposte a una ri-replicazione di basso livello mediante deplezione di Geminin. Hanno indagato quali geni di riparazione del DNA e del checkpoint diventano cruciali in questo stato di stress e hanno trovato che FANCD2, nota soprattutto per riparare incrociamenti del DNA nella anemia di Fanconi, emerge come un protettore chiave della sopravvivenza cellulare e dell'integrità del genoma.
Un primo intervento alle macchine di copia sovraccariche
Il gruppo ha quindi seguito dove e quando FANCD2 compare nelle cellule in ri-replicazione. Poco dopo la rimozione di Geminin, FANCD2 si accumula rapidamente sulla cromatina e forma brillanti fuochi nucleari, molto prima che sia rilevabile una diffusa rottura del DNA. Usando marcature del DNA neo-sintetizzato insieme ad assay di prossimità, hanno mostrato che FANCD2 viene reclutato direttamente alle macchine di replicazione attive, specialmente nelle cellule il cui DNA è già in corso di seconda copiatura. In cellule sincronizzate rilasciate nel ciclo di divisione successivo, è emersa una popolazione distinta con un pattern diffusamente eccedente di DNA replicato. Queste cellule mostravano forti segnali di FANCD2 e RPA, indicatori di stress di replicazione in corso, e venivano trattenute al confine prima della mitosi da un checkpoint attivo, suggerendo che FANCD2 faccia parte di una risposta precoce che stabilizza le forcelle sotto stress piuttosto che limitarsi a reagire al DNA spezzato.
Frenare forcelle in fuga e lacune nascoste
Per valutare come FANCD2 modelli la copiatura del DNA, i ricercatori hanno combinato la perdita di Geminin con la deplezione di FANCD2. Sorprendentemente, la rimozione di FANCD2 non ha aumentato la frazione di cellule con genomi evidentemente ri-replicati. Al contrario, saggi su fibre di DNA a singola molecola hanno rivelato che le forcelle di replicazione percorrevano distanze maggiori e diventavano più asimmetriche, segno di progressione diseguale e instabile. Queste forcelle più veloci lasciavano dietro di sé più lacune a singolo filamento nel DNA appena sintetizzato, visibili come intensi focolai di RPA e BrdU nativo e confermate dalla sensibilità dei tratti marcati a un enzima che taglia regioni a singolo filamento. Le cellule prive sia di Geminin sia di FANCD2 mostravano un aumento di rotture cromosomiche, frammenti, corpi nucleari e micronuclei, tutti segnali di grave instabilità genomica. Il blocco di PARP, un fattore che normalmente aiuta a gestire tali lacune, ha imitato e peggiorato questi difetti, sottolineando che la formazione incontrollata di lacune è centrale per il danno.
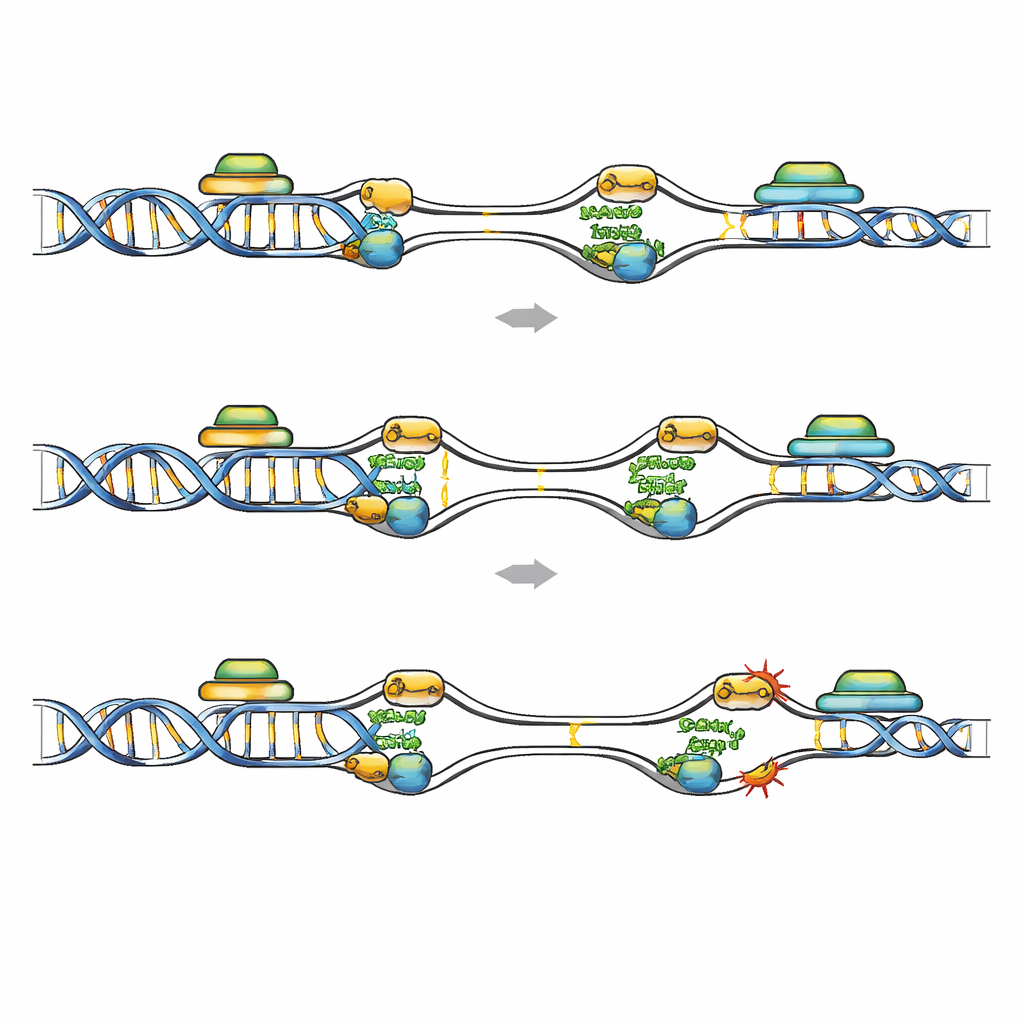
Punti caldi fragili dove copia e trascrizione si scontrano
La mappatura del genoma degli legami di FANCD2 ha mostrato dove la ri-replicazione è più pericolosa. In cellule leucemiche deplete di Geminin, FANCD2 si è spostata dai classici siti fragili comuni verso origini di replicazione a attivazione precoce inserite all'interno di geni brevi, ricchi in GC e altamente trascritti. Queste regioni portano marche di trascrizione attiva e sono predisposte alla formazione di R-loop, dove l'RNA nascente ibrida con il suo stampo di DNA, potenzialmente bloccando la replicazione. Dataset pubblici hanno mostrato più danno al DNA e segnali elevati di ibridi RNA–DNA nei geni arricchiti di FANCD2 dopo la perdita di Geminin, e queste regioni si sovrapponevano con i cosiddetti siti fragili a replicazione precoce. Quando la trascrizione è stata ampiamente attenuata con un farmaco, o quando gli R-loop sono stati specificamente rimossi sovraesprimendo RNase H1, il numero di focolai di FANCD2, RPA e danno al DNA nelle cellule carenti di Geminin è diminuito notevolmente. Questo indica che le collisioni tra origini riattivate e unità trascrizionali attive, amplificate dagli R-loop, creano punti caldi fragili che FANCD2 deve proteggere.
Affinare la protezione tramite tag chimici
FANCD2 viene attivata in parte dall'attacco di un piccolo tag simile all'ubiquitina. Depletando FANCA, un componente centrale della macchina di marcatura, e usando cellule che esprimono un mutante di FANCD2 resistente a questa modificazione, gli autori hanno mostrato che la mono-ubiquitinazione migliora la sopravvivenza delle cellule in ri-replicazione ma non è assolutamente necessaria. Anche FANCD2 non marcata forniva una protezione parziale, coerente con ruoli distinti sia nel riconoscere sia nello stabilizzare le forcelle sotto stress. Il quadro complessivo è che FANCD2 aiuta a rallentare e organizzare la replicazione alle origini precoci più vulnerabili e limita quante e quanto grandi diventino le lacune a singolo filamento.
Perché questo è importante per la terapia del cancro
Per i non specialisti, il messaggio principale è che non tutti gli errori di replicazione sono catastrofici fin dall'inizio. La ri-replicazione lieve, come accade in alcuni tumori, può essere tollerata se sistemi protettivi come FANCD2 tengono sotto controllo la copia incontrollata del DNA e impediscono che le lacune fragili si trasformino in cromosomi spezzati. Quando questa salvaguardia viene rimossa o sopraffatta, gli stessi errori di licensing a basso livello si trasformano rapidamente in frantumazione del genoma. Poiché la perdita di Geminin e i difetti del licensing della replicazione sono arricchiti nelle cellule tumorali, e molti tumori presentano già debolezze nella rete Fanconi/BRCA, le vulnerabilità qui svelate suggeriscono strategie terapeutiche: combinare inibitori che spingono le cellule tumorali verso la ri-replicazione con farmaci che esacerbano l'accumulo di lacune, come gli inibitori di PARP, potrebbe spingere selettivamente le cellule maligne oltre il loro limite di tolleranza, risparmiando le cellule normali con protezioni intatte.
Citazione: Badra-Fajardo, N., Karydi, E., Bayona-Feliu, A. et al. FANCD2 restrains fork progression and prevents fragility at early origins upon re-replication. Nat Commun 17, 2478 (2026). https://doi.org/10.1038/s41467-026-68966-4
Parole chiave: Stress della replicazione del DNA, FANCD2, Geminin, ri-replicazione, instabilità genomica