Clear Sky Science · it
Il ripiegamento indotto dall’associazione governa l’assemblaggio del light chain surrogato e del core del recettore pre‑B
Come il nostro corpo mette alla prova i nuovi anticorpi
Prima che una cellula B giovane nel midollo osseo sia autorizzata a entrare a far parte del sistema immunitario, deve superare una prova severa: è in grado di costruire un nucleo anticorpale funzionante? Questo articolo esplora come una versione “di prova” di una parte dell’anticorpo, chiamata catena leggera surrogata, contribuisca a svolgere quel test. Osservando come queste proteine si ripiegano e si incastrano, gli autori rivelano un sistema nascosto di controllo qualità che decide quali futuri anticorpi sono abbastanza validi da essere mantenuti e quali vengono scartati.
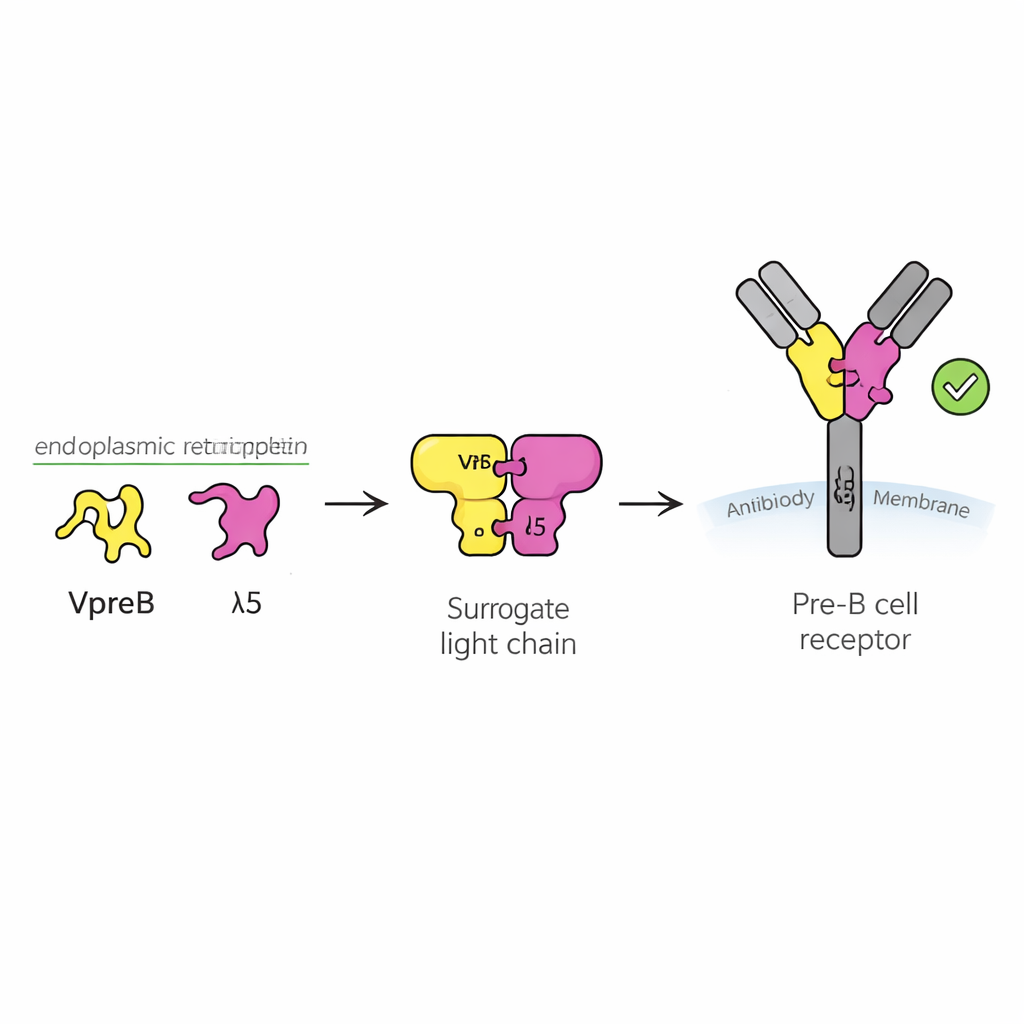
Un punto di controllo di sicurezza per le giovani cellule immunitarie
Gli anticorpi sono proteine a forma di Y che riconoscono i germi invasori. Sono costruiti da due parti principali: catene pesanti e catene leggere. Durante lo sviluppo delle cellule B, la catena pesante viene prodotta per prima, e la cellula deve stabilire se questa nuova catena pesante è utile prima di investire energia nella produzione di una catena leggera corrispondente. Per farlo, la cellula utilizza un sostituto temporaneo chiamato catena leggera surrogata, composta da due proteine denominate VpreB e λ5. Insieme alla catena pesante formano il recettore pre‑B, un sensore sulla superficie cellulare che invia un segnale di “vai” o “stop”. Circa la metà delle catene pesanti appena riassemblate fallisce questo test, quindi capire come funziona la catena leggera surrogata è fondamentale per comprendere come si costruisce un repertorio anticorpale sano.
Ripiegamento per associazione: aiutare un partner instabile
Gli autori hanno scoperto che una componente, VpreB, è in gran parte non ripiegata e instabile quando è da sola. Utilizzando tecniche biofisiche, hanno mostrato che essa assume la sua struttura tridimensionale corretta solo quando si lega a λ5. Un breve tratto di λ5, dalla forma di uno strand beta, si inserisce in VpreB e completa la sua struttura, come inserire un dente mancante in un ingranaggio. Questo “ripiegamento indotto dall’associazione” non solo stabilizza VpreB, ma crea anche una partnership molto stretta tra le due proteine, con un’affinità nell’ordine dei nanomolari bassi. Nelle cellule, solo quando VpreB e λ5 si assemblano in questa catena leggera surrogata sfuggono alla ritenzione nel reticolo endoplasmatico e vengono secrete o trasferite oltre, sottolineando come ripiegamento e controllo qualità siano strettamente collegati.
Completare la catena pesante e superare l’ispezione
La storia non finisce con VpreB e λ5. Una regione cruciale della catena pesante, chiamata CH1, è inizialmente non strutturata e trattenuta all’interno della cellula. I ricercatori hanno mostrato che λ5, agendo in parte come una chaperone, può indurre il ripiegamento di CH1 quando si lega ad essa. Questo secondo passaggio di ripiegamento indotto dall’associazione è essenziale per costruire il recettore pre‑B completo e permetterne l’uscita dal reticolo endoplasmatico fino alla superficie cellulare. Interessantemente, entrambe le parti della catena leggera surrogata — VpreB e λ5 — possono entrare in contatto con la catena pesante, ma solo λ5 è in grado di spingere CH1 verso il suo stato finale, ripiegato e competente. Quando ciò non avviene, il recettore parziale viene trattenuto e la cellula respinge effettivamente quella catena pesante.
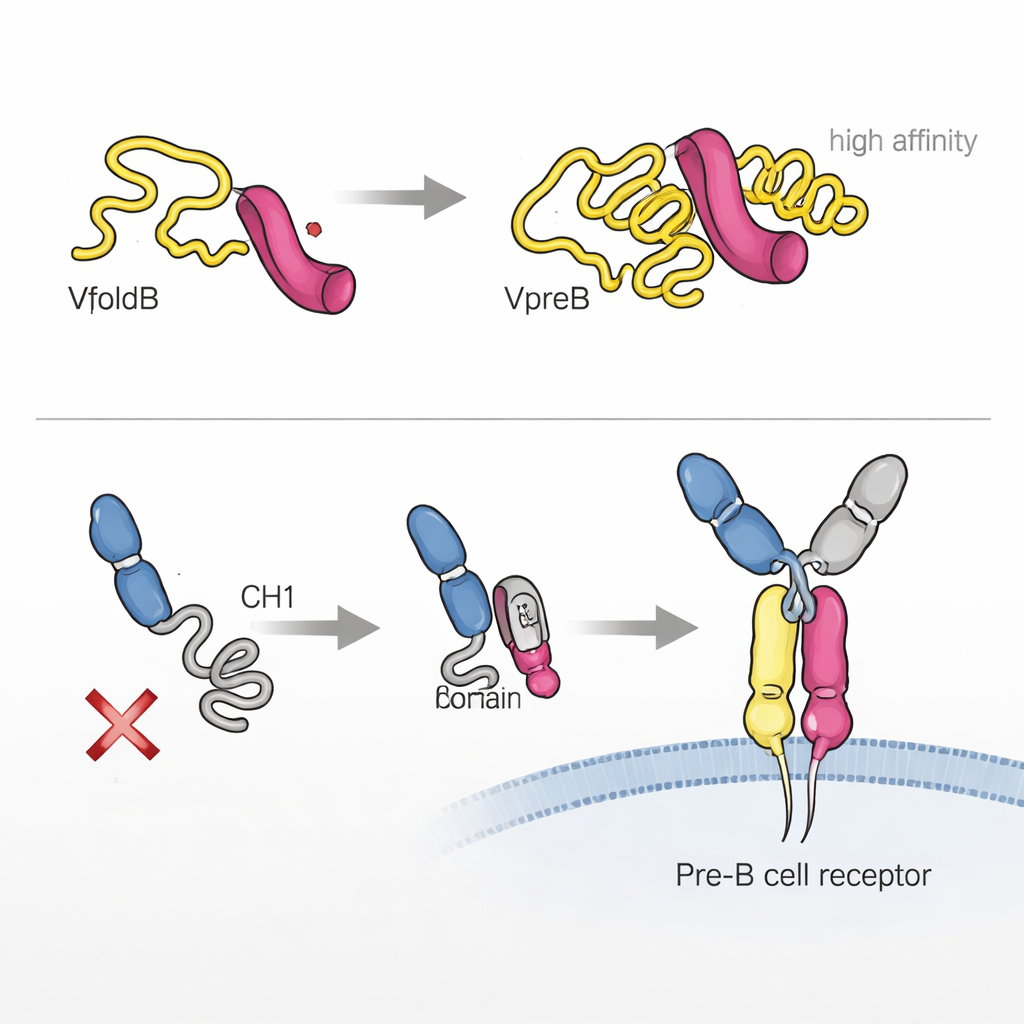
Code flessibili che affinano il legame e la segnalazione
Sia VpreB che λ5 portano segmenti flosci e non strutturati noti come regioni uniche, che non somigliano a nessuna sequenza proteica nota. Sebbene queste code non siano strettamente necessarie perché le due proteine si assemblino in vitro, il team ha scoperto che influenzano fortemente la velocità di formazione della catena leggera surrogata, la sua stabilità e quanto bene si lega a segmenti della catena pesante. Nelle cellule, la rimozione di queste regioni ha ridotto l’efficienza con cui i complessi assemblati venivano secreti. In particolare, la coda di λ5 si è rivelata multitasking: accelera l’assemblaggio, è essenziale per certi contatti con la regione variabile della catena pesante e contribuisce in modo sostanziale a come il recettore pre‑B interagisce con antigeni e altri ligandi. In alcuni casi, l’affinità di legame di una combinazione catena leggera surrogata–catena pesante si è avvicinata a quella di un frammento anticorpale normale.
Perché questo è importante per la diversità degli anticorpi
Mappando questi eventi di ripiegamento e assemblaggio passo dopo passo, gli autori propongono che la catena leggera surrogata faccia più che semplicemente tenere la catena pesante in posizione. Funziona come un ispettore dinamico, usando il suo nucleo strutturato e le code flessibili per rilevare se una catena pesante può ripiegarsi correttamente e interagire produttivamente con bersagli potenziali. Le combinazioni riuscite vengono ripiegate, stabilizzate e autorizzate a raggiungere la superficie cellulare, dove inviano segnali che permettono alla cellula B di continuare la maturazione. Le combinazioni difettose vengono intrappolate ed eventualmente eliminate. Per il lettore non specialista, il messaggio è che il tuo sistema immunitario esegue un sofisticato “banco di prova” per i futuri anticorpi, costruito da proteine che letteralmente si ripiegano a vicenda, assicurando che solo i nuclei anticorpali ben comportati vadano avanti per difenderti.
Citazione: König, J., Sarmiento Alam, N.C., He, R. et al. Association-induced folding governs surrogate light chain and pre-B cell receptor core assembly. Nat Commun 17, 1202 (2026). https://doi.org/10.1038/s41467-026-68965-5
Parole chiave: Sviluppo delle cellule B, ripiegamento degli anticorpi, catena leggera surrogata, controllo qualità delle proteine, recettore pre‑B