Clear Sky Science · it
Sbloccare la deracemizzazione enzimatica di alleni strutturalmente diversi mediante fotoenzimi progettati
Perché mescolare e abbinare le molecole conta
Molti farmaci funzionano solo quando i loro atomi sono disposti in un modo tridimensionale molto specifico, come una mano sinistra che entra in un guanto sinistro ma non in uno destro. I chimici possono spesso sintetizzare queste molecole “a mano unica”, ma è difficile farlo in modo pulito quando i mattoncini di partenza sono complessi. Questo articolo affronta quella sfida per una classe difficile di strutture attorcigliate chiamate alleni, utilizzando enzimi progettati che sfruttano la luce. Il lavoro mostra come biologia e fotochimica possano essere combinate per selezionare la “mano” molecolare desiderata da una miscela caotica, promettendo vie più rapide e pulite verso futuri farmaci e materiali.
Mattoncini attorcigliati con grande ricompensa
Gli alleni sono sequenze lineari di tre atomi di carbonio con due doppi legami adiacenti, ma questa disposizione semplice incurva lo spazio in modo che la molecola nel suo complesso acquisti una chiralità. Questi twist assiali compaiono in prodotti naturali, agenti per la protezione delle colture e catalizzatori avanzati. Sfortunatamente, i metodi tradizionali per ottenere alleni chirali tendono a essere altamente specializzati: un catalizzatore che funziona benissimo per un allene spesso fallisce per un altro con piccole modifiche strutturali. Anche i catalizzatori chimici attivati dalla luce sviluppati di recente incontrano questo problema. Di conseguenza, i chimici devono riprogettare ripetutamente i catalizzatori da zero quando esplorano nuovi alleni, rallentando la scoperta e aumentando gli scarti.
Prendere in prestito la selettività della natura e aggiungere la luce
Gli enzimi nei sistemi viventi eccellono nel riconoscere e trasformare forme specifiche con una precisione notevole, ma si sono evoluti per bersagli naturali, non per alleni sintetici. Gli autori hanno cercato di creare un “fotoenzima” che combini la selettività tipica degli enzimi con la capacità di utilizzare la luce come sorgente di energia. Sono partiti da un’impalcatura proteica chiamata CTB10 e l’hanno geneticamente modificata per inserire un amminoacido non naturale che funziona come una piccola antenna luminosa incorporata. Quando questo speciale componente assorbe luce ultravioletta, può trasferire energia a un allene vicino, eccitandolo temporaneamente e consentendo che il suo twist venga rimescolato. Ripetendo questo processo molte volte, l’enzima può rimuovere selettivamente una mano da una miscela 50:50 e lasciare principalmente l’altra. 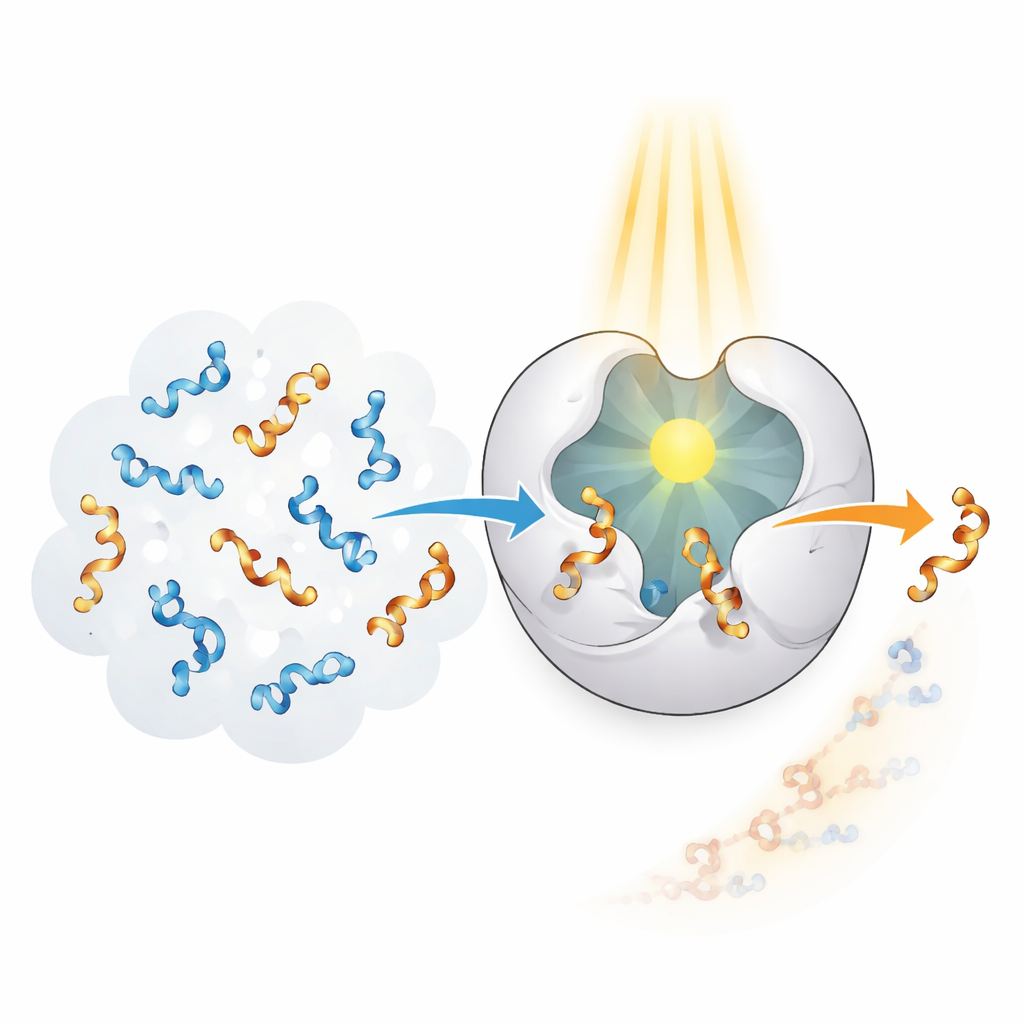
Intagliare tasche su misura per ospiti diversi
Progettare un tale sistema non è semplice come illuminare una proteina. Il team ha usato modellizzazione al computer, mutazioni strategiche e immagini a raggi X per scolpire diverse versioni del fotoenzima, ciascuna con una tasca interna leggermente diversa. Queste tasche tengono l’allene in una posa definita accanto all’antenna luminosa e stabilizzano parti chiave della molecola tramite legami idrogeno e interazioni sottili di impaccamento. Passo dopo passo, i ricercatori hanno migliorato sia la forza di legame sia l’allineamento tra enzima e allene, elementi cruciali per un trasferimento di energia efficiente. Le varianti finali hanno mostrato prestazioni impressionanti, convertendo acidi carbossilici, esteri e ammidi di allene in prodotti a mano singola con purezza molto elevata, spesso superiore al 99% di una mano, e operando all’aria senza bisogno di condizioni delicate.
Osservare il meccanismo a risoluzione atomica
Per capire perché i nuovi fotoenzimi preferiscono una mano rispetto all’altra, gli autori hanno cristallizzato coppie enzima‑substrato e le hanno esaminate a risoluzione atomica. Hanno scoperto che la mano dell’allene favorita si trova più vicina al gruppo che cattura la luce e può assumere diverse conformazioni leggermente differenti, tutte compatibili con un efficiente trasferimento di energia. La mano sfavorita o si lega debolmente o sta più lontano, rendendo molto meno probabile la sua eccitazione. Esperimenti aggiuntivi con materiali di partenza puri di mano destra e sinistra hanno confermato questo bias: l’enzima converte rapidamente la mano favorita in un intermedio reattivo, che poi si rilassa in soluzione tornando a una miscela in cui l’altra mano si accumula. In sostanza, la proteina si comporta come un tornello molecolare, eccitando e consumando ripetutamente una mano mentre permette all’altra di accumularsi. 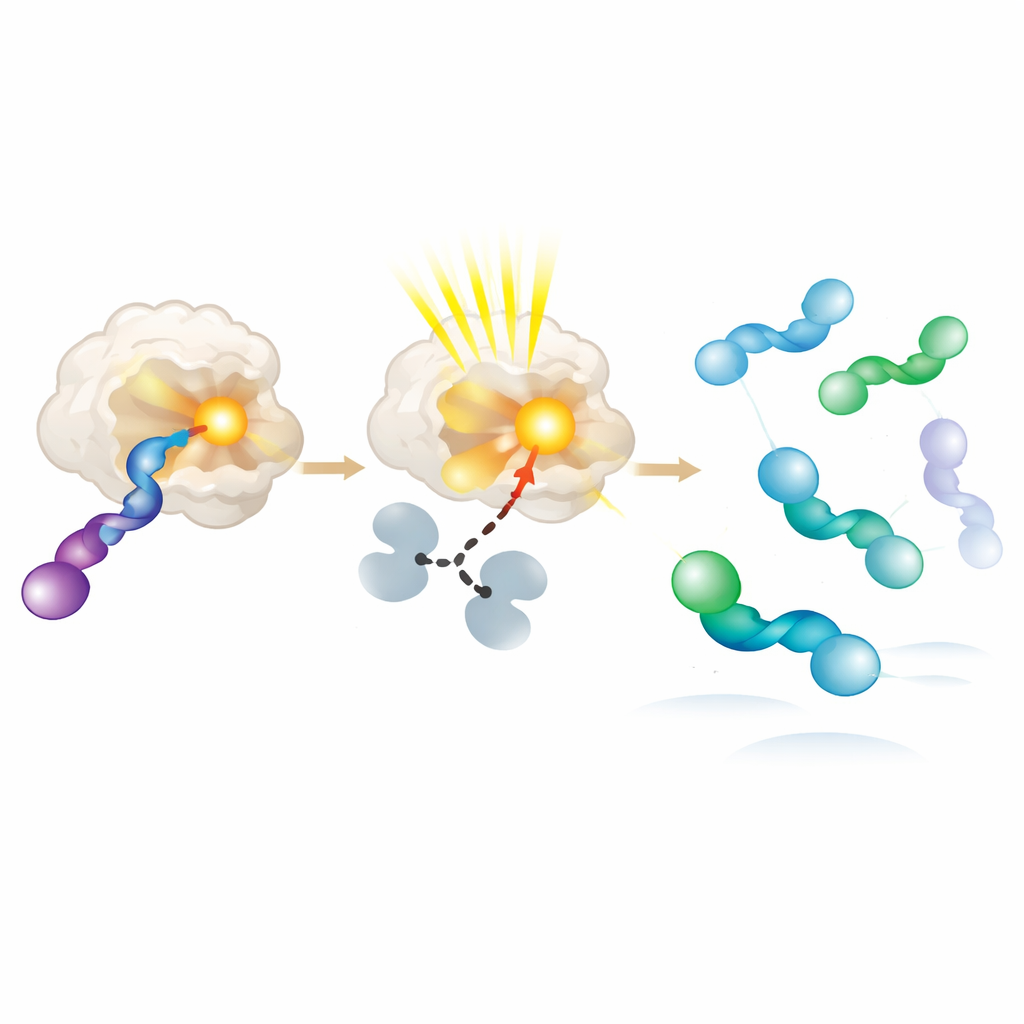
Cosa significa per la chimica del futuro
Per i non‑specialisti, il messaggio principale è che il team ha creato una macchina proteica programmabile che usa la luce per selezionare e valorizzare molecole attorcigliate con una versatilità senza precedenti. Invece di progettare un nuovo catalizzatore chimico per ogni bersaglio, i ricercatori possono ora partire da questa piattaforma di fotoenzimi e sintonizzare la sua tasca interna per accettare molti alleni diversi. Questo approccio riduce il divario tra il controllo raffinato della natura e la necessità dell’industria chimica di metodi ampi e robusti. A lungo termine, tali enzimi alimentati dalla luce potrebbero aiutare i chimici a preparare blocchi di costruzione complessi e a mano singola per farmaci e materiali in modo più efficiente, con meno passaggi e meno sprechi.
Citazione: Fu, K., Li, M., Deng, Z. et al. Unlocking enzymatic deracemization of structurally diverse allenes by designed photoenzymes. Nat Commun 17, 2082 (2026). https://doi.org/10.1038/s41467-026-68964-6
Parole chiave: fotoenzima, deracemizzazione, allene chirale, biocatalisi, trasferimento di energia tripletto