Clear Sky Science · it
L’infezione da HCMV altera le funzioni di barriera e promuove la transizione epiteliale–mesenchimale in un modello di organoide di colangiocita
Perché questa storia del virus nel fegato è importante
Il citomegalovirus umano è un virus molto comune che la maggior parte di noi porta senza saperlo. Tuttavia nei neonati e nelle persone con sistemi immunitari deboli può essere associato a gravi problemi del fegato e delle vie biliari, inclusa una rara ma devastante malattia infantile chiamata atresia biliare. Questo studio utilizza minuscoli dotti biliari coltivati in laboratorio per mostrare come il virus possa danneggiare direttamente questi sottili tubi e innescare cambiamenti fibrotici che possono contribuire a spiegare i legami, da tempo dibattuti, tra infezione e malattia epatica cronica.
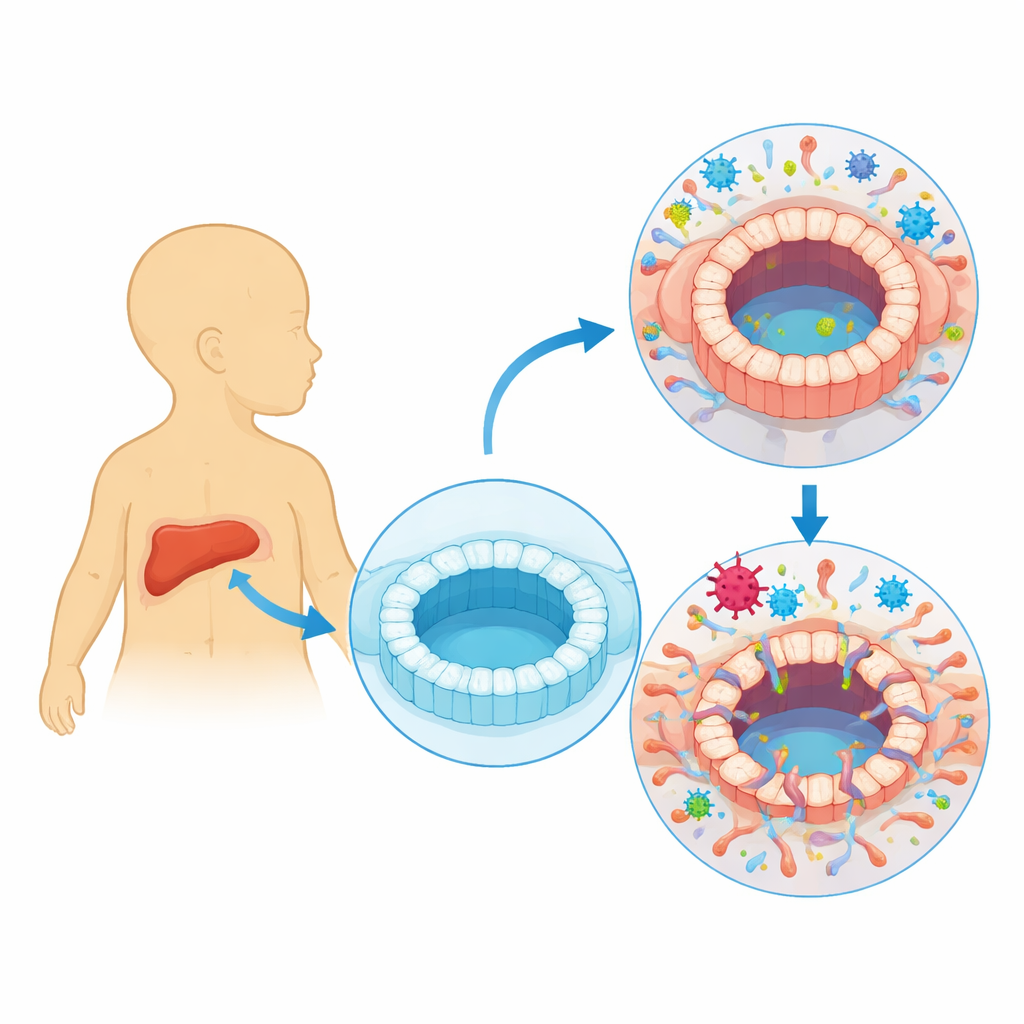
Uno sguardo più ravvicinato a un virus comune ma silenzioso
Il citomegalovirus umano (HCMV) di solito rimane silente nel nostro corpo, alternando fasi attive, in cui produce nuove particelle virali, a fasi latenti, in cui si nasconde all’interno di certi globuli del sangue. I medici hanno a lungo osservato che persone con infezione attiva da HCMV possono sviluppare lesioni delle vie biliari e colestasi, condizioni in cui la bile non scorre correttamente. Molti neonati con atresia biliare, in cui i dotti biliari si bloccano e si cicatrizzano subito dopo la nascita, mostrano anche segni di una recente infezione da HCMV. Rimane tuttavia incerto se il virus infetti direttamente le cellule che rivestono i dotti biliari o sia semplicemente presente come contingente durante la malattia.
Costruire minuscoli dotti biliari in coltura
Per rispondere a questa domanda, i ricercatori hanno creato organoidi tridimensionali che imitano i dotti biliari umani. Sono partiti da cellule staminali pluripotenti indotte, riprogrammate da sangue umano, e le hanno indirizzate a differenziarsi in cellule simili ai colangiociti — il tipo che riveste i dotti biliari. Queste cellule si sono auto-organizzate in sfere cave con una cavità centrale e connessioni cellula–cellula strette, ricordando un dotto biliare in miniatura. Il gruppo ha quindi esposto gli organoidi a un ceppo di HCMV marcato con un indicatore fluorescente che si accende quando il virus si replica attivamente. Questo ha permesso di tracciare le cellule infette e misurare come gli organoidi cambiassero nel tempo.
Come l’infezione deforma la struttura e indebolisce la barriera
Una volta infettati, gli organoidi hanno smesso di crescere normalmente e sono diventati irregolari, con pareti ispessite e deformate. Alcune cellule brillavano intensamente, indicando attività virale completa e produzione di nuove particelle; altre contenevano materiale genetico virale a livelli più bassi, suggerendo uno stato più dormiente, simile alla latenza. Test funzionali hanno rivelato che gli organoidi infettati perdevano capacità chiave del dotto biliare. Non si gonfiavano più correttamente in risposta a uno stimolo che dipende dai canali di trasporto ionico e mostravano una maggiore permeabilità in un saggio di resistenza elettrica che misura la tenuta della barriera. Proteine che normalmente sigillano gli spazi tra le cellule, come i componenti delle giunzioni strette, risultavano ridotte e il trasporto di un colorante di prova dentro e fuori la cavità interna era anomalo. Complessivamente, questi cambiamenti mostrano che l’HCMV può compromettere direttamente la parete del dotto biliare, rendendola più permeabile e disfunzionale.
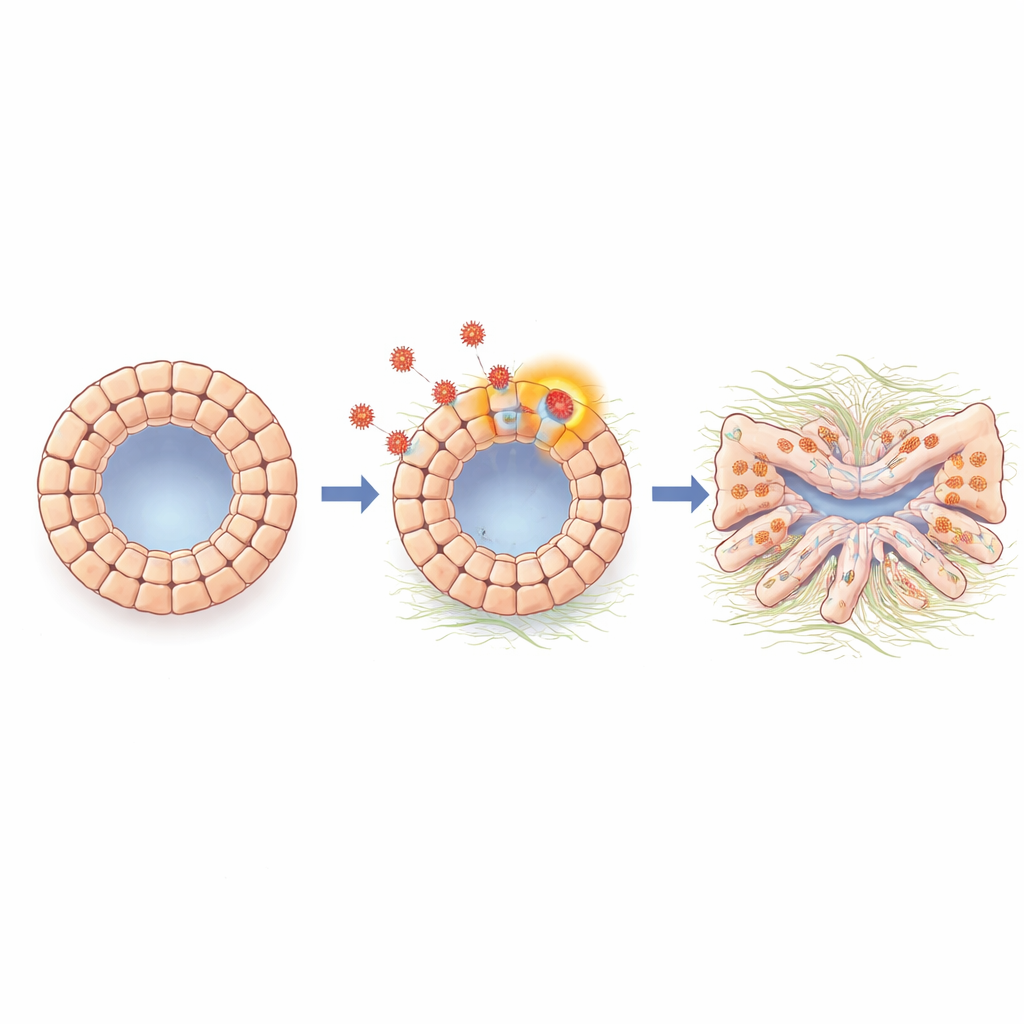
Le cellule cambiano identità verso uno stato fibrotico
Approfondendo l’analisi, gli scienziati hanno esaminato l’attività genica negli organoidi sia in massa sia a risoluzione di singola cellula. Hanno rilevato una forte attivazione di un programma simile alla transizione epiteliale–mesenchimale, un processo in cui le cellule superficiali strettamente connesse allentano i loro legami, assumono caratteristiche più mobili e fibrose e iniziano a produrre molecole associate alla cicatrizzazione tissutale. Gli organoidi infettati mostravano livelli aumentati di N-caderina e di altri marcatori legati a questo cambiamento, oltre all’aumento di geni coinvolti nella fibrosi e nella produzione di matrice. Una molecola di segnalazione chiamata TGF-beta, nota per promuovere la cicatrizzazione in molti organi, risultava potenziata durante l’infezione. Quando il team ha bloccato la segnalazione di TGF-beta con un inibitore a piccola molecola o con un anticorpo, gli organoidi hanno recuperato una forma più normale e molti dei geni legati alla fibrosi e alla transizione sono tornati verso i livelli di base, indicando che TGF-beta è un mediatore chiave che collega la presenza virale ai danni cellulari.
Dai tubi coltivati in laboratorio ai bambini malati
Per verificare se queste osservazioni di laboratorio si riferiscono alla malattia reale, i ricercatori hanno esaminato tessuto epatico di bambini con atresia biliare e di altri pazienti pediatrici con malattie del fegato. Usando sonde sensibili, hanno rilevato DNA di HCMV nei colangiociti — le cellule dei dotti biliari — in circa due terzi dei campioni di atresia biliare, ma con una frequenza molto inferiore nei fegati non affetti da atresia biliare. Nelle stesse aree in cui si trovava il DNA virale, le cellule biliari mostravano livelli più alti di TGF-beta e N-caderina, corrispondenti al modello di transizione e cicatrizzazione osservato negli organoidi. Ciò suggerisce che, in almeno una sottopopolazione di bambini, l’HCMV infetti direttamente i colangiociti e li spinga verso uno stato fibrotico attivando vie dipendenti da TGF-beta.
Cosa significa per la comprensione e il trattamento delle malattie dei dotti biliari
In termini semplici, questo lavoro mostra che un virus comune può invadere le cellule che rivestono i dotti biliari, allentare le loro connessioni strette e spingerle verso un’identità meno specializzata e più fibrotica attraverso un segnale mediato da TGF-beta. Questi cambiamenti indeboliscono le funzioni di barriera e di trasporto dei dotti e possono contribuire all’ostruzione e alla fibrosi osservate in malattie come l’atresia biliare. Pur non essendo l’agente causale di tutti i casi di malattia dei dotti biliari, lo studio rafforza l’idea che, nei neonati vulnerabili, l’infezione virale possa essere un fattore importante — e che mirare alle vie correlate a TGF-beta potrebbe un giorno aiutare a proteggere o ripristinare dotti biliari fragili.
Citazione: Ye, Z., Hu, X., Rahaman, S.M. et al. HCMV infection disrupts barrier functions and promotes epithelial–mesenchymal transition in a cholangiocyte organoid model. Nat Commun 17, 2273 (2026). https://doi.org/10.1038/s41467-026-68962-8
Parole chiave: citomegalovirus, atresia biliare, organoidi delle vie biliari, transizione epiteliale mesenchimale, segnalazione TGF-beta