Clear Sky Science · it
Comprendere la promozione da metalli alcalini nella catalisi di idrogenazione tramite la Strong Metal–Base Interaction
Perché modificare i catalizzatori conta nella vita di tutti i giorni
Trasformare molecole semplici come anidride carbonica e idrogeno in combustibili e prodotti chimici utili è centrale per un’energia più pulita e un’industria più sostenibile. Molti dei catalizzatori metallici che guidano queste reazioni contengono già piccole quantità di metalli alcalini come sodio o potassio come “promotori”, ma il loro ruolo reale è sorprendentemente poco chiaro. Questo studio svela un principio unificante sul funzionamento di questi additivi, offrendo un modo per progettare catalizzatori più intelligenti in grado di indirizzare le reazioni verso prodotti desiderati e lontano dagli sprechi.
Uno sguardo più attento ai metalli potenziati
I catalizzatori a base di metalli di transizione come rodio e nichel sono supportati su solidi e aiutano a rompere e riformare legami chimici. Per decenni, l’industria ha aggiunto metalli alcalini per rendere questi catalizzatori più attivi, più selettivi o più duraturi. Le spiegazioni tradizionali si sono concentrate su effetti geometrici semplici (modifiche di forma e dimensione delle particelle) o su un diretto trasferimento di elettroni dal metallo alcalino al metallo attivo. Tuttavia, in condizioni operative reali questi promotori esistono principalmente come ossidi, non come atomi metallici nudi, il che rende il trasferimento di carica diretto un quadro incompleto.
Scoprire una solida collaborazione sulla superficie
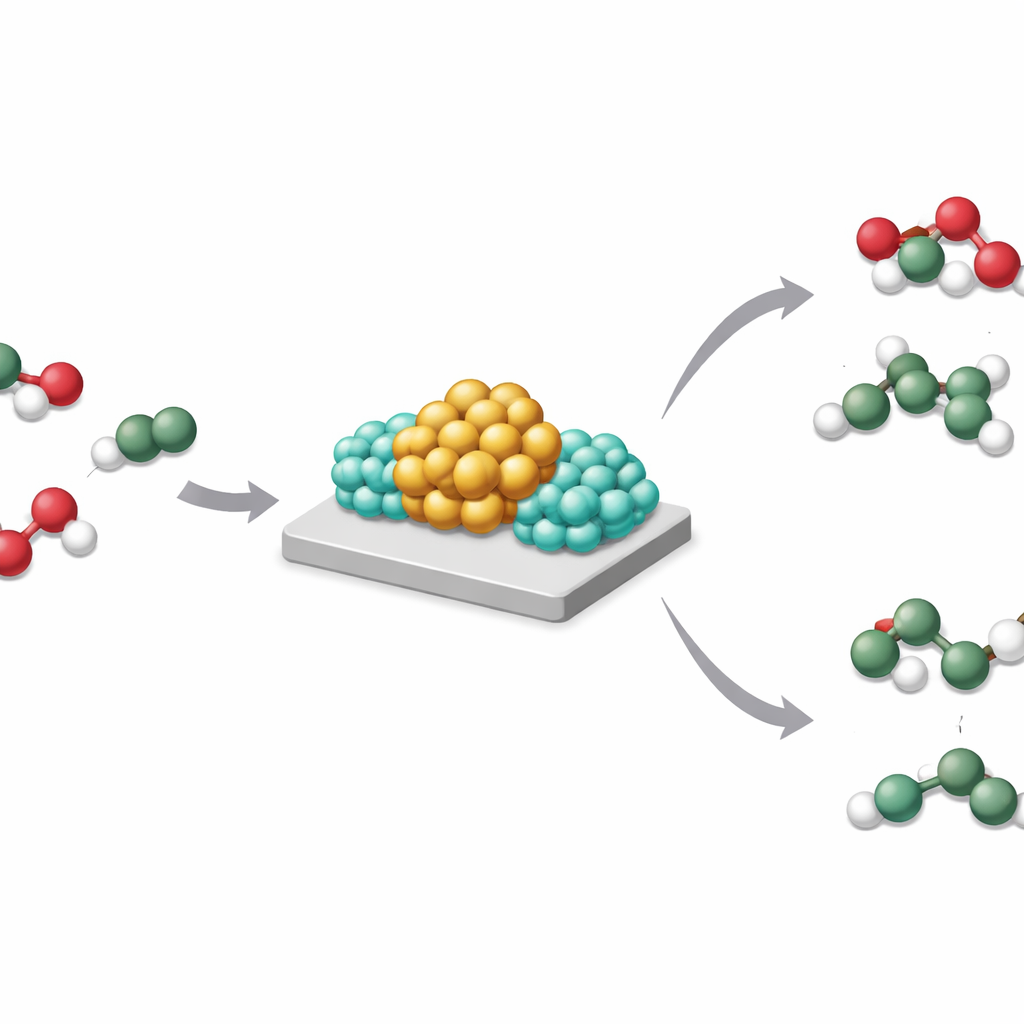
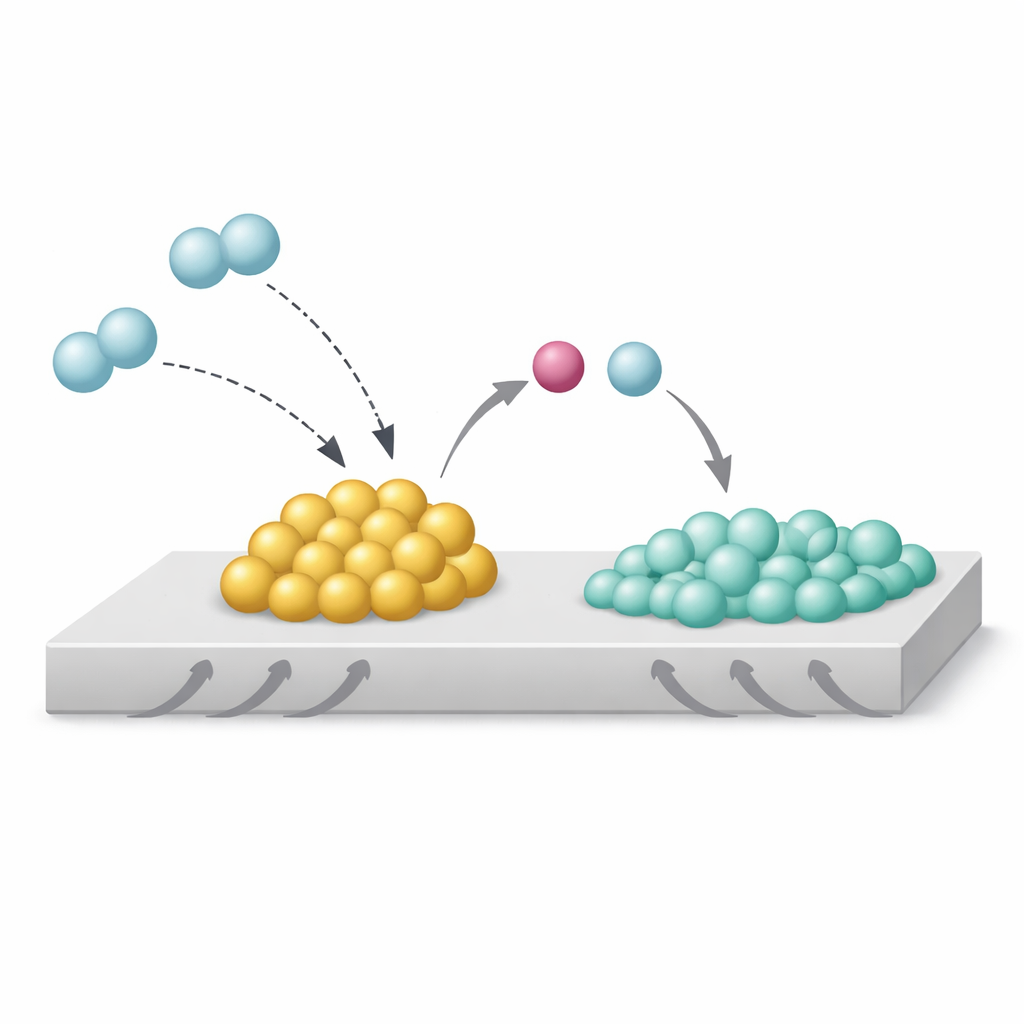
Gli autori hanno studiato un sistema modello: nanoparticelle di rodio su biossido di titanio, con e senza l’aggiunta di sodio. Utilizzando microscopie elettroniche avanzate, spettroscopia a raggi X e simulazioni al computer, hanno scoperto che il sodio si trova come ossido, Na₂O, proprio al margine di contatto tra le particelle di rodio e il supporto. In presenza di idrogeno, questa disposizione crea ciò che chiamano Strong Metal–Base Interaction, o SMBI. In questi punti di contatto speciali, le molecole di idrogeno si scindono in modo asimmetrico: il più basico Na₂O cattura la parte simile a un protone, mentre il rodio trattiene il partner ricco di elettroni. Questa scissione eterolitica rende la superficie del rodio insolitamente ricca di elettroni e impedisce che l’idrogeno si disperda, o “spillover”, sul supporto di biossido di titanio.
Come questo effetto nascosto dirige le reazioni
Questa sottile riorganizzazione di dove risiedono idrogeno ed elettroni ha grandi conseguenze. Nella idrogenazione della CO2, il rodio puro su biossido di titanio favorisce l’iddrogenazione profonda fino al metano. Quando si aggiunge sodio, lo stesso catalizzatore produce soprattutto monossido di carbonio, un prezioso elemento di partenza, e genera molto meno metano. Un comportamento simile si osserva con litio o potassio, o quando il rodio viene sostituito dal nichel. Gli autori mostrano che quando l’idrogeno può libero effettuare spillover sul supporto, domina l’iddrogenazione profonda; quando la SMBI mantiene l’idrogeno concentrato al confine metallo‑base e lontano dal supporto, prevalgono prodotti più moderati.
Doppio legame diverso, esito diverso
Il gruppo ha quindi investigato come la SMBI influenza comuni reazioni di idrogenazione organica che coinvolgono doppi legami carbonio–carbonio, carbonio–ossigeno e azoto–ossigeno. Per un doppio legame carbonio–carbonio nella vinilacetato, la promozione con sodio rende il catalizzatore più veloce, probabilmente perché il rodio ricco di elettroni aiuta a indebolire quel legame mentre l’idrogeno più debolmente legato si addiziona in modo efficiente. Al contrario, per molecole come acetofenone e nitrobenzene, i cui gruppi reattivi preferiscono adsorbirsi sul supporto ossidico, la stessa aggiunta di sodio rallenta la reazione. Qui, il ridotto spillover di idrogeno significa che il supporto non riceve più abbastanza idrogeno per guidare quelle trasformazioni, rivelando che non tutti i doppi legami beneficiano allo stesso modo dall’effetto promozionale.
Progettare catalizzatori con controllo intenzionale
Combinando esperimenti e teoria, gli autori sostengono che la SMBI fornisce un modo unificato per capire come i promotori di metalli alcalini rimodellano le superfici catalitiche. Piuttosto che agire come semplici donatori di elettroni, gli ossidi alcalini funzionano come forti trappole per protoni, costringendo l’idrogeno a scindersi in modo polarizzato e confinando l’idrogeno reattivo vicino all’interfaccia metallo‑base. Questa intuizione spiega tendenze enigmatiche attraverso molte reazioni di idrogenazione e metalli, e indica una regola pratica di progettazione: regolando quanto e dove vengono posti gli ossidi alcalini attorno alle particelle metalliche, i chimici possono indirizzare deliberatamente le reazioni verso prodotti specifici ottimizzando attività e stabilità per processi chimici più puliti.
Citazione: Jung, M., Dickieson, M.P., Chen, P. et al. Understanding alkali metal promotion in hydrogenation catalysis through Strong Metal–Base Interaction. Nat Commun 17, 2465 (2026). https://doi.org/10.1038/s41467-026-68952-w
Parole chiave: catalisi di idrogenazione, promotori metalli alcalini, conversione CO2, catalizzatori eterogenei, interfacce metallo‑ossido