Clear Sky Science · it
RiboBright rivela differenze specifiche di tipo cellulare nell'organizzazione e nel movimento dei ribosomi
Vedere illuminarsi le fabbriche di proteine della cellula
Ogni secondo, ciascuna delle nostre cellule produce migliaia di nuove proteine usando piccole macchine chiamate ribosomi. Fino a oggi, osservare dove si trovano queste macchine e come si muovono all'interno di cellule viventi è risultato sorprendentemente difficile. Questo studio presenta RiboBright, una piccola molecola fluorescente che si lega ai ribosomi e li illumina, permettendo agli scienziati di tracciare queste fabbriche proteiche cellula per cellula. Il lavoro mostra che i ribosomi sono organizzati e impiegati in modo molto diverso a seconda del tipo cellulare, soprattutto mentre le cellule staminali scelgono il loro destino futuro.
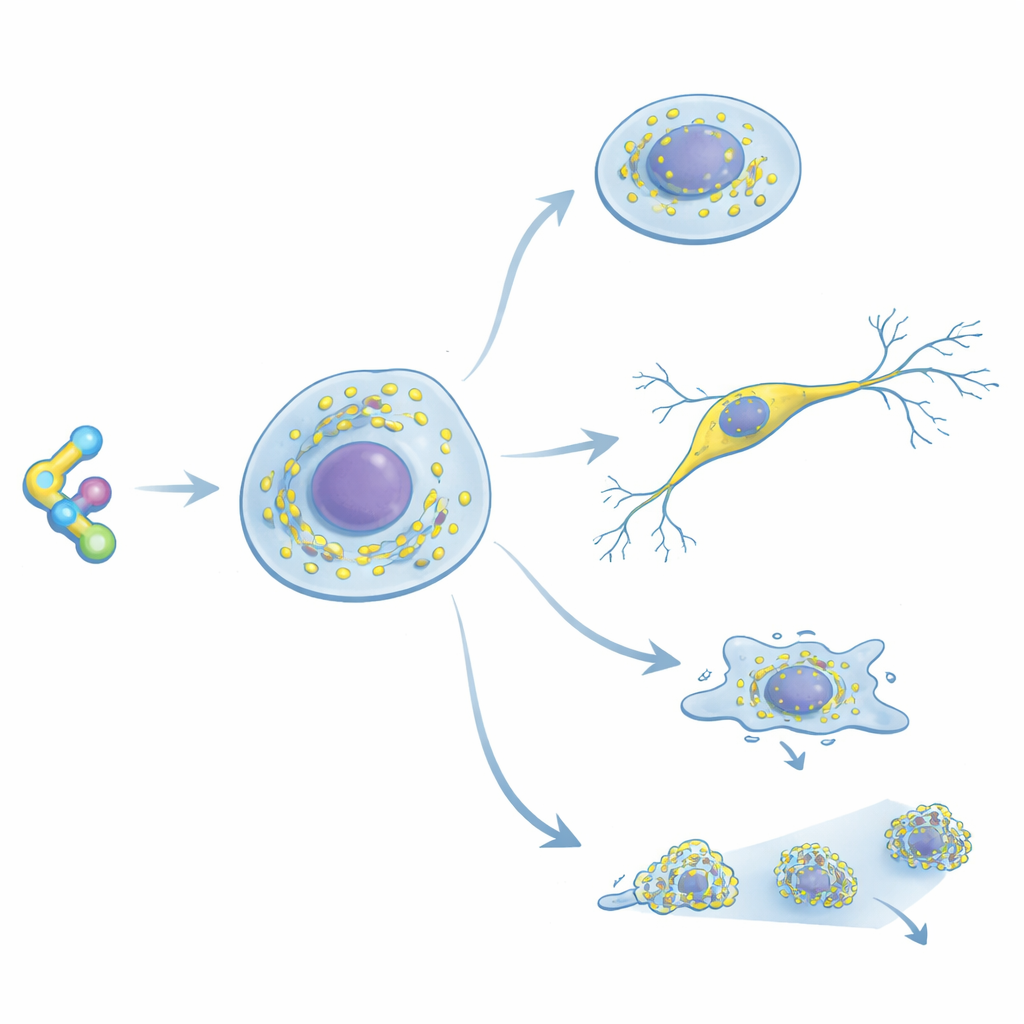
Un nuovo modo per evidenziare i ribosomi
I ricercatori hanno sviluppato RiboBright modificando la cicloeossiprodossima, un farmaco classico noto per legarsi in modo forte e selettivo ai ribosomi di animali e umani. Hanno attaccato un particolare colorante a «rotore molecolare» in una posizione del farmaco che non indebolisce la sua tenuta sul ribosoma. Questo colorante emette poca luce quando ruota liberamente in soluzione, ma diventa brillante quando il suo movimento è ristretto — ad esempio quando la sonda si infila nel ribosoma. Test in provetta hanno mostrato che le molecole modificate bloccano ancora la produzione proteica a dosi quasi sovrapponibili a quelle del farmaco originale, confermando un buon legame. In cellule viventi, una versione in particolare ha prodotto punti nitidi e luminosi, indicando un equilibrio ottimale tra legame saldo al ribosoma e forte emissione luminosa; questa sonda ottimizzata è stata denominata RiboBright.
Dimostrare che la sonda mira a ribosomi reali
Per essere certi che RiboBright marcasse davvero i ribosomi, il team ha combinato diversi approcci complementari. Quando le cellule sono state pre-trattate con la stessa cicloeossiprodossima o con un altro composto non correlato che blocca i ribosomi, il segnale di RiboBright è quasi scomparso, suggerendo che tutti e tre competono per lo stesso sito di legame. Indagini chimiche sull'RNA ribosomiale hanno inoltre mostrato che RiboBright protegge lo stesso nucleotide che la cicloeossiprodossima mette al riparo, coerente con un sito di ancoraggio identico. La microscopia ad alta risoluzione ha rivelato che il segnale di RiboBright si sovrappone fortemente con marcatori della subunità ribosomiale grande e con strutture come il reticolo endoplasmatico e i mitocondri, dove molti ribosomi risiedono. Allo stesso tempo, alcuni punti luminosi fluttuano liberi nel citoplasma, probabilmente rappresentando ribosomi mobili non attaccati alle membrane.
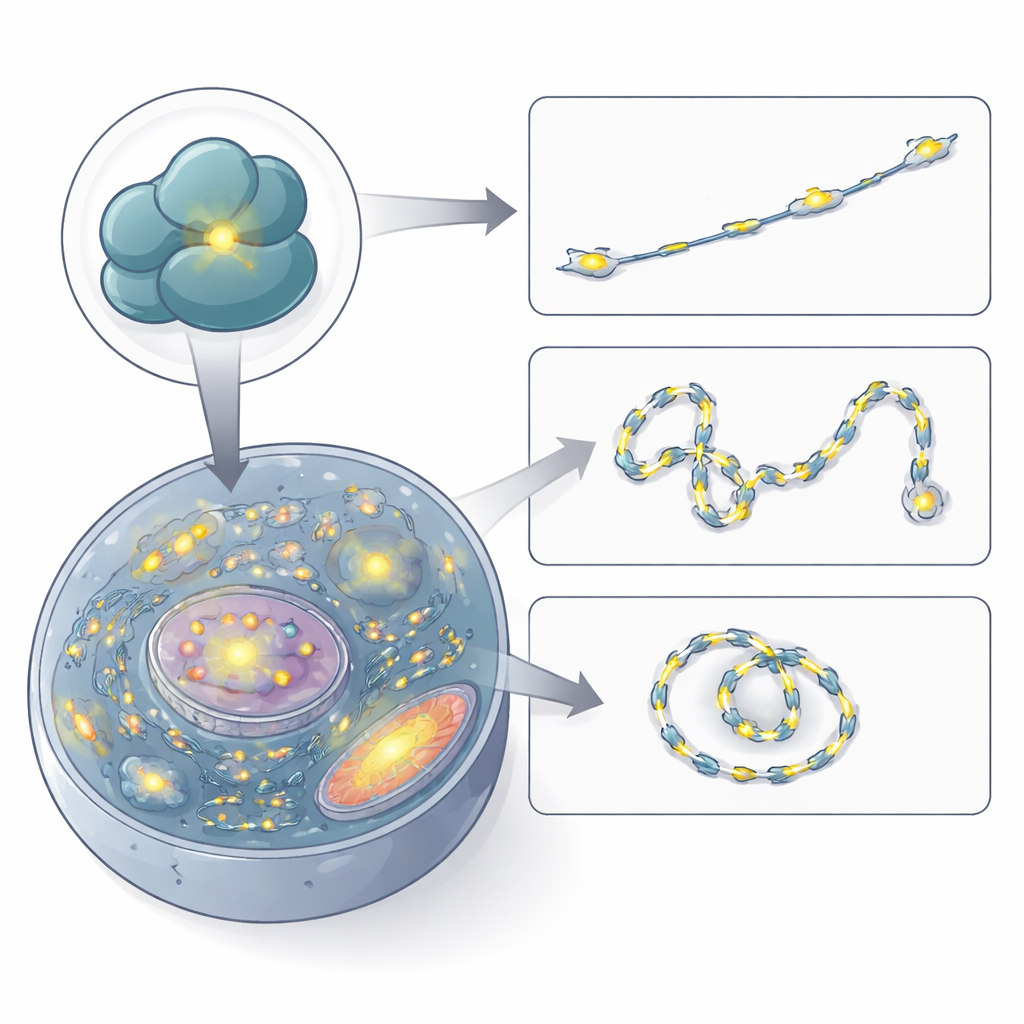
Osservare i ribosomi muoversi nelle cellule viventi
Con la certezza della sua specificità, gli autori hanno usato RiboBright per filmare i ribosomi in azione. Registrando immagini ogni poche centinaia di millisecondi, hanno ricostruito i percorsi di singoli puntini fluorescenti attraverso la cellula. Molti punti si muovevano appena o restavano confinati in piccole regioni, suggerendo ribosomi che traducono in loco su messaggeri fissati o sul reticolo endoplasmatico. Altri vagavano in modo casuale e diffusivo, e una frazione più piccola mostrava un chiaro moto diretto, suggerendo trasporto attivo lungo rotaie cellulari. Le velocità misurate corrispondono a stime precedenti per gli mRNA e per ammassi di ribosomi, confermando che RiboBright può catturare dinamiche realistiche dei ribosomi in tempo reale.
Tipi cellulari diversi, strategie ribosomiali diverse
RiboBright ha inoltre rivelato quanto fortemente il contenuto e l'organizzazione dei ribosomi dipendano dall'identità cellulare. In dieci linee cellulari umane e murine, incluse cellule staminali, cellule tumorali e cellule non cancerose, il modello e la luminosità dei punti ribosomiali variavano in modo marcato. Alcune cellule contenevano grandi ammassi luminosi che possono corrispondere a regioni di intensa produzione proteica, mentre altre mostravano per lo più puntini piccoli e dispersi. Sorprendentemente, il mero numero di ribosomi in una cellula non prevedeva in modo affidabile quanto proteina produceva: nella maggior parte dei tipi cellulari, la produzione proteica e il contenuto ribosomiale mostravano poca correlazione. Le cellule staminali embrionali si distinguevano per avere una bassa produttività per ribosoma e una traduzione relativamente uniforme tra le singole cellule, suggerendo che mantengono grandi riserve di ribosomi poco utilizzati pur mantenendo bassa la variabilità nella produzione proteica.
I ribosomi durante le prime decisioni sul destino cellulare
Il gruppo ha quindi seguito cellule staminali embrionali murine mentre iniziavano a differenziarsi in due lignaggi precoci: un ramo simile all'ectoderma e un ramo simile all'endoderma extraembrionale (XEN). Usando RiboBright assieme a marcatori di superficie cellulare, hanno scoperto che entrambi i lignaggi emergenti acquisivano leggermente più contenuto ribosomiale totale rispetto alle cellule indifferenziate, ma disponevano questi ribosomi in modo diverso. Le cellule simili a XEN, che sviluppano lunghe protrusioni, mostravano un movimento dei ribosomi più lento e più confinato, coerente con sintesi proteica localizzata in regioni specializzate. Al contrario, le cellule simili all'ectoderma mostravano ribosomi più mobili e, dopo circa due giorni, sviluppavano sorprendenti «hub translazionali» dove sia il segnale ribosomiale sia la nuova sintesi proteica raggiungevano il picco. Nelle prime 72 ore di differenziazione, la produzione proteica complessiva e i livelli ribosomiali sono calati moderatamente, ma i ribosomi rimanenti sono diventati leggermente più efficienti, soprattutto nelle cellule in differenziamento.
Cosa significa per la comprensione delle cellule
Nel complesso, questi risultati dipingono un quadro più ricco dei ribosomi come macchine dinamiche e dipendenti dal contesto, piuttosto che come semplici operai uniformi. RiboBright fornisce ai ricercatori uno strumento pratico per visualizzare e contare i ribosomi in molti tipi cellulari, sia in campioni fissati sia vivi, e per mettere in relazione posizione e movimento dei ribosomi con la quantità di proteina che una cellula effettivamente produce. Per i non specialisti, il messaggio chiave è che le cellule modulano non solo quanti stabilimenti di produzione costruiscono, ma anche dove li collocano e quanto attivamente li fanno funzionare, in modi che dipendono dal tipo cellulare e dallo stato di sviluppo. Questa nuova sonda fluorescente rende visibili quelle logistiche nascoste, aprendo la strada allo studio di come il comportamento dei ribosomi contribuisca allo sviluppo, alle malattie e alle risposte alle terapie.
Citazione: Poulladofonou, G., Grandi, C., Hu, X. et al. RiboBright reveals cell-type-specific differences in ribosome organization and movement. Nat Commun 17, 2734 (2026). https://doi.org/10.1038/s41467-026-68947-7
Parole chiave: ribosomi, sonde fluorescenti, imaging a singola cellula, differenziazione delle cellule staminali, sintesi proteica