Clear Sky Science · it
FCHo2, non talin, abilita l'attivazione inside-out dell'integrina ɑvβ5 nelle adesioni curve
Come le cellule percepiscono la forma dell'ambiente
I nostri corpi sono composti da cellule che continuamente afferrano l'ambiente circostante, tirando e spingendo per muoversi, dividersi o restare ferme. Questo articolo mostra che le cellule non percepiscono solo quanto sia rigido il loro ambiente, ma ne leggono anche la forma. Identificando un sistema adesivo speciale che si attiva solo dove la membrana cellulare è fortemente curva, gli autori dimostrano che le cellule usano "prese" interne diverse per superfici piatte rispetto a contesti fibrillari, con implicazioni importanti per la formazione dei tessuti e la diffusione dei tumori.
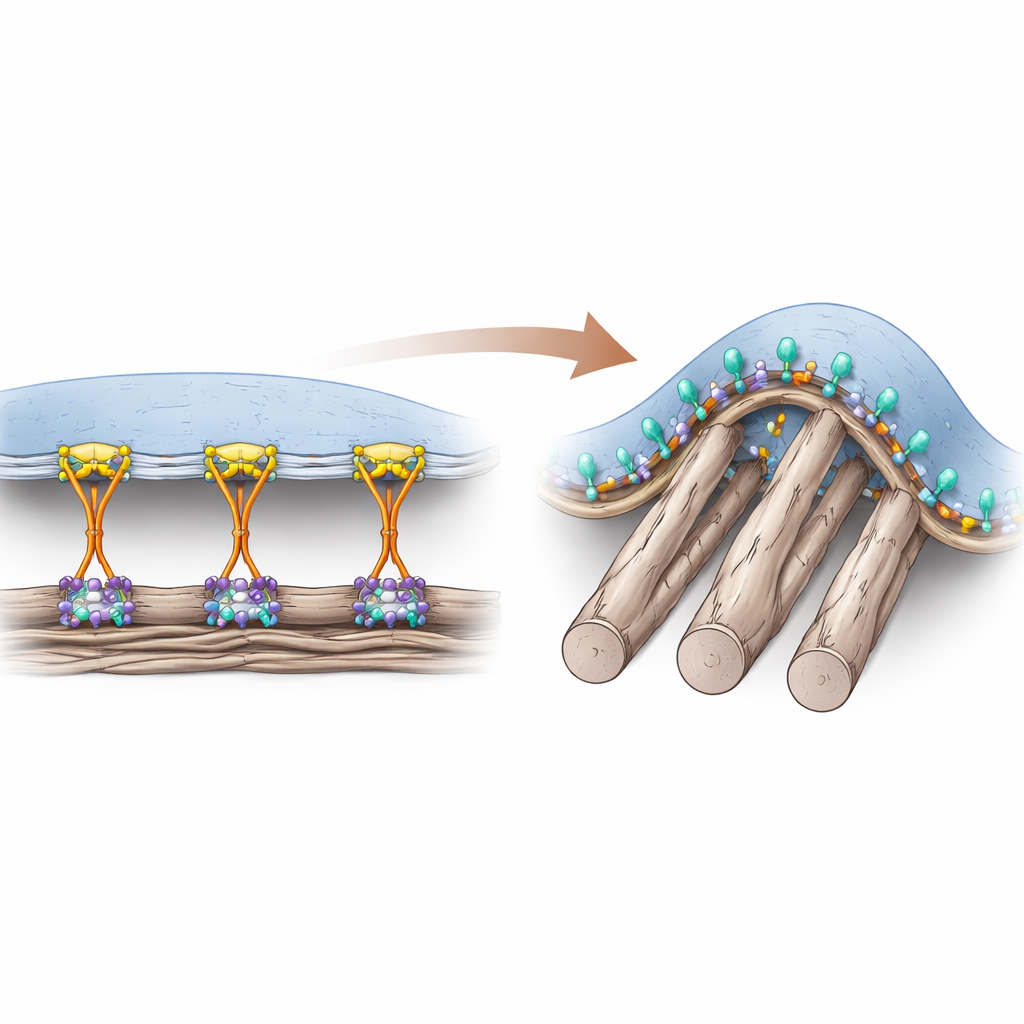
Due modi in cui le cellule si aggrappano
Le cellule si attaccano al materiale ricco di proteine che le circonda usando recettori di superficie chiamati integrine. Per anni i ricercatori hanno pensato che una proteina ausiliaria chiamata talin fosse assolutamente essenziale per attivare le integrine "dall'interno" della cellula, permettendo un legame forte nelle classiche sedi di ancoraggio note come adesioni focali. Queste adesioni si formano principalmente su superfici piatte e rigide e trasmettono grandi forze di trazione attraverso il citoscheletro. Tuttavia, nei tessuti viventi molte delle fibre circostanti sono morbide e cilindriche, creando punti di contatto curvi che non supportano facilmente queste strutture ad alto carico. Gli autori avevano precedentemente individuato un tipo diverso di struttura adesiva, chiamata adesione curva, che appare proprio dove la membrana si piega attorno a fibre sottili e che dipende da una specifica integrina, αvβ5.
Le prese curve usano un aiuto diverso
Nello studio nuovo, il gruppo mostra che talin, pur essendo presente, non è il principale attivatore dell'integrina αvβ5 nelle adesioni curve. Al suo posto, una proteina sensibile alla curvatura chiamata FCHo2 assume questo ruolo. Usando barre e pilastri nanoscopici ingegnerizzati per piegare le membrane cellulari in modo controllato, hanno osservato che αvβ5 si raggruppa fortemente nelle regioni curve, ma solo quando FCHo2 può legarsi a una sequenza molto corta—un motivo HDRRE—situata appena all'interno della cellula sulla coda β5. Quando questo motivo è alterato, l'integrina funziona ancora nelle adesioni focali ma non può più formare adesioni curve. L'abbattimento di FCHo2 lascia in gran parte intatte le adesioni focali classiche ma elimina le adesioni curve, mentre la rimozione di talin indebolisce gravemente le adesioni focali lasciando le adesioni curve per lo più non influenzate.
Un singolo cambiamento di amminoacido come selettore di forma
Un enigma era perché un'integrina strettamente correlata, αvβ3, non possa formare adesioni curve nonostante la sua coda interna somigli molto a quella di β5. Scambiando domini tra le due integrine e introducendo mutazioni puntiformi, gli autori hanno identificato una posizione cruciale vicino al sito di legame di talin: la maggior parte delle integrine β ha un triptofano (W), ma β5 ha unicamente una tirosina (Y766). Quando la tirosina di β5 è stata sostituita con triptofano, l'integrina ha perso la capacità di partecipare alle adesioni curve e si è comportata più come β3, favorendo solo adesioni focali. Il cambiamento inverso—inserire tirosina in un chimerico simile a β3—ha ripristinato la sensibilità alla curvatura. Ulteriori esperimenti con varianti che imitano gli stati fosforilati o non fosforilati di questa tirosina suggeriscono che la sua modifica chimica può indirizzare l'integrina verso adesioni focali piatte ad alta forza o verso adesioni curve a bassa forza.
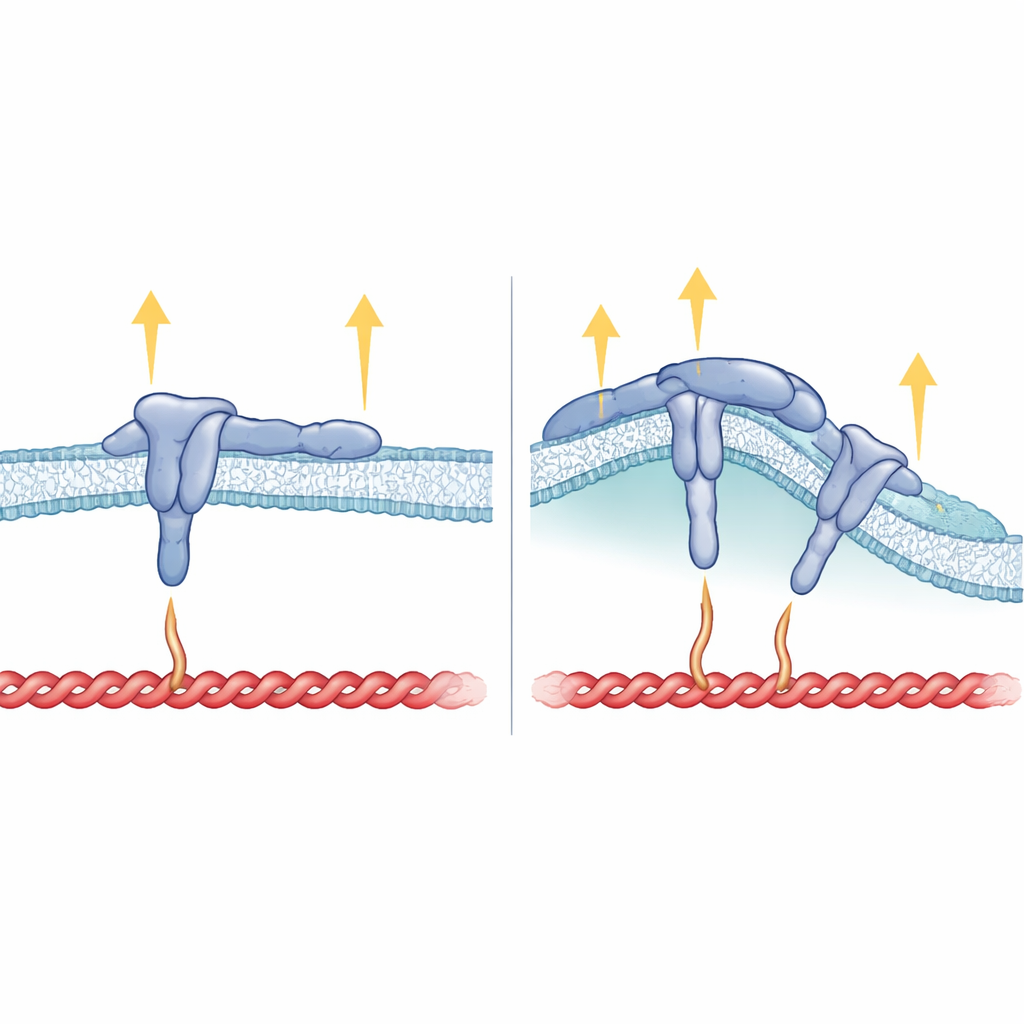
Come si incastrano forma della membrana, struttura dell'integrina e forza
Oltre alla coda interna, anche il tratto di β5 che attraversa la membrana si è dimostrato critico. Quando i ricercatori hanno sostituito il segmento transmembrana di β5 con quello di β3, l'integrina risultante poteva ancora formare adesioni focali ma non preferiva più i siti curvi né si associava a FCHo2. Ciò suggerisce che il modo in cui l'integrina è inserita nella membrana aiuti a orientare il motivo HDRRE in modo che FCHo2 possa agganciarsi nelle regioni curve e stabilizzare αvβ5 legata al ligando e attiva. Nelle adesioni curve, talin sembra toccare solo una parte più distante della coda dell'integrina e non sopportare alte tensioni, il che spiega perché altri componenti sensibili alla forza come vinculina, tensina e kindlin sono in gran parte assenti. Al contrario, nelle adesioni focali, talin afferra sia siti vicini sia lontani sulla coda e sulla membrana, sostenendo forti forze di trazione ma impedendo a FCHo2 di accedere alla stessa regione.
Cosa significa per il comportamento cellulare
Per un osservatore non esperto, il messaggio di questo lavoro è che le cellule possiedono due «modalità di presa» separate per attaccarsi all'ambiente. Su aree piatte e rigide usano adesioni focali guidate da talin costruite per tirare con forza. Su strutture morbide, fibrillari e curve passano a adesioni curve guidate da FCHo2 che stabilizzano l'integrina αvβ5 con forze molto più basse. Una piccola variazione nella sequenza dell'integrina—e se quel sito è chimicamente modificato—aiuta a decidere quale modalità venga impiegata. Questo sistema duplice permette alle cellule di interpretare sia la rigidità sia la forma in ambienti tridimensionali, influenzando come migrano, organizzano i tessuti e potenzialmente come invadono durante la malattia.
Citazione: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
Parole chiave: integrine, adesione cellulare, curvatura della membrana, FCHo2, cito scheletro