Clear Sky Science · it
Sviluppi e sfide nella progressione degli hit nella drug discovery basata su frammenti
Trasformare minuscoli pezzi chimici nei medicinali del futuro
I medicinali moderni vengono spesso scoperti setacciando enormi collezioni di molecole, un processo lento, costoso e sempre meno efficiente. Questo articolo esplora un approccio più recente chiamato drug discovery basata su frammenti, che parte da pezzi chimici molto piccoli e li costruisce passo dopo passo in candidati farmaceutici promettenti. Per il lettore offre una finestra su come un progetto più intelligente, l’automazione e l’intelligenza artificiale potrebbero rendere più rapide da trovare e più accessibili le terapie di domani.
Perché partire da piccoli frammenti invece di screenare tutto
La scoperta di farmaci tradizionale spesso si basa sul testare milioni di molecole relativamente grandi per vedere quali si legano a una proteina coinvolta nella malattia. I metodi basati su frammenti seguono la via opposta: screenare una collezione molto più piccola di molecole minuscole, o “frammenti”, ognuna rappresentante una forma chimica semplice. Questi frammenti si legano solo debolmente, ma poiché sono così piccoli e diversi, esplorano le possibilità chimiche in modo molto più efficiente. La sfida è che i segnali deboli sono difficili da rilevare e interpretare, quindi i ricercatori hanno bisogno di esperimenti molto sensibili e di controlli incrociati attenti per essere certi che un frammento si leghi veramente e non sia semplicemente un artefatto dell’essay. Tecniche strutturali come la cristallografia a raggi X e la crio-microscopia elettronica possono rivelare esattamente come un frammento si dispone in una tasca proteica, mentre metodi in soluzione come la NMR, la calorimetria e la risonanza plasmonica di superficie misurano quanto forte e quanto velocemente si lega.
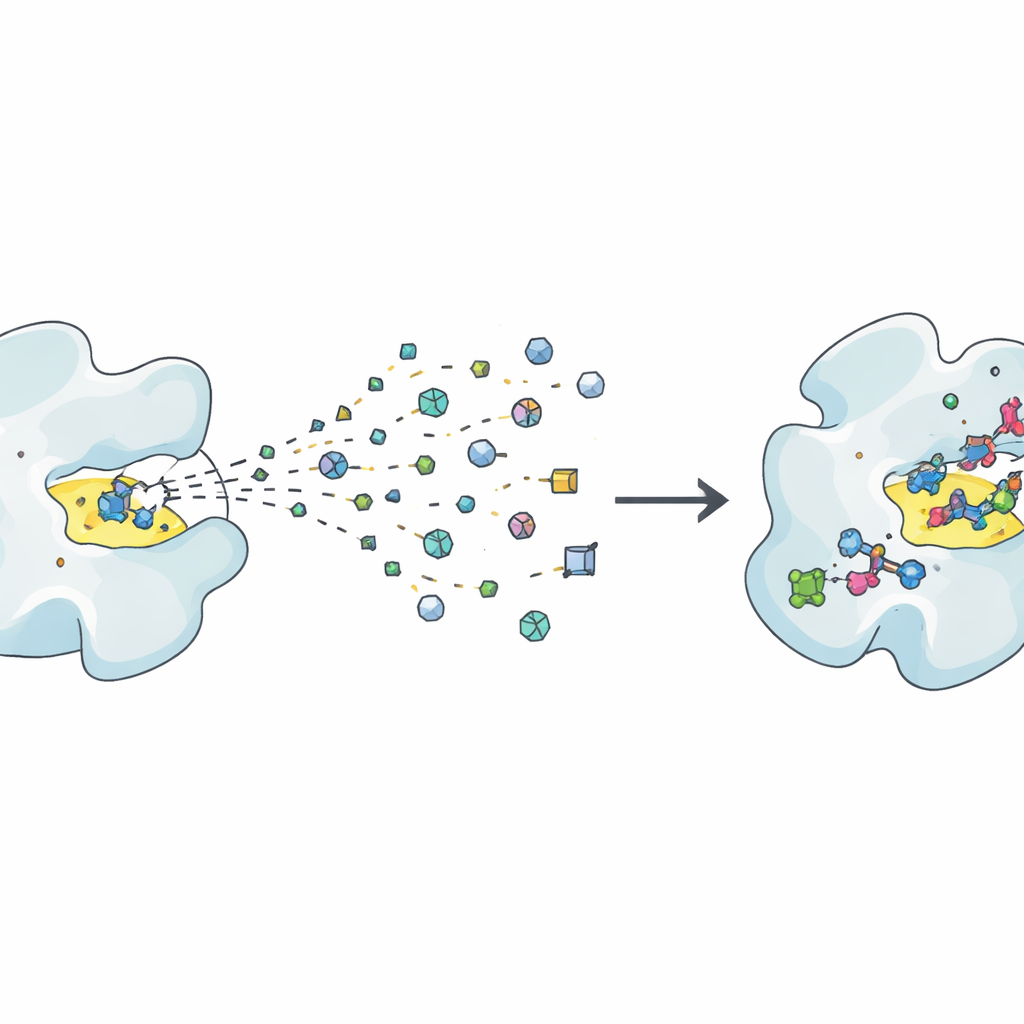
Dai primi hit ai lead promettenti
Una volta individuati frammenti utili, inizia il vero lavoro: trasformare questi deboli “hit” in composti “lead” forti e selettivi. L’articolo inquadra questo percorso come ripetuti cicli di “Design, Make, Test”. Nella fase di Design chimici e algoritmi propongono modi per far crescere, collegare o fondere i frammenti in modo che riempiano meglio la tasca della proteina, evitino reattività indesiderata e mantengano buone proprietà fisiche come la solubilità. Nella fase Make questi progetti vengono sintetizzati, sempre più spesso con l’aiuto di robot, chimica ad alto rendimento e software intelligenti per la pianificazione delle rotte. La fase Test misura poi se le nuove molecole si legano davvero meglio, agiscono sulla funzione biologica prevista ed evitano insidie comuni come i composti che interferiscono con molte prove e danno segnali fuorvianti. Poiché i frammenti partono da segnali deboli, spesso sono necessari diversi giri di questo ciclo prima che i composti diventino sufficientemente potenti da assomigliare a veri candidati farmaceutici.
Nuovi strumenti: automazione, IA e librerie smart
La review mette in evidenza come una nuova generazione di strumenti stia rimodellando ogni fase di questo ciclo. Le librerie di frammenti sono ora progettate non solo per essere diverse, ma anche “sinteticamente socievoli”, cioè facilmente espandibili in molte direzioni utilizzando reazioni robuste. Set specializzati di frammenti mirano a famiglie proteiche particolari, siti contenenti metalli o addirittura formano legami covalenti con specifici amminoacidi, aiutando ad affrontare target prima considerati “non druggable”. Sul fronte digitale, modelli di intelligenza artificiale e simulazioni basate sulla fisica aiutano a suggerire quali modifiche chimiche potrebbero migliorare il legame o ridurre la tossicità, e possono setacciare spazi virtuali ultra-grandi di miliardi di molecole possibili. Queste predizioni sono sempre più combinate con cicli di apprendimento attivo, in cui un piccolo numero di simulazioni o esperimenti costosi addestra modelli più veloci che possono guidare la successiva ondata di progetti.
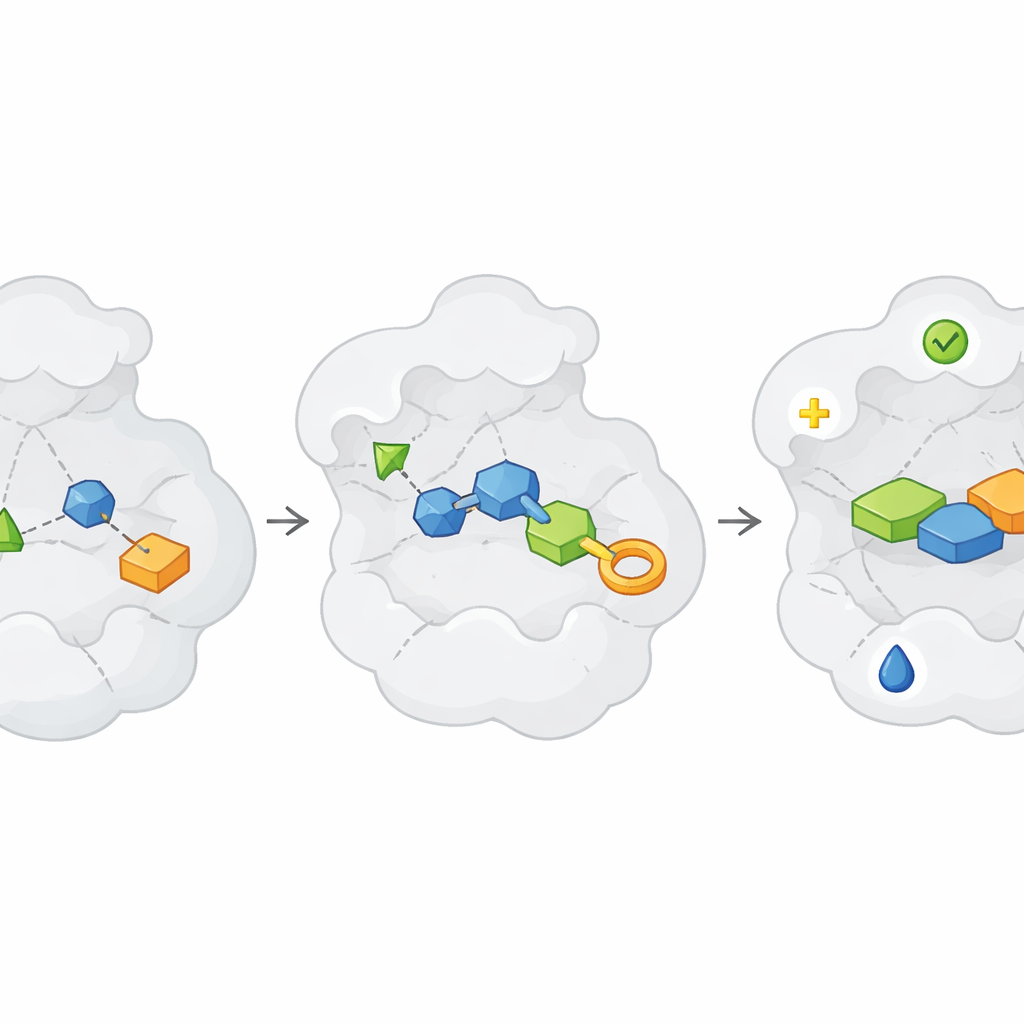
Sintesi e test su larga scala senza rallentare
Un importante collo di bottiglia nella scoperta di farmaci è semplicemente produrre e purificare abbastanza composti da testare. L’articolo descrive come robot per la sintesi ad alto rendimento, la chimica in flusso e nuovi metodi di estrazione possano sfornare centinaia o migliaia di molecole correlate attorno a un framment hit. Alcuni approcci addirittura saltano la purificazione completa all’inizio: miscele di reazione grezze vengono testate direttamente in assay sensibili come la cristallografia, misure cinetiche o NMR, un approccio talvolta chiamato “direct-to-biology”. Controlli di qualità come la spettrometria di massa sono usati in parallelo per tracciare quali miscele contengono effettivamente il prodotto desiderato. Sebbene i dati possano essere rumorosi, combinare questi test rapidi con analisi intelligenti e successive sintesi pulite permette ai ricercatori di mappare le relazioni struttura–attività molto più rapidamente rispetto alla chimica tradizionale uno per uno.
Cosa significa questo per i medicinali del futuro
Nel complesso, l’articolo conclude che la drug discovery basata su frammenti è maturata in una strategia potente e flessibile per trovare nuovi medicinali, specialmente se accoppiata con automazione moderna e IA. Partire da blocchi costruttivi minuscoli ed efficienti permette agli scienziati di esplorare lo spazio chimico in modo più ponderato, ma richiede una validazione attenta perché i segnali iniziali sono così deboli. Gli autori sostengono che i maggiori guadagni deriveranno dall’integrazione stretta di design, sintesi e test in flussi di lavoro semi-automatizzati e guidati dai dati, condividendo nel contempo dati e metodi sui frammenti in modo aperto così che anche i gruppi con risorse limitate possano beneficiare. Se questi sviluppi continueranno, gli approcci basati su frammenti potrebbero contribuire a invertire il declino a lungo termine della produttività della ricerca e accelerare l’arrivo di farmaci più sicuri ed efficaci per un’ampia gamma di malattie.
Citazione: Grosjean, H., Biggin, P.C. Developments and challenges in hit progression within fragment-based drug discovery. Nat Commun 17, 2226 (2026). https://doi.org/10.1038/s41467-026-68941-z
Parole chiave: drug discovery basata su frammenti, ottimizzazione da hit a lead, ciclo design-make-test, screening ad alto rendimento, progettazione farmaceutica computazionale