Clear Sky Science · it
Espansione clonale di linfociti T citotossici CD8⁺ associata ad ARIA da lecanemab
Perché questo è importante per le persone con Alzheimer
Il lecanemab è uno dei primi farmaci in grado di rimuovere l’amiloide dal cervello e di rallentare in misura modesta la perdita di memoria nella malattia di Alzheimer. Tuttavia, alcuni pazienti trattati con questa terapia sviluppano edema cerebrale o piccole emorragie cerebrali, alterazioni visibili alla risonanza magnetica raccolte sotto il termine anomalie di imaging correlate all’amiloide (ARIA). Questo studio pone una domanda cruciale per pazienti e famiglie: cosa succede nel sistema immunitario quando compare l’ARIA, e potrebbe un semplice esame del sangue un giorno aiutare a prevedere chi è più a rischio?
La promessa e il rischio di un nuovo trattamento per l’Alzheimer
Il lecanemab è un anticorpo somministrato per infusione che prende di mira gli aggregati di una proteina chiamata beta‑amiloide, caratteristica della malattia di Alzheimer. Favorendo la rimozione dell’amiloide, può rallentare in modo modesto il declino cognitivo. Ma questo beneficio comporta una preoccupazione per la sicurezza: alcune persone sviluppano ARIA, che può includere aree di edema cerebrale o microemorragie. Questi effetti collaterali richiedono monitoraggio frequente con risonanza magnetica e possono limitare l’accesso al farmaco. Non tutti sono ugualmente vulnerabili: i portatori di una variante genetica chiamata APOE4 sono a rischio maggiore, ma i geni da soli non spiegano perché l’ARIA si manifesti, specialmente nelle fasi iniziali del trattamento. Poiché il lecanemab viene somministrato attraverso il circolo sanguigno, gli autori hanno ipotizzato che un’analisi approfondita delle cellule immunitarie nel sangue potesse rivelare segnali di avvertimento precoci o meccanismi che collegano il trattamento a danni vascolari nel cervello. 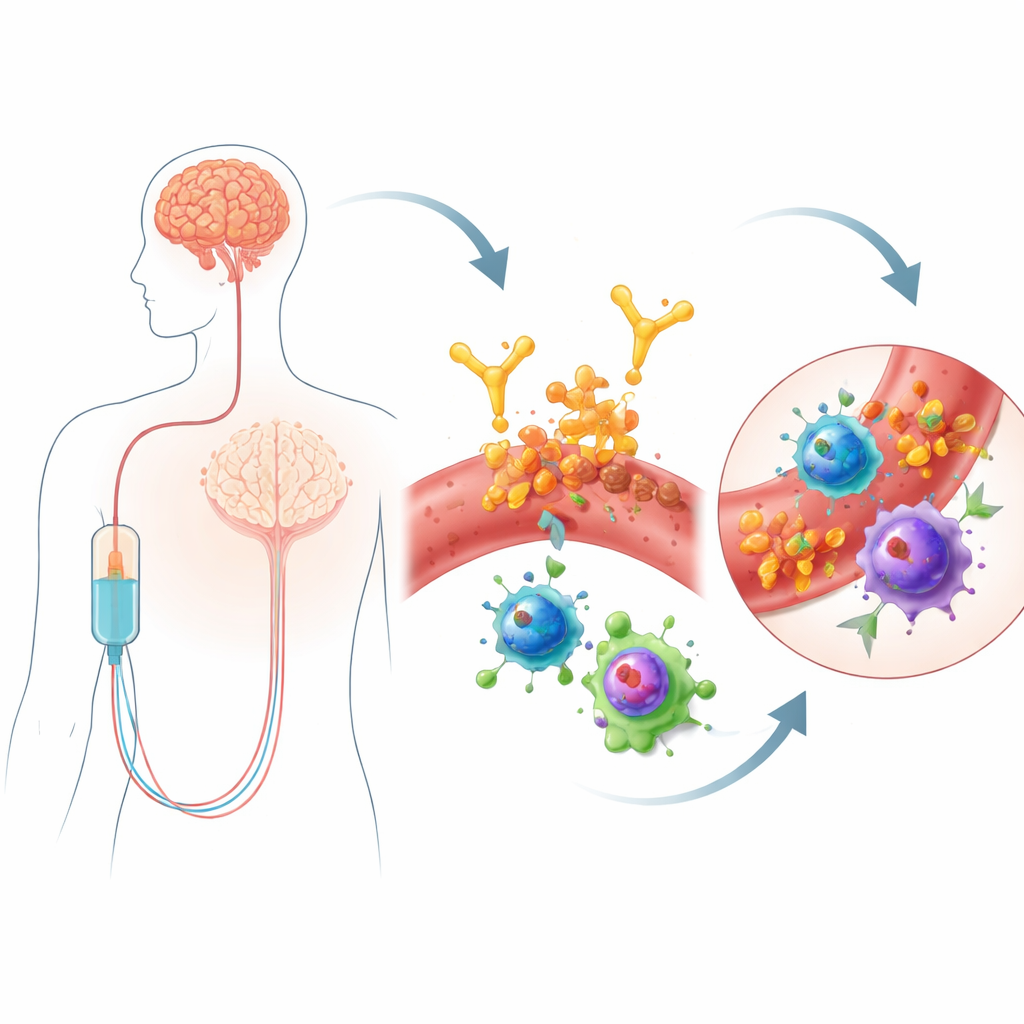
Monitorare le cellule immunitarie nei pazienti che hanno sviluppato o meno ARIA
I ricercatori hanno studiato sei persone con Alzheimer in trattamento con lecanemab presso una clinica regionale della memoria. Tre hanno sviluppato varie forme di ARIA e tre pazienti controlli corrispondenti (simili per età, sesso, genotipo APOE e numero di infusioni) non l’hanno sviluppata. Il sangue è stato prelevato appena prima delle infusioni e il team ha usato un approccio intensivo "multi‑omico": sequenziamento dell’RNA a cellula singola per leggere quali geni erano attivi in migliaia di singole cellule immunitarie, marcatori anticorpali per definire i tipi cellulari, sequenziamento dei recettori delle cellule T per tracciare i cloni e metabolomica mirata per misurare centinaia di piccole molecole coinvolte nel metabolismo cellulare. Questo ha permesso di chiedersi non solo quali tipi cellulari fossero presenti, ma quanto fossero attivi, quale carburante utilizzassero e se specifiche famiglie di cellule T si espandessero in risposta a qualche stimolo.
Espansione di linfociti T killer altamente armati
È emerso uno schema chiaro nei pazienti che hanno sviluppato ARIA. Rispetto ai controlli, avevano una proporzione più alta di linfociti T CD8 "killer" e meno linfociti T CD4 helper. All’interno del comparto CD8, due sottogruppi si sono distinti: le cellule della memoria effettrice e una forma terminalmente differenziata nota come cellule TEMRA. Queste TEMRA sono come soldati veterani—altamente specializzate per l’attacco, dotate di meccanismi potenti per uccidere le cellule bersaglio. Nei pazienti ARIA‑positivi, le cellule TEMRA erano più numerose, più clonalmente espanse (cioè particolari famiglie di cellule T si erano moltiplicate) e mostravano programmi genici associati a citotossicità, migrazione lungo i vasi sanguigni e segni di stimolazione cronica. Stati di cellule T simili sono stati osservati nell’invecchiamento, nelle infezioni croniche, nella sclerosi multipla e nel liquido cerebrospinale di persone con Alzheimer, dove possono accumularsi vicino ai vasi sanguigni e alla superficie cerebrale.
Rimodellamento metabolico e dialogo con altre cellule immunitarie
Il gruppo ha inoltre rilevato che queste cellule effettrici CD8 avevano rimodellato il loro metabolismo. Invece di fare principalmente affidamento sulla produzione efficiente di energia nei mitocondri, si erano spostate verso la glicolisi, una via più rapida ma meno efficiente che sostiene attività intense e di breve durata. Le misurazioni dei metaboliti nelle cellule del sangue hanno confermato questo quadro: i livelli di lattato e piruvato erano aumentati, mentre componenti chiave del ciclo dell’acido citrico risultavano ridotti, uno schema tipico delle cellule immunitarie infiammatorie. I monociti, un altro tipo di globuli bianchi, hanno mostrato cambiamenti complementari. Nei pazienti ARIA‑positivi i monociti attivavano geni per la presentazione degli antigeni, per l’adesione alle altre cellule e per la produzione di chemochine—segnali chimici che attirano le cellule T. La modellizzazione computazionale delle coppie ligando‑recettore ha suggerito che i monociti inviassero segnali di attivazione e richiamo più forti alle cellule effettrici CD8, creando un ambiente che favorisce l’interazione di questi killer con le pareti vascolari.
Codici di indirizzo che guidano le cellule T verso i vasi cerebrali
Poiché questo studio ha campionato solo il sangue, gli autori si sono rivolti a un dataset indipendente a cellula singola proveniente da cervelli di pazienti trattati con lecanemab per verificare se gli stessi programmi delle cellule T fossero collegati a nicchie vascolari nel cervello. Quando hanno proiettato i loro sottogruppi CD8 su questa mappa cerebrale, le cellule TEMRA e della memoria effettrice dei pazienti ARIA‑positivi mostravano "codici di indirizzo" trascrizionali—combinazioni di molecole di adesione e recettori per chemochine—that corrispondevano alle cellule endoteliali (dei vasi sanguigni) nel cervello malato. Queste firme suggeriscono che i linfociti T espansi non siano solo altamente armati e metabolicamente attivati, ma anche predisposti a dirigersi verso e interagire con vasi cerebrali stressati nei siti di rimozione dell’amiloide. 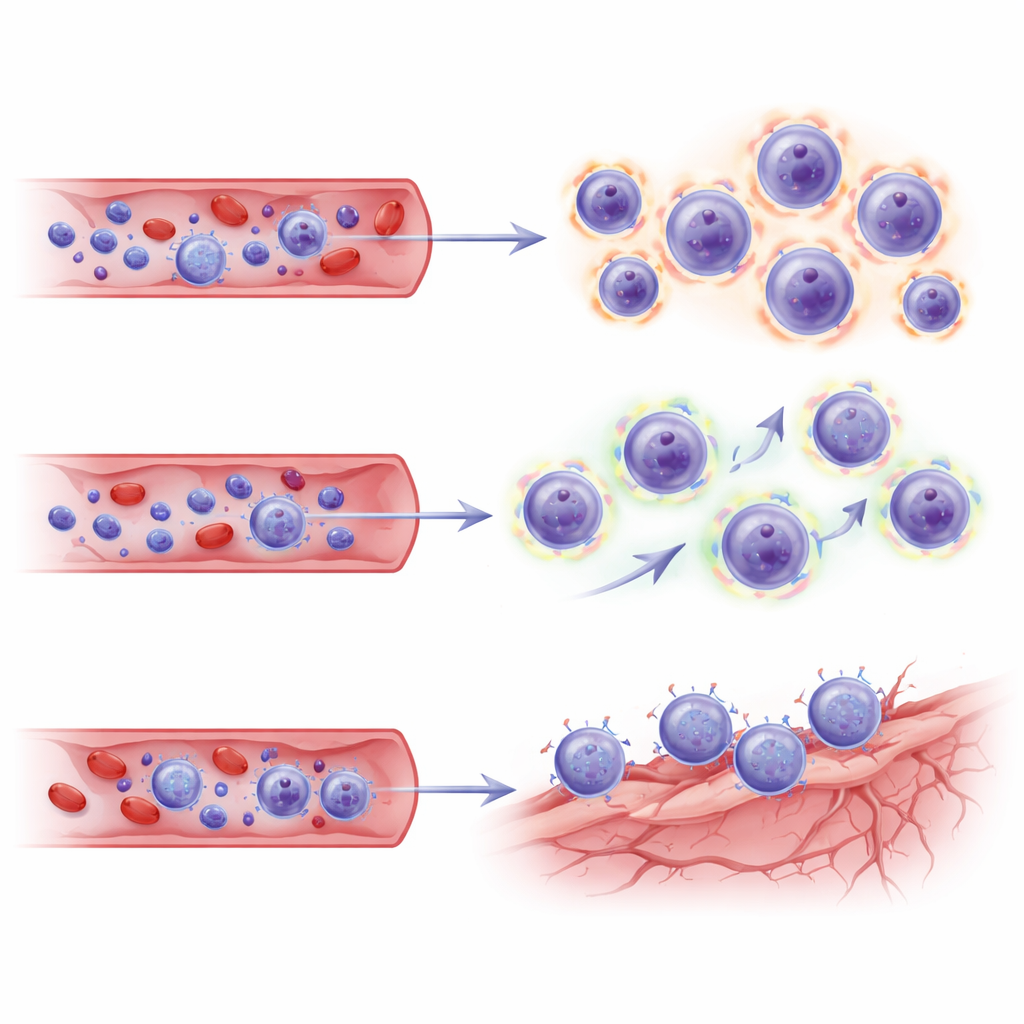
Cosa potrebbe significare per i pazienti e per le cure future
Nel complesso, questo studio, piccolo ma dettagliato, dipinge l’ARIA come qualcosa di più di un effetto collaterale passivo della rimozione dell’amiloide. Piuttosto, sembra connessa a una risposta immunitaria coordinata nel sangue: espansione e attivazione metabolica di specifici cloni di linfociti T killer, potenziamento dei segnali dai monociti e caratteristiche molecolari che favoriscono l’interazione con i vasi cerebrali. Il lavoro non dimostra che queste cellule siano la causa dell’ARIA—i cambiamenti immunitari potrebbero essere una reazione al danno vascolare piuttosto che la sua fonte—ma fornisce ipotesi verificabili e una traccia per biomarcatori basati sul sangue. In futuro, misurare l’abbondanza e lo stato metabolico delle cellule CD8 TEMRA, insieme a molecole di segnalazione chiave, potrebbe aiutare a identificare i pazienti a rischio più elevato di ARIA, guidare i programmi di monitoraggio o persino ispirare strategie mirate per modulare temporaneamente questa risposta immunitaria mantenendo i benefici delle terapie che rimuovono l’amiloide.
Citazione: Johnson, L.A., Saito, K., Pallerla, A.V. et al. Clonal expansion of cytotoxic CD8⁺ T cells in lecanemab-associated ARIA. Nat Commun 17, 2180 (2026). https://doi.org/10.1038/s41467-026-68921-3
Parole chiave: Malattia di Alzheimer, lecanemab, cellule immunitarie, vasi sanguigni cerebrali, effetti collaterali del trattamento