Clear Sky Science · it
Le proteine TMEM63 agiscono come scramblasi lipidici attivati meccanicamente e modulati dal colesterolo contribuendo alla meccano-resilienza della membrana
Come le cellule restano intatte sotto stress fisico
Le cellule del nostro corpo sono continuamente compressi, allungati e scosse, sia nei cuori che battono, nei muscoli al lavoro o nei tumori che spingono attraverso i tessuti. Questo studio rivela come una famiglia di proteine di membrana, chiamata OSCA/TMEM63, aiuti le cellule a sopravvivere a forze meccaniche intense riorganizzando i grassi nel loro involucro esterno. Capire questo sistema ammortizzatore integrato potrebbe offrire nuove prospettive su disturbi dell’udito, dell’isolamento nervoso e persino sulla diffusione del cancro.
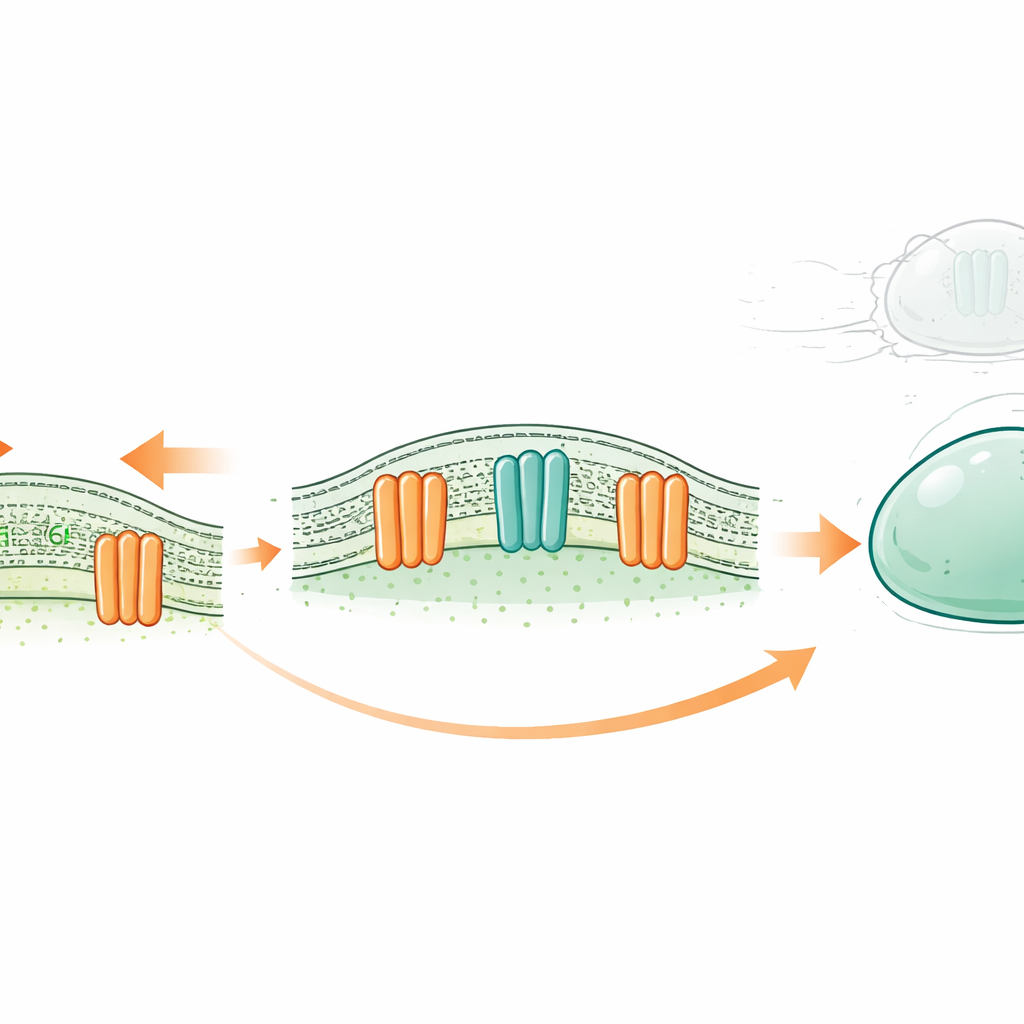
Un nuovo tipo di ammortizzatore cellulare
Ogni cellula è avvolta da una sottile membrana oleosa composta da due strati di molecole simili a grassi chiamate lipidi. Tradizionalmente, alcune proteine di membrana venivano considerate esclusivamente canali ionici—piccole valvole che permettono il passaggio di particelle cariche in risposta a stimoli come l’allungamento. La famiglia OSCA/TMEM63, presente dalle piante agli esseri umani, è nota per aprirsi in risposta alla tensione di membrana. Lavori strutturali precedenti avevano suggerito che, a differenza dei canali ionici classici, i loro pori sono in parte rivestiti dagli stessi lipidi. Questo ha sollevato una possibilità provocatoria: questi canali potrebbero anche agire come “scramblasi”, invertendo la posizione dei lipidi tra lo strato interno e quello esterno della membrana quando la cellula è sottoposta a forza?
Osservare i lipidi che ruotano attraverso la membrana
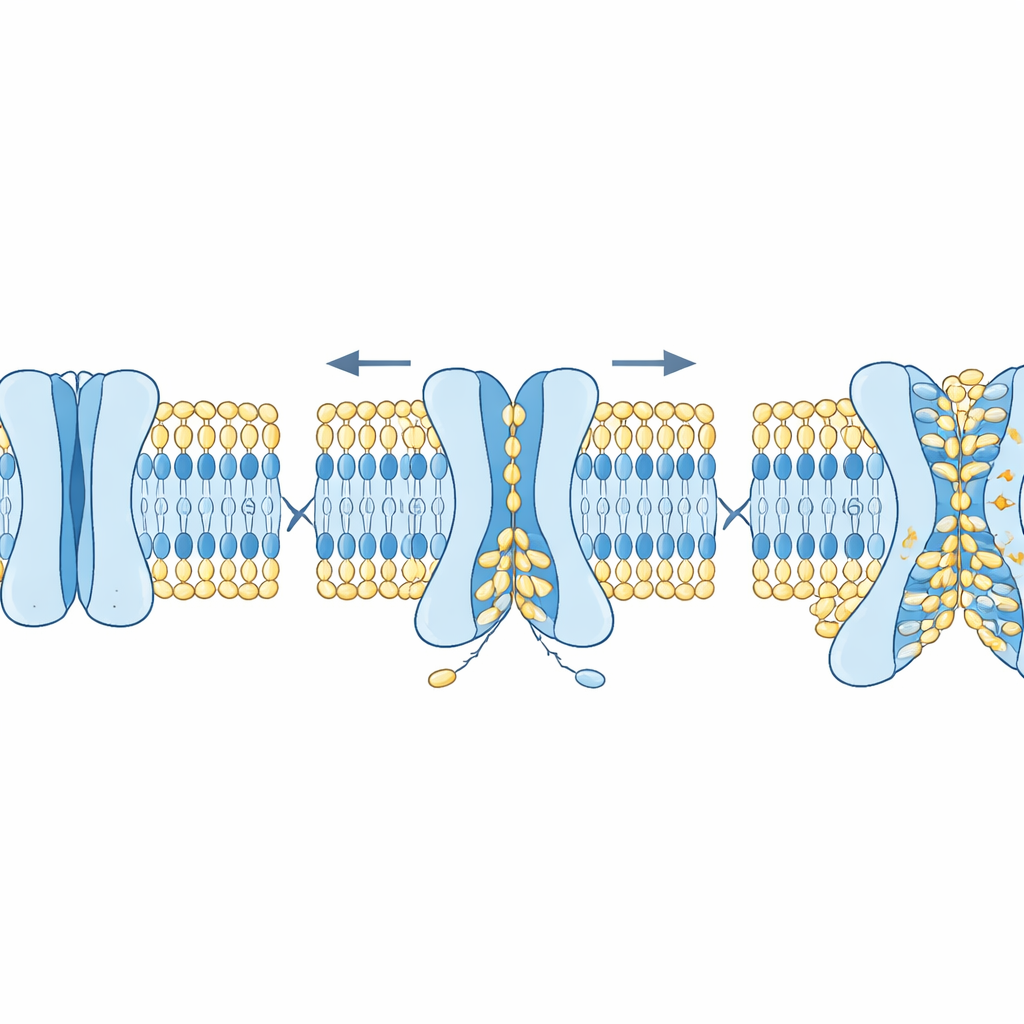
Per verificare questa ipotesi, gli autori hanno combinato simulazioni al computer con sistemi sperimentali riduzionisti costruiti da componenti purificati. Nelle simulazioni, versioni aperte di diverse proteine OSCA e TMEM63 sono state inserite in membrane modello. Le molecole lipidiche si sono mosse spontaneamente attraverso una scanalatura in queste proteine da un lato del doppio strato all’altro, formando una cintura che collegava le due foglie lasciando al contempo un percorso riempito d’acqua per gli ioni. In esperimenti paralleli, il gruppo ha costruito gigantesche “bolle” artificiali (vescicole) contenenti lipidi fluorescenti e proteine specifiche. Quando un agente esterno spegneva la fluorescenza sulla superficie esterna, qualsiasi ulteriore calo del segnale poteva essere spiegato solo dal ribaltamento dei lipidi dallo strato interno verso l’esterno. Le vescicole contenenti OSCA1.1, OSCA1.2, OSCA2.2 o TMEM63A/B hanno mostrato questa perdita supplementare di fluorescenza, indicando uno scrambling attivo, mentre i canali di controllo che non scambiano lipidi non lo hanno fatto.
Come la struttura e il colesterolo modulano il processo
I ricercatori hanno quindi chiesto quali caratteristiche delle proteine TMEM63 controllino questo comportamento duale. Usando AlphaFold2, hanno generato molte forme plausibili delle proteine umane TMEM63, dal chiuso al sempre più aperto. Le simulazioni hanno rivelato che un piccolo numero di amminoacidi ingombranti agiscono come “strozzature” nella scanalatura. Una residuo limita principalmente il flusso ionico, mentre altri ostacolano il movimento dei lipidi. Mutare la strozzatura ionica aumentava la conduttanza elettrica senza modificare molto lo scrambling lipidico, mentre mutare la porta dei lipidi rendeva i lipidi più propensi a ribaltarsi e persino faceva comparire sulle cellule segnali di “mangiami” sulla superficie senza alcuno stimolo aggiuntivo. Un altro regolatore chiave è stato il colesterolo, un componente che irrigidisce le membrane cellulari. Aggiungere colesterolo alle membrane modello rallentava notevolmente lo scrambling lipidico e stabilizzava lo stato chiuso di TMEM63A, sia nelle simulazioni sia nelle strutture ottenute con crio–microscopia elettronica in cui il colesterolo si annidava in siti specifici sulla proteina.
La forza meccanica come interruttore
Se il colesterolo normalmente frena lo scrambling all’interno delle cellule, cosa lo attiva al momento giusto? Il team ha usato molecole zuccherine ad anello chiamate ciclodextrine per estrarre selettivamente lipidi dalle membrane e così aumentare la tensione senza rimuovere il colesterolo. Nelle vescicole di dimensioni cellulari, l’aggiunta di ciclodextrina ha attivato lo scrambling lipidico da parte di TMEM63A solo quando la proteina era presente, dimostrando che lo stress meccanico da solo può scatenare il ribaltamento. Approcci simili in cellule vive hanno mostrato che la sola rimozione lieve del colesterolo non era sufficiente; era necessaria una sfida meccanica successiva per osservare uno scrambling marcato. Quando cellule ingegnerizzate per esprimere TMEM63A venivano ripetutamente allungate, esponevano rapidamente certi lipidi sulla superficie esterna, un segno distintivo dello scrambling, mentre le cellule prive di queste proteine mostravano cambiamenti molto più contenuti.
Proteggere le cellule dalla rottura
Oltre al ribaltamento dei lipidi, lo scrambling attivato meccanicamente modificava il comportamento fisico delle membrane sotto stress estremo. In vescicole artificiali esposte a forze elevate, quelle prive di scramblasi tendevano a scoppiare, mentre le vescicole contenenti TMEM63A o uno scramblasi noto si contraevano, formavano tubuli sottili e in gran parte restavano integre. In una linea cellulare di cancro cerebrale umano che esprime naturalmente TMEM63A e TMEM63B, la riduzione dei livelli di una qualsiasi delle due proteine aumentava la probabilità che le cellule si rompessero quando sottoposte a forte stress meccanico. Nel loro insieme, questi risultati supportano un modello in cui le proteine OSCA/TMEM63 agiscono come valvole che si aprono sotto tensione e attenuano temporaneamente la differenza abituale tra le facce interna ed esterna della membrana. Permettendo ai lipidi di ridistribuirsi rapidamente, aiutano a equalizzare lo stress e a prevenire lacerazioni catastrofiche.
Cosa significa per la salute e la malattia
In termini semplici, questo lavoro mostra che alcuni canali sensibili allo stiramento fanno più che condurre segnali elettrici: riorganizzano anche la “pelle” esterna della cellula per aiutarla a sopravvivere alla compressione. Le proteine TMEM63 emergono come scramblasi lipidici attivati meccanicamente la cui attività è finemente modulata dalla composizione della membrana, in particolare dal colesterolo. Questo meccanismo di meccano-resilienza può essere importante ovunque le cellule siano esposte a grandi forze, dagli assoni isolanti e dalle cellule sensoriali dell’udito fino alle cellule tumorali che si fanno strada attraverso tessuti densi. Comprendere e, in futuro, manipolare questa funzione doppia canale ionico–scramblasi potrebbe aprire nuove strade per proteggere tessuti vulnerabili—o, al contrario, per rendere più fragili cellule tumorali difficili da eliminare.
Citazione: Lin, Y., Zhou, Z., Han, Y. et al. TMEM63 proteins act as mechanically activated cholesterol modulated lipid scramblases contributing to membrane mechano-resilience. Nat Commun 17, 2717 (2026). https://doi.org/10.1038/s41467-026-68919-x
Parole chiave: canali ionici meccanosensibili, scrambling lipidico, meccanica della membrana cellulare, regolazione del colesterolo, proteine TMEM63 OSCA