Clear Sky Science · it
Un peptide crittico neurotossico derivante dallo splicing critico di PKN1 dipendente da TDP-43
Minacce nascoste all’interno delle cellule cerebrali
Molte malattie cerebrali, tra cui la sclerosi laterale amiotrofica (SLA) e la malattia di Alzheimer, sono caratterizzate dall’accumulo di ammassi di una proteina chiamata TDP-43. Gli scienziati sanno che quando questa proteina smette di funzionare correttamente, i neuroni perdono messaggi vitali e alla fine muoiono. Questo studio rivela una svolta più sorprendente: il malfunzionamento di TDP-43 può anche indurre le cellule cerebrali a produrre un mini‑proteina precedentemente sconosciuta e tossica, che a sua volta danneggia i circuiti della memoria. Comprendere questo attore nascosto può aprire nuove strade per la diagnosi e il trattamento di demenze devastanti.
Come un correttore cellulare mantiene l’RNA in ordine
All’interno dei neuroni, TDP-43 agisce come un correttore per l’RNA, i messaggi intermedi che collegano il DNA alle proteine. Si lega a brevi sequenze specifiche e impedisce l’inserimento di “pezzi extra” indesiderati in questi messaggi. Quando TDP-43 viene perso o si localizza in modo anomalo, come nella SLA e in molti casi di Alzheimer, questi pezzi extra—chiamati esoni crittici—possono inserirsi nell’RNA. Finora, la maggior parte degli esoni crittici conosciuti causava semplicemente la perdita della proteina normale rendendo il messaggio instabile e rapidamente degradato. Non era chiaro se tali eventi potessero anche generare nuove proteine dannose.
Uno splicing crittico crea un frammento tossico
Gli autori si sono concentrati su un gene chiamato PKN1, che contribuisce a mantenere l’impalcatura interna e il flusso di segnalazione dei neuroni. Utilizzando modelli cellulari in cui TDP-43 era ridotto, hanno scoperto un esone crittico precedentemente non riconosciuto, denominato PKN1‑5a1, inserito tra due segmenti normali dell’RNA di PKN1. Questa inserzione introduce un segnale di stop precoce, producendo un RNA abbreviato. Sorprendentemente, parte di questo messaggio difettoso sfugge al sistema di controllo qualità della cellula ed è tradotto in un frammento stabile della proteina PKN1 contenente solo i primi 207 amminoacidi. Il gruppo ha chiamato questo prodotto troncato PKN207. Hanno dimostrato che TDP-43 normalmente previene questo errore legandosi a diverse regioni ricche di UG che fiancheggiano l’esone crittico; quando questo legame viene perso, l’esone viene inserito e PKN207 viene prodotto.
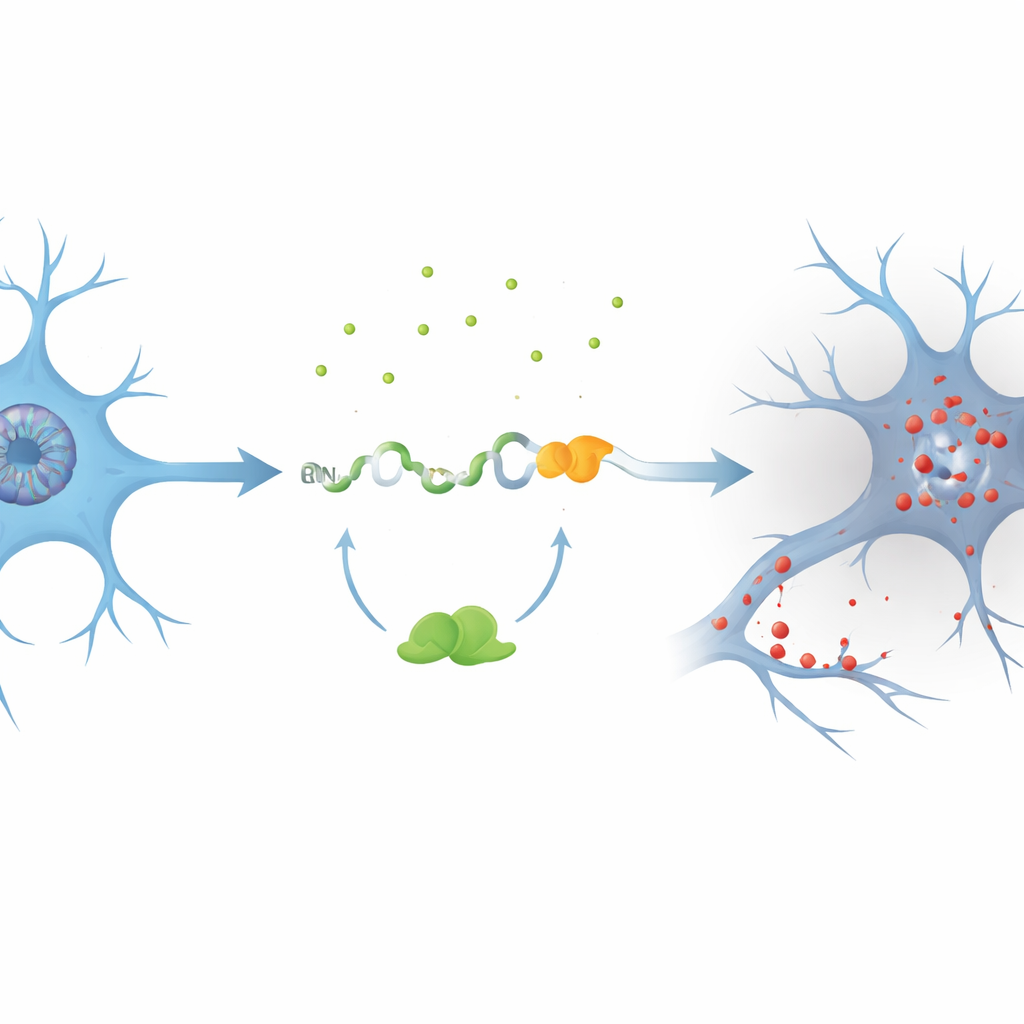
Prove da cervelli di pazienti e grandi dataset
Per verificare se questo evento avviene nella malattia umana, i ricercatori hanno analizzato dati di RNA-seq provenienti da centinaia di campioni di cervello e midollo spinale di pazienti con SLA. Hanno rilevato un’attivazione diffusa dell’esone crittico PKN1‑5a1 in aree note per essere colpite dalla patologia di TDP-43, come la corteccia motoria e il midollo spinale, ma non nel cervelletto relativamente risparmiato. Hanno quindi generato anticorpi altamente specifici che riconoscono solo la coda unica di PKN207, non la proteina PKN1 a lunghezza intera. Nel tessuto ippocampale di pazienti con Alzheimer che presentavano anche TDP-43 anomalo e fosforilato, questi anticorpi hanno rilevato una banda distinta corrispondente a PKN207, mentre tale banda era assente nei cervelli di controllo. Ulteriori dataset di Alzheimer hanno confermato che l’esone crittico è attivato anche nelle fasi precoci della malattia, suggerendo che questo errore molecolare potrebbe iniziare molto prima che i sintomi diventino evidenti.
Una mini‑proteina con grande impatto sulla memoria
La presenza di PKN207 nel cervello umano malato ha sollevato la domanda chiave: è dannoso? Per testarlo, il gruppo ha usato virus per indurre la produzione di PKN1 normale o di PKN207 specificamente nell’ippocampo—una regione cerebrale critica per la memoria—di topi giovani. Mesi dopo, entrambi i gruppi di topi mostravano difficoltà di apprendimento nel test del labirinto d’acqua di Morris, nuotando più a lungo per trovare una piattaforma nascosta. Il loro liquido cerebrospinale conteneva livelli più elevati di una proteina strutturale, la catena leggera dei neurofilamenti, un marcatore di danno assonale. In neuroni coltivati, l’aumento di PKN207 ha innescato lesioni cellulari, misurate tramite fuoriuscita di un enzima indicativo di danno alla membrana. Un profilo proteico dettagliato dell’ippocampo ha rivelato ampie alterazioni in vie legate alla forza sinaptica (potenziamento a lungo termine) e a note malattie neurodegenerative, con una perturbazione particolarmente marcata di molecole che supportano una segnalazione efficiente e un’impalcatura di fibre nervose sana.
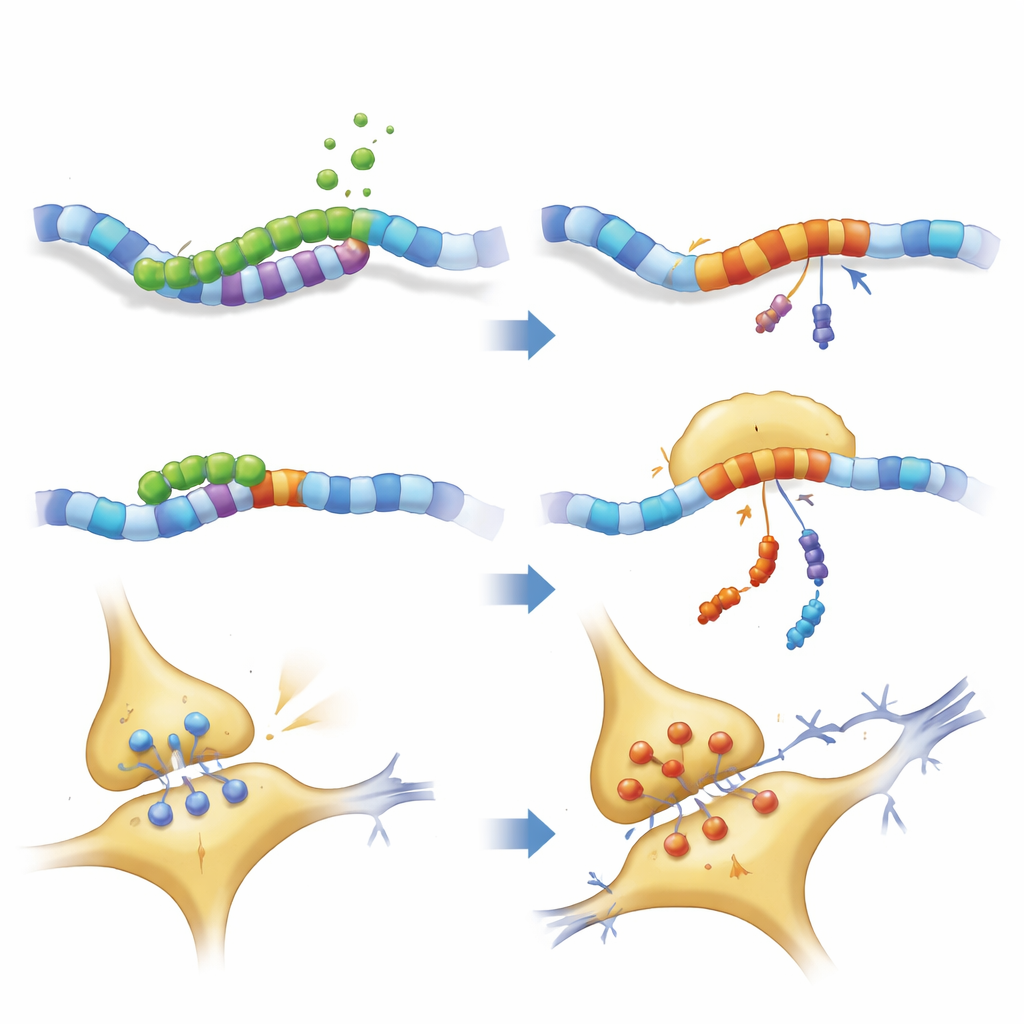
Come il frammento sconvolge il cablaggio cerebrale
Un esame più approfondito della struttura neuronale ha mostrato che sia PKN1 a lunghezza intera sia PKN207 alteravano la rete dei neurofilamenti che conferisce agli assoni la loro forma e aiuta il trasporto del carico. Proteine motorie e strutturali chiave risultavano ridotte, mentre alcuni componenti dei neurofilamenti si accumulavano, suggerendo ingorghi nel traffico e possibili aggregazioni. Registrazioni elettriche da fette ippocampali hanno confermato che i topi che esprimevano PKN207 avevano un potenziamento a lungo termine indebolito—il processo mediante il quale le sinapsi si rafforzano dopo attività ripetuta e una base cellulare ampiamente accettata per apprendimento e memoria. Pur mancando il dominio enzimatico di PKN1, la presenza di PKN207 era sufficiente a imitare e talvolta superare gli effetti disturbanti della proteina completa, implicando che la regione N-terminale condivisa può, da sola, interferire con l’omeostasi neuronale.
Perché questa scoperta è importante per le malattie cerebrali
Questo lavoro aggiunge un nuovo livello alla nostra comprensione dei disturbi correlati a TDP-43. Piuttosto che causare soltanto la perdita di RNA essenziali, il malfunzionamento di TDP-43 può anche generare un micro‑proteina stabile e tossica che compromette sinapsi e cognizione. L’esone crittico PKN1‑5a1 e il suo peptide prodotto PKN207 emergono ora come potenziali biomarcatori di disfunzione precoce di TDP-43 e come possibili bersagli per terapie che correggono lo splicing o bloccano il frammento nocivo. Più in generale, lo studio suggerisce che altri esoni nascosti potrebbero a loro volta dare origine a peptidi promotori di malattia, indicando ai ricercatori un panorama ricco—e precedentemente trascurato—di colpevoli molecolari nella neurodegenerazione.
Citazione: Yang, M., Wang, Q., Yan, R. et al. A neurotoxic cryptic peptide arising from TDP-43-dependent cryptic splicing of PKN1. Nat Commun 17, 2963 (2026). https://doi.org/10.1038/s41467-026-68916-0
Parole chiave: TDP-43, splicing critico, PKN1, neurodegenerazione, Alzheimer e SLA