Clear Sky Science · it
Controli epigenetici delle proteine FOX regolano l’equilibrio lisi‑latenza del herpesvirus
Perché i virus erpetici nascosti contano
Molte persone convivono per tutta la vita con i virus herpes simplex, spesso senza saperlo. Questi virus possono rimanere silenti all’interno dei neuroni per anni e poi riattivarsi all’improvviso, causando herpes labiale, malattie oculari o problemi più gravi in persone con sistema immunitario compromesso. Ciò che mantiene il virus «addormentato» nella maggior parte dei casi, e ciò che lo riaccende, è stato a lungo un enigma. Questo studio mette in luce una componente chiave di quel sistema di controllo: una lotta tra due gruppi opposti di proteine umane che rimodellano il DNA virale e determinano se l’herpes resta silente o inizia a produrre nuovi virus.
Due squadre cellulari che tirano in direzioni opposte
Gli autori si sono concentrati su una vasta famiglia di proteine umane leganti il DNA chiamate proteine FOX, che normalmente regolano i nostri geni durante lo sviluppo e il metabolismo. Testando molti membri della famiglia FOX in cellule con caratteristiche neuronali, hanno identificato due schieramenti distinti. Un gruppo (inclusi proteine come FOXF1) ha fortemente favorito la replicazione del virus herpes simplex di tipo 1 (HSV‑1) e di diversi alfaherpesvirus correlati. Un altro gruppo (FOXK1 e FOXK2) ha fatto l’opposto, sopprimendo vigorosamente la crescita virale. Questo equilibrio non era identico in tutti i tipi cellulari: le cellule non neuronali e i neuroni sotto stress tendevano a produrre più proteine FOX attivatrici, mentre i neuroni sensoriali a riposo esprimevano pochissimo le FOX attivatrici ma alti livelli delle FOX repressorie FOXK.
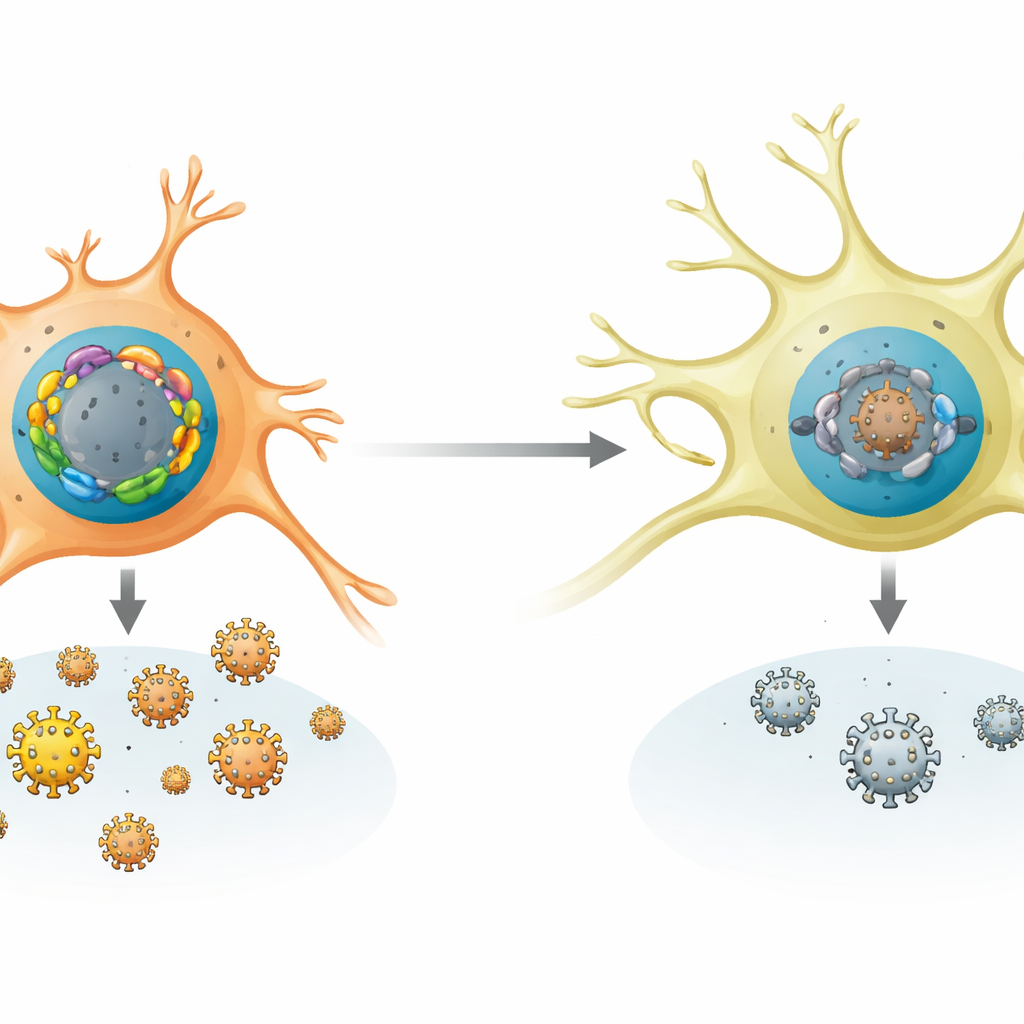
Come i neuroni favoriscono lo stato silente
Il gruppo ha confrontato l’attività genica delle FOX in molti tipi cellulari umani e murini e in animali infetti. I neuroni sensoriali, il sito naturale della latenza di HSV‑1, mostravano uno schema che favorisce il silenzio: forte espressione di FOXK1 e FOXK2 e bassa espressione della maggior parte delle FOX attivatrici. Nei topi, l’infezione iniziale e successivi segnali di stress come il calore o lesioni tissutali aumentavano selettivamente i livelli di diverse Fox attivatrici senza ridurre quelle repressorie. In neuroni murini coltivati e in topi viventi, la delezione o il knockdown delle FOXK ha facilitato la replicazione di HSV‑1 e la riattivazione dalla latenza. Al contrario, indurre nei neuroni la produzione di FOX attivatrici in eccesso era sufficiente a scatenare la riattivazione anche in assenza di trigger chimici, dimostrando quanto lo stato virale sia sensibile a questo equilibrio tra FOX.
Afferrare il DNA virale e aprirlo o chiuderlo
Per comprendere il meccanismo sottostante, i ricercatori hanno mappato dove le proteine FOX si legano sul genoma virale. Hanno scoperto che sia l’attivatrice FOXF1 sia la repressoria FOXK1 si legano ampiamente al DNA di HSV‑1, non solo in pochi motivi di sequenza specifici. Questo legame dipende da una regione conservata delle proteine FOX che afferra la spina dorsale del DNA piuttosto che singole basi, permettendo loro di attaccarsi quasi ovunque. Una volta posizionate, le due «fazioni» reclutano partner molecolari diversi che rimodellano la cromatina, la combinazione di DNA e delle sue proteine di impacchettamento. Le FOX attivatrici, in particolare FOXF1, si associano a CBP e P300, enzimi che aggiungono gruppi acetile agli istoni e allentano la cromatina. Questo rende il DNA virale più accessibile e potenzia l’espressione dei geni virali precoci, medi e tardivi. FOXK1, al contrario, lavora con fattori come SIN3A e MAX, associati alla deacetilazione degli istoni e alla repressione genica, stringendo la cromatina virale e mantenendo i geni spenti.
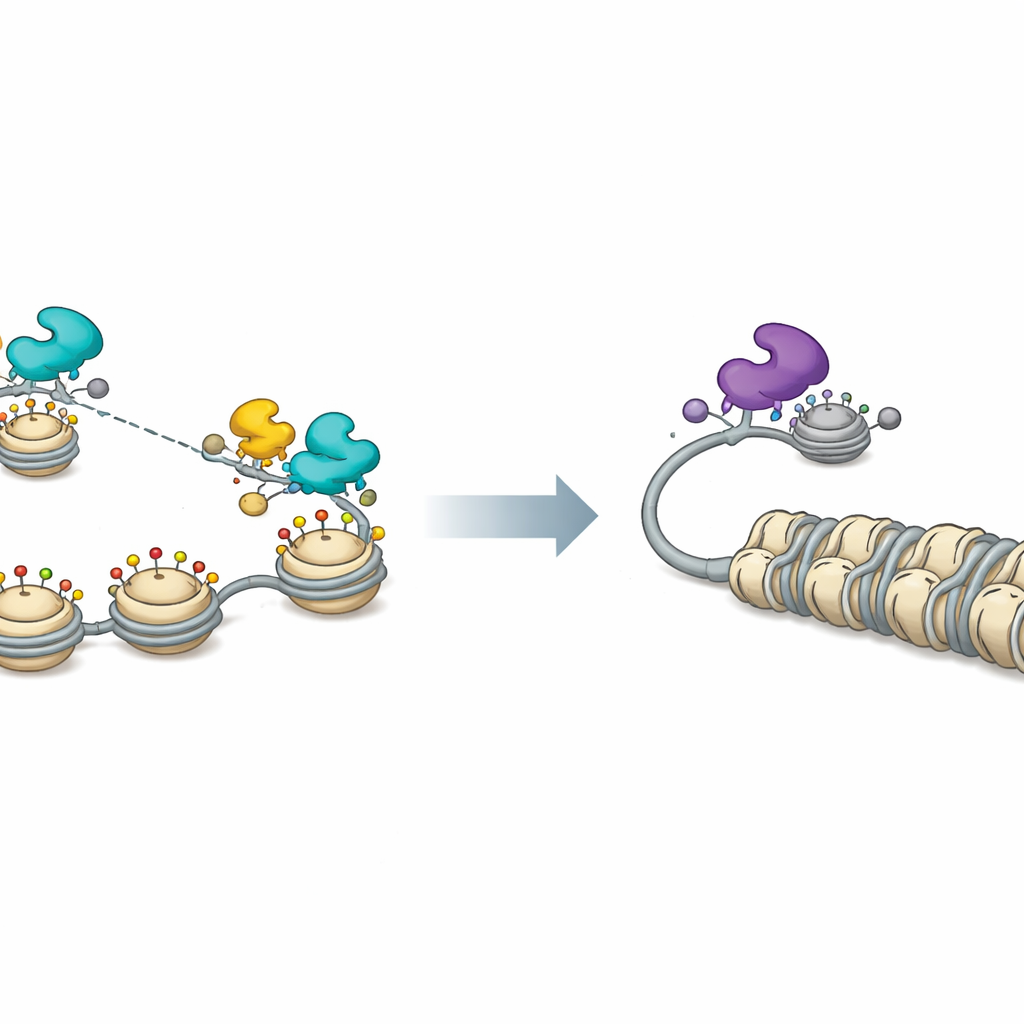
Un interruttore cromatinico per il sonno e il risveglio virale
Le misurazioni sulla cromatina virale hanno confermato questo quadro. Quando FOXF1 era presente, gli istoni sul DNA virale risultavano rimossi o chimicamente modificati in modi associati a una cromatina aperta e attiva, e l’accessibilità complessiva dei promotori virali aumentava su tutto il genoma. L’espressione di FOXF1 disperdeva anche piccole strutture nucleari chiamate corpi nucleari PML, che normalmente contribuiscono a mantenere il DNA virale represso. L’inibizione di CBP e P300 annullava molti di questi effetti attivatori e riduceva l’espressione genica virale indotta da FOXF1. Sul versante repressivo, i ricercatori hanno mostrato che i partner associati a FOXK1 e l’attività delle deacetilasi istoniche sono importanti per mantenere bassa la replicazione di HSV‑1; l’inibizione chimica delle deacetilasi aumentava la produzione virale e indeboliva la soppressione mediata da FOXK1.
Cosa significa per il controllo delle infezioni lifelong
Nel complesso, il lavoro suggerisce che lo stato attivo o dormiente di HSV‑1 dipende in larga misura dal mix di proteine FOX nel neurone ospite. I neuroni sensoriali a riposo favoriscono naturalmente lo stato repressivo dominato da FOXK, spingendo il virus in una forma profondamente silente e cromatinicamente compattata. Stress o altre condizioni che aumentano le FOX attivatrici possono ribaltare questo equilibrio, aprendo la cromatina virale e permettendo il riavvio del ciclo litico. Svelando questa lotta epigenetica, lo studio indica nuove strategie con cui gli scienziati potrebbero un giorno spingere i virus erpetici più saldamente in latenza innocua o, alternativamente, costringerli a emergere dal nascondiglio in condizioni controllate così da poterli eliminare.
Citazione: Xiang, Y., Yang, X., Zhang, J. et al. Counteracting FOX proteins epigenetically control the herpesvirus lytic-latent balance. Nat Commun 17, 2256 (2026). https://doi.org/10.1038/s41467-026-68915-1
Parole chiave: latenza del virus herpes simplex, fattori di trascrizione FOX, cromatina virale, regolazione epigenetica, riattivazione virale