Clear Sky Science · it
Espandere il potenziale di danneggiamento del DNA delle metallo-nucleasi artificiali con la chimica click
Costruire forbici molecolari più intelligenti
La chemioterapia agisce spesso danneggiando il DNA delle cellule tumorali, ma i farmaci odierni possono essere strumenti rozzi che colpiscono anche i tessuti sani. Questo studio esplora una nuova classe di “forbici molecolari” altamente programmabili, composte da rame e piccoli elementi organici assemblati con la chimica click. Modulando la loro forma e il modo in cui afferrano il DNA, i ricercatori mirano a creare agenti che taglino il materiale genetico con maggiore precisione, aprendo la strada a potenziali terapie antitumorali e antibatteriche future.
Assemblare un tagliente a tre braccia
Il gruppo usa la chimica click catalizzata dal rame, un metodo premiato con il Nobel noto per la sua affidabilità, per assemblare una famiglia di molecole chiamate ligandi Tri-Click (TC). Ogni molecola TC è un nucleo a tre braccia in grado di ospitare tre ioni rame contemporaneamente, formando un cluster compatto capace di attaccare il DNA. Sostituendo diversi gruppi “donatori” chimici all’estremità di ciascuna braccia—a base di azoto, ossigeno o zolfo—gli scienziati hanno testato sistematicamente come sottili cambiamenti strutturali influenzino il legame con il rame, il riconoscimento del DNA e l’attività biologica. Tra diversi nuovi progetti, le versioni con donatori azotati planari a forma di anello sono risultate particolarmente promettenti per afferrare saldamente il DNA.
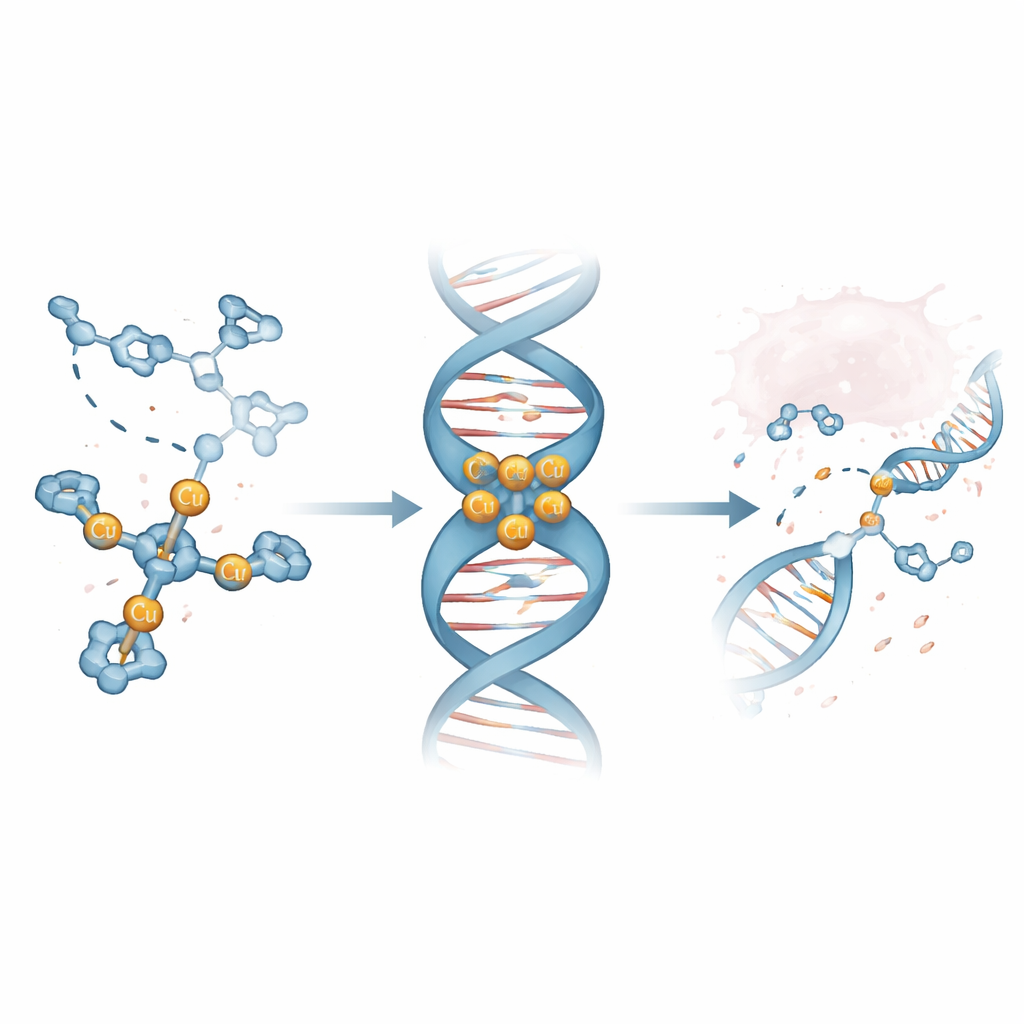
Trovare una molecola guida che ama le scanalature del DNA
Usando spettrometria di massa e metodi ottici, i ricercatori hanno mostrato che un complesso, chiamato Cu3-TC-Py, forma in modo affidabile un cluster a tre rame stabile in soluzione. Esperimenti di competizione con coloranti fluorescenti legati a DNA di timo bovino hanno rivelato che Cu3-TC-Py scaccia questi coloranti a concentrazioni molto basse, indicando un forte legame con il DNA. Test successivi su brevi frammenti di DNA a forcina hanno mostrato che questo complesso preferisce inserirsi nella scanalatura minore—la valle più stretta che avvolge la doppia elica del DNA—e che favorisce in particolare tratti ricchi di coppie di basi G e C. Simulazioni al computer ad alta risoluzione hanno supportato questo quadro, mostrando il complesso a tre braccia seduto nella scanalatura, con le cariche positive che avvolgono il DNA carico negativamente e compattano lievemente l’elica.
Dal forte legame al collasso e alla rottura del DNA
A livello di singola molecola, il team ha osservato lunghe catene di DNA confinate in canali nanometrici mentre interagivano con Cu3-TC-Py. A basse dosi, il complesso competeva con un colorante che allunga, scacciandolo quando si legava nelle scanalature. A dosi più elevate, il DNA ha iniziato a restringersi per poi condensarsi completamente, coerente con una forte attrazione elettrostatica tra il cluster di rame e lo scheletro del DNA. Quando il DNA plasmidico è stato esposto al complesso in presenza di un agente riducente, le catene sono passate dalla forma nativa avvolta a forme rilassate e poi completamente lineari, un andamento che segnala la formazione sia di rotture a singolo filamento sia a doppio filamento. Ulteriori test con scavenger di radicali hanno implicato specie ossigenate a vita breve—come superossido, ossigeno singoletto e radicali idrossilici—come i veri strumenti di taglio generati nelle vicinanze del complesso legato.
Attaccare il DNA in cellule tumorali e batteriche
Superando il DNA purificato, i ricercatori hanno esaminato il comportamento di Cu3-TC-Py all’interno di cellule viventi. In pannelli di cellule tumorali, i ligandi liberi contenenti gruppi aromatici ricchi di azoto hanno mostrato un’inibizione della crescita molto più marcata rispetto ai progetti precedenti, e il complesso di rame completamente formato è risultato ancora più potente, uccidendo diverse linee cellulari tumorali a concentrazioni micromolari. Misurazioni del rame intracellulare hanno rivelato che Cu3-TC-Py trasporta il rame in modo efficiente nelle cellule e provoca un accumulo di DNA danneggiato, rilevato con un metodo di imaging assistito dalla riparazione che marca le lesioni lungo filamenti genomici stirati. Nei batteri, la microscopia ha mostrato che il trattamento ha rapidamente distrutto la compattezza del cromosoma batterico, disperdendo il DNA in tutta la cellula e imitando la frammentazione severa osservata con un potente antibiotico che danneggia il DNA, coerente con una distruzione genetica diffusa.
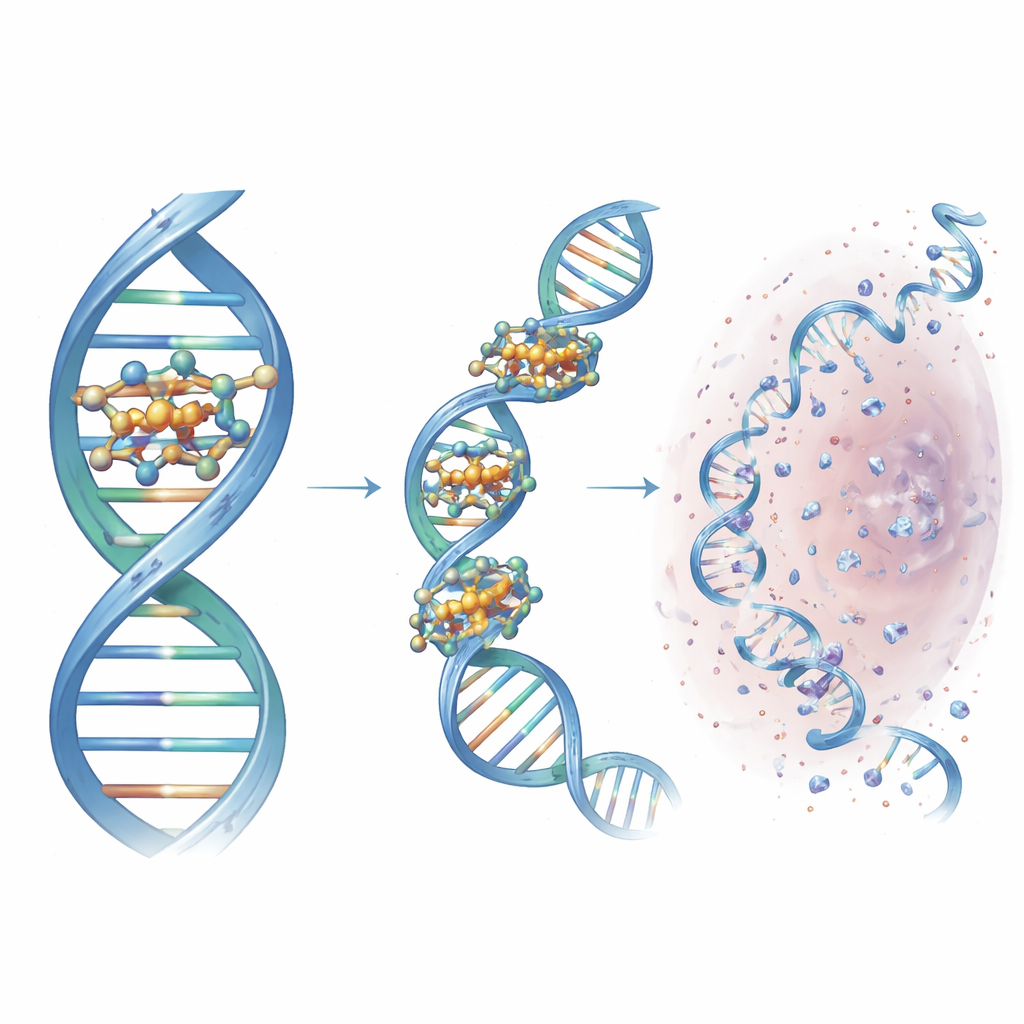
Perché queste forbici progettate sono importanti
Per un non specialista, il messaggio chiave è che i ricercatori hanno trasformato uno scaffold semplice e modulare basato sulla chimica click in una macchina di taglio del DNA finemente sintonizzata. Scegliendo i giusti gruppi azotati ad anello, hanno creato un cluster compatto di rame che si ancorato in una scanalatura specifica del DNA, avvicina i filamenti e genera localmente specie ossidanti reattive che sezionano la doppia elica. Questo composto guida, Cu3-TC-Py, danneggia il DNA in modo efficiente sia nelle cellule tumorali sia in quelle batteriche e mostra come il design razionale possa affinare l’azione di farmaci a base di metalli. Sebbene resti molto lavoro prima di un uso clinico, lo studio traccia regole di progetto per le forbici molecolari di nuova generazione che un giorno potrebbero offrire terapie antitumorali più mirate e nuove strategie antimicrobiche.
Citazione: Gibney, A., Sidarta, M., Delahunt, E. et al. Expanding the DNA damaging potential of artificial metallo-nucleases with click chemistry. Nat Commun 17, 2309 (2026). https://doi.org/10.1038/s41467-026-68911-5
Parole chiave: chimica click, danno al DNA, complessi di rame, agenti antitumorali, nucleasi artificiali