Clear Sky Science · it
Riadattamento evolutivo di un complesso tiolasi metabolico abilita la biosintesi di antibiotici
Come i microbi di tutti i giorni reinventano la loro chimica
Molti degli antibiotici e dei farmaci su cui facciamo affidamento sono silenziosamente prodotti dai batteri. Questi piccoli chimici impiegano enzimi—macchine molecolari—per costruire composti difensivi complessi. Questo studio rivela come un enzima centrale del metabolismo, un tempo utilizzato per le funzioni di base della cellula, sia stato riconvertito nel corso dell’evoluzione nei batteri orali per fabbricare un potente antibiotico. Capire questa trasformazione non solo mostra come la natura inventi nuova chimica, ma offre anche indizi per progettare farmaci di nuova generazione e biocatalizzatori.
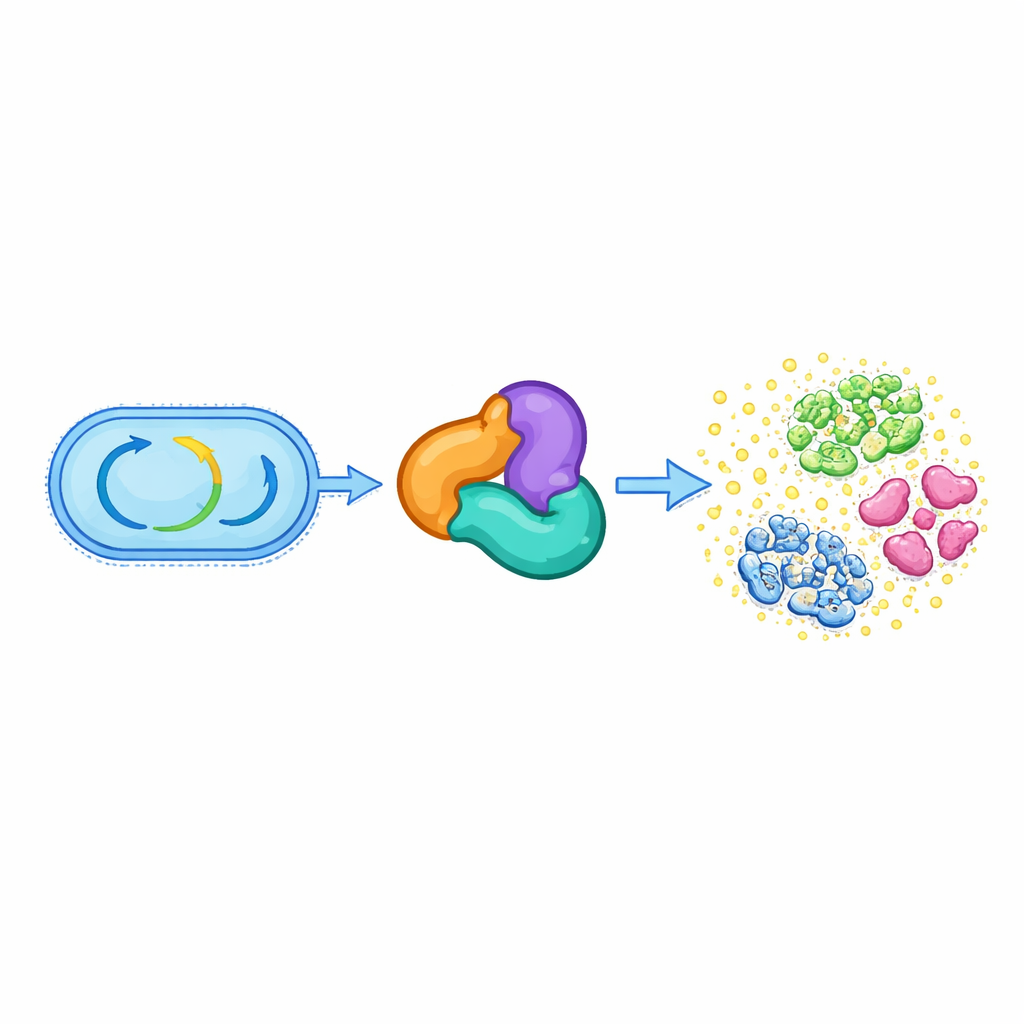
Dal metabolismo di base all’arsenale chimico
Tutte le cellule viventi dipendono da un insieme di enzimi conservati che gestiscono il loro metabolismo centrale, ad esempio degradando i grassi e costruendo molecole essenziali. Un gruppo di questi, chiamato superfamiglia delle tiolasi, normalmente aiuta a gestire piccoli metaboliti ricchi di energia come l’acetil‑CoA e sostiene vie vitali per la sintesi di lipidi e altri componenti cellulari. Gli autori hanno scoperto che in diverse specie orali di Streptococcus un complesso triassociato basato su tiolasi—composto da proteine correlate a HMGS, ACAT e una terza proteina ausiliaria—ha abbandonato il suo ruolo metabolico ancestrale. Invece, questo complesso completa ora la biosintesi di un antibiotico chiamato reutericyclin A, che aiuta questi batteri a competere nell’ambiente affollato della bocca.
Un nuovo tipo di reazione enzimatica su uno scaffold antibiotico
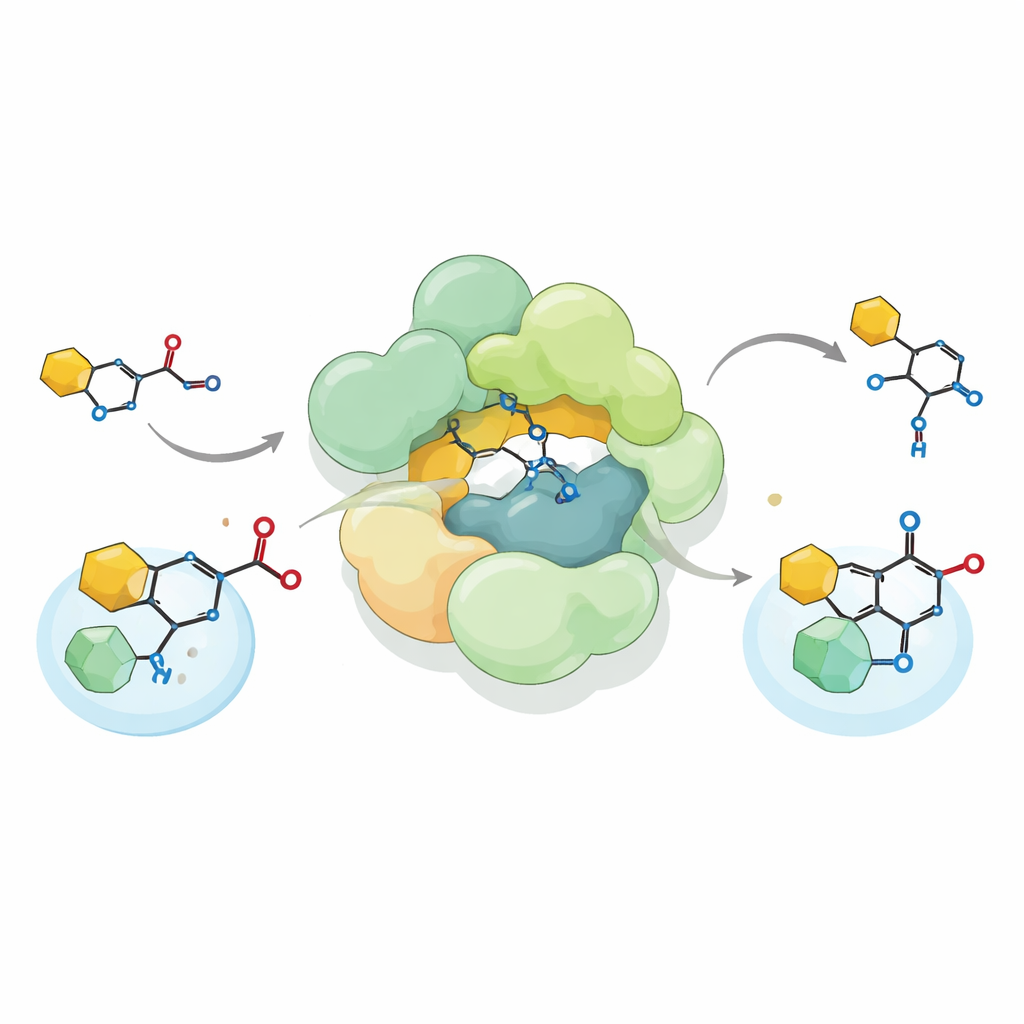
Ricostituendo in vitro il complesso di Streptococcus e alimentandolo con un precursore chimicamente sintetizzato della reutericyclin A, i ricercatori hanno dimostrato che il complesso esegue una insolita reazione di formazione di legami carbonio–carbonio nota come acilazione C di Friedel–Crafts. Piuttosto che legare un gruppo acetile all’ossigeno, come fanno molti enzimi, esso installa questo gruppo direttamente su un atomo di carbonio di un anello pirrolidina‑2,4‑dione—una parte importante dello scaffold della reutericyclin. Il complesso accetta sia donatori acetile naturali come l’acetil‑CoA sia diversi donatori artificiali, e può perfino operare la reazione in senso inverso, rompendo il legame che ha creato. Questa flessibilità amplia il repertorio noto degli aciltransferasi biologici e suggerisce come tali enzimi possano essere adattati per costruire prodotti chimici diversi.
Riadattare uno scaffold proteico conservato
Usando microscopia crio‑elettronica ad alta risoluzione, il team ha risolto la struttura tridimensionale del complesso di Streptococcus, denominato SmaATase. Nonostante la nuova funzione, SmaATase conserva una sorprendente somiglianza architettonica con un complesso correlato negli archei che partecipa alla via del mevalonato per la sintesi di lipidi isoprenoidi. Entrambi sono grandi assemblaggi multimersici costruiti da moduli ripetuti e presentano una cavità condivisa dove il cofattore CoA può legarsi e muoversi tra siti attivi. Tuttavia, residui catalitici chiave, essenziali per la reazione metabolica originale, sono assenti o alterati nella versione batterica. Test biochimici confermano che SmaATase non è più in grado di produrre il prodotto ancestrale HMG‑CoA e utilizza invece l’acetil‑CoA esclusivamente come donatore per i suoi nuovi substrati a piccola molecola.
Una traccia evolutiva dal metabolismo agli antibiotici
Per capire come si sia potuto svolgere un tale riadattamento, gli autori hanno confrontato sequenze e attività di complessi affini in numerosi batteri e archei. Hanno identificato oltre mille cluster genici contenenti lo stesso trio di tipi enzimatici. Alcuni supportano ancora la chimica classica delle tiolasi; altri, come quelli in Pseudomonas, alimentano diversi piccoli antibiotici. Un complesso rappresentativo di Pseudomonas fluorescens sembra trovarsi a metà di questo percorso evolutivo: il suo dominio di tipo HMGS è disattivato, ma la sua unità simile ad ACAT svolge ancora una reazione più convenzionale su substrati legati a CoA. In SmaATase e nel corrispondente di Pseudomonas che produce il composto protettivo per le colture DAPG, ulteriori modifiche intorno al sito attivo hanno adattato gli enzimi a riconoscere accettori non standard come anelli aromatici o core di tetramico acido.
Perché un piccolo gruppo acetile fa la differenza
In definitiva, il vantaggio biologico di questo maquillage molecolare è evidente. Quando il team ha testato gli antibiotici acetilati reutericyclin A e DAPG su un pannello di batteri Gram‑positivi, queste molecole hanno mostrato una forte attività battericida, mentre i loro precursori non acetilati erano molto più deboli o quasi inattivi. Quel piccolo gruppo acetile, collocato nella posizione giusta dal complesso enzimatico riadattato, trasforma uno scaffold modesto in un’arma potente, permettendo a Streptococcus nella bocca o a Pseudomonas intorno alle radici delle piante di soppiantare i vicini. Questo lavoro mette in mostra come l’evoluzione possa riciclare strutture enzimatiche esistenti con mutazioni minime ma strategiche, trasformando macchinari metabolici di routine in strumenti specializzati per la difesa chimica—e offrendo un modello per gli ingegneri che vogliano progettare nuovi catalizzatori di formazione di legami carbonio–carbonio per la scoperta di farmaci e la biologia sintetica.
Citazione: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
Parole chiave: evoluzione degli enzimi, biosintesi di prodotti naturali, chimica degli antibiotici, riutilizzo metabolico, alchilazione di Friedel–Crafts