Clear Sky Science · it
Modellazione della fibrosi polmonare basata su iPSC umane rivela che l'inibizione di p300/CBP sopprime lo stato cellulare transizionale alveolare
Perché i polmoni cicatrizzati ci riguardano tutti
La fibrosi polmonare idiopatica (IPF) è una malattia inesorabile in cui i polmoni si trasformano lentamente in tessuto cicatriziale, rendendo ogni respiro più difficile. I farmaci attuali possono solo rallentare questo processo e spesso causano effetti collaterali problematici. Questo studio utilizza strumenti all'avanguardia di biologia delle cellule staminali e genomica per ricreare in laboratorio polmoni cicatrizzati, ponendo una domanda semplice ma vitale: possiamo trovare un interruttore che indirizzi le cellule polmonari danneggiate lontano da uno stato dannoso e di nuovo verso la guarigione?
Una finestra coltivata in laboratorio su un polmone cicatrizzato
Per studiare l'IPF, i ricercatori hanno costruito mini polmoni a partire da cellule staminali pluripotenti indotte umane (iPSC). Queste iPSC sono state indirizzate a diventare cellule alveolari—le cellule che rivestono le piccole sacche d'aria dove l'ossigeno entra nel sangue—and sono state coltivate insieme a fibroblasti polmonari, le cellule del tessuto connettivo che formano la cicatrice. Incorporati in un gel morbido, questi “organoidi alveolari” si comportavano in modo molto simile al tessuto polmonare reale. Quando esposti al farmaco chemioterapico bleomicina, un noto fattore scatenante di danno polmonare, i gel si accorciavano mentre i fibroblasti li tiravano, imitando la contrazione tissutale osservata nella fibrosi.
Usando questo sistema, il team ha testato una libreria di 264 piccole molecole e ha misurato automaticamente quanto ciascun farmaco impedisse la contrazione del gel, con uno strumento di analisi delle immagini basato su deep learning per garantire misurazioni oggettive. Molti composti non avevano effetto, ma una famiglia ha chiaramente emergendo: gli inibitori delle proteine p300 e CBP, che aiutano a controllare come il DNA è impacchettato e quali geni vengono attivati. Tutti e otto i composti mirati a p300/CBP nella libreria hanno ridotto la contrazione a basse dosi, evidenziando questa via come una leva promettente contro la fibrosi. 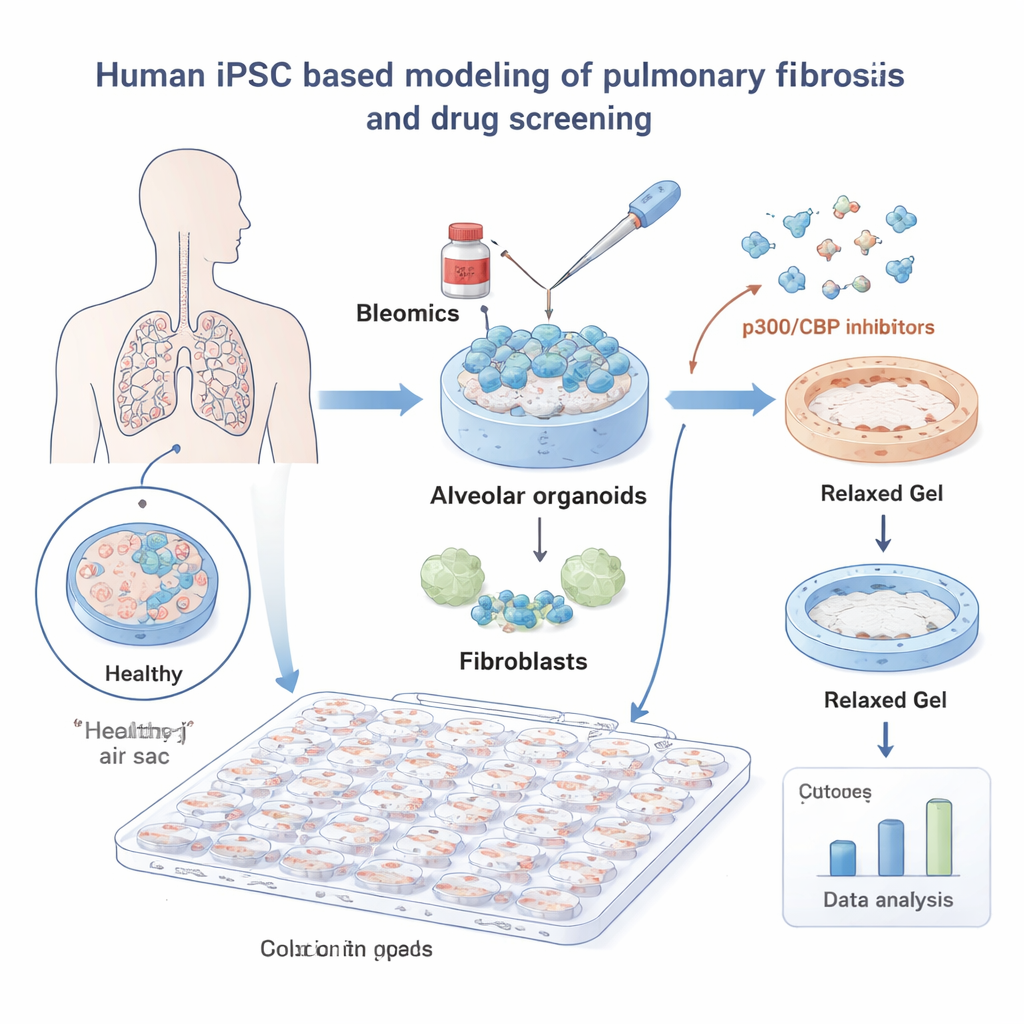
I colpevoli: le cellule polmonari transizionali
Lavori recenti hanno rivelato un tipo cellulare “intermedio” problematico nei polmoni malati, chiamato stato cellulare transizionale alveolare. Normalmente, cellule di supporto note come AT2 maturano in cellule AT1 ultra‑sottili che rivestono le sacche d'aria e permettono lo scambio gassoso. Nell'IPF, tuttavia, le cellule AT2 spesso si bloccano in questo stato transizionale, esprimendo geni di stress e riparazione senza completare il percorso verso AT1 pienamente funzionali. Queste cellule transizionali si raggruppano nelle regioni fibrotiche e comunicano fortemente con i fibroblasti, ma non era chiaro se fossero semplicemente un sottoprodotto del danno o attori attivi nella formazione della cicatrice.
Sequenziando l'RNA e profilando la cromatina aperta nei loro organoidi, gli autori hanno mostrato che le cellule transizionali che emergevano nel loro modello corrispondevano strettamente a quelle trovate nei polmoni di pazienti con IPF. Queste cellule transizionali indotte esibivano firme geniche di stress, infiammazione e rimodellamento della matrice, e attivavano fortemente i fibroblasti polmonari adulti co‑coltivati. Fondamentalmente, quando p300/CBP veniva bloccato, i marcatori dello stato transizionale diminuivano, l'identità AT2 era meglio preservata e l'attivazione dei fibroblasti si attenuava. In altre parole, i farmaci non avvelenavano le cellule in modo generico; piuttosto, impedivano selettivamente alle cellule AT2 di restare intrappolate in questo limbo dannoso.
Sciogliere gli interruttori molecolari
Per capire come p300/CBP orienti questa decisione di destino, il team ha esaminato marche chimiche sugli istoni—proteine che aiutano a impacchettare il DNA. Un marchio particolare, l'acetilazione di H3K27, è comunemente posto da p300/CBP sugli enhancer e promotori attivi. Nelle cellule transizionali, regioni vicine a geni di risposta allo stress e pro‑fibrotici mostravano forte acetilazione di H3K27 ed erano arricchite per siti di legame di fattori di trascrizione come AP‑1 e HNF1B. Quando le cellule venivano trattate con inibitori di p300/CBP, queste marche di acetilazione diminui‑ vano in quei siti e l'espressione di molti geni pro‑fibrotici calava. Bloccare direttamente AP‑1, o ridurre AP‑1 e HNF1B con piccoli RNA interferenti, riduceva allo stesso modo il programma transizionale e la contrazione degli organoidi, collegando questo trio—p300/CBP, AP‑1 e HNF1B—all'ingranaggio che alimenta il rimodellamento fibrotico.
Oltre alla coltura, lo studio ha testato un inibitore, CBP30, in topi con danno polmonare indotto da bleomicina. Gli animali trattati con CBP30 avevano meno cellule epiteliali transizionali, minore attivazione dei miofibroblasti formatori di cicatrice e ridotta espressione di marcatori di fibrosi. Questa convalida incrociata tra modelli umani basati su cellule staminali e un modello animale rafforza l'idea che p300/CBP non sia solo un artefatto di laboratorio ma un regolatore genuino della cicatrizzazione polmonare. 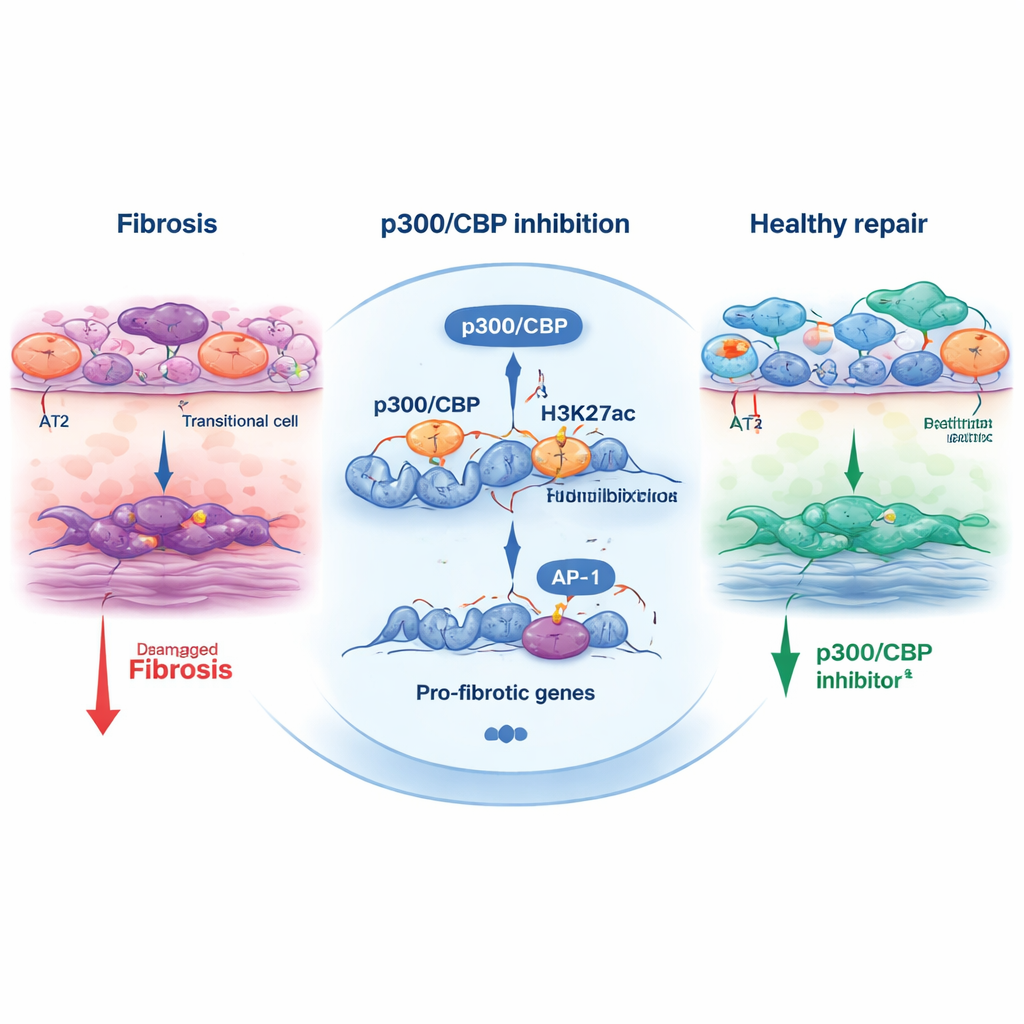
Cosa significa per i trattamenti futuri
Per i non specialisti, il messaggio chiave è che gli autori hanno costruito un modello umano realistico di polmoni fibrotici e lo hanno usato per mettere in luce un nuovo bersaglio farmacologico. Il loro lavoro suggerisce che la cicatrizzazione polmonare è guidata in parte da uno stato cellulare transizionale indotto dallo stress e reversibile che fuorvia il tessuto circostante. Riducendo l'attività di p300/CBP, potrebbe essere possibile quietare questo stato, mantenere le cellule alveolari su un percorso di sviluppo sano e ridurre i segnali che spingono i fibroblasti a iperattivarsi. Sebbene gli inibitori di p300/CBP debbano ancora essere ottimizzati in termini di sicurezza e testati clinicamente, questo studio indica la strada verso terapie che affrontano la discomunicazione cellulare alla radice nell'IPF invece di limitarsi a rallentare le sue conseguenze.
Citazione: Tsutsui, Y., Masui, A., Konishi, S. et al. Human iPSC-based Modeling of Pulmonary Fibrosis Reveals p300/CBP Inhibition Suppresses Alveolar Transitional Cell State. Nat Commun 17, 1214 (2026). https://doi.org/10.1038/s41467-026-68909-z
Parole chiave: fibrosi polmonare idiopatica, organoidi alveolari, inibitori di p300/CBP, cellule epiteliali transizionali, cellule staminali polmonari