Clear Sky Science · it
Progettare plasmidi con origini di replicazione sintetiche
Perché riscrivere il DNA microbico è importante
Molti degli strumenti alla base della biotecnologia moderna, dalla produzione di insulina ai circuiti genetici d’avanguardia, si affidano a piccoli anelli di DNA chiamati plasmidi. Questi cavalli di battaglia genetici trasportano geni ingegnerizzati nei batteri, ma il loro progetto di base è cambiato pochissimo in decenni. Questo studio mostra che il cuore stesso dei plasmidi — le sequenze che dicono alle cellule quando e quante volte copiarli — può essere completamente ripensato. Ricostruendo da zero questo “motore di copia”, gli autori creano plasmidi più facili da regolare, combinare e programmare, aprendo la strada a diagnostica più flessibile, bioproduzione e biologia sintetica.
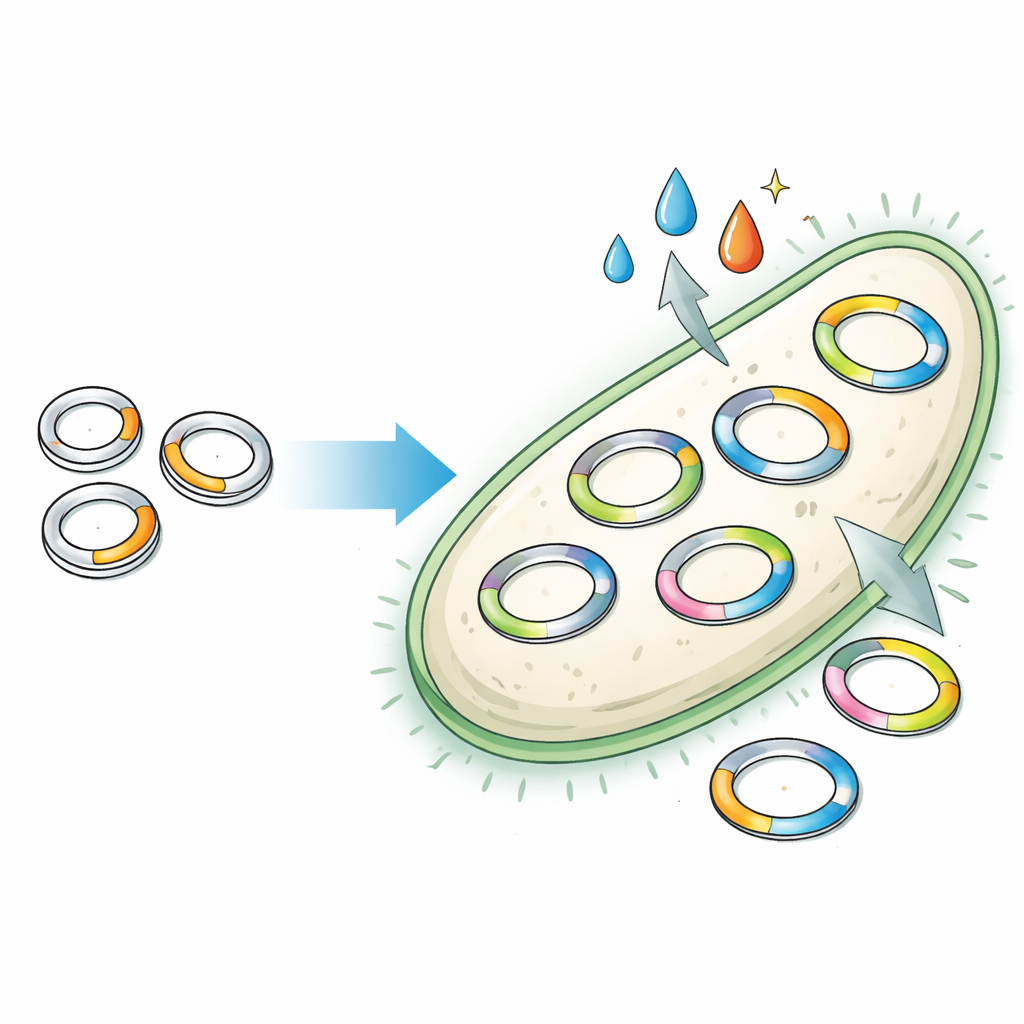
Strumenti vecchi con limiti nascosti
I plasmidi si sono evoluti naturalmente come DNA mobile, aiutando i batteri a condividere tratti come la resistenza agli antibiotici o nuovi modi per digerire fonti di cibo. In laboratorio, gli ingegneri sfruttano questi plasmidi per portare geni utili, ma la maggior parte si basa su pochi progetti classici scoperti negli anni ’80. Quei progetti nascondono una matassa di parti genetiche sovrapposte che controllano quante copie di un plasmide si trovano in ogni cellula e se plasmidi diversi possono coesistere pacificamente. Poiché queste parti sono fuse insieme, cambiare una caratteristica può rompere in modo imprevedibile un’altra. Di conseguenza, gli scienziati si trovano con un menu ridotto di plasmidi con numeri di copie fissi e compatibilità limitata, il che restringe la complessità dei sistemi ingegnerizzati.
Ricostruire il motore di copia da zero
I ricercatori si sono concentrati su un’origine di replicazione ampiamente usata della famiglia di plasmidi pMB1. Nella sua forma naturale, questa origine usa una conversazione finemente bilanciata tra due RNA — uno che avvia la copia del DNA e un altro che la spegne — per mantenere sotto controllo il numero di plasmidi. Il team ha prima “rifattorizzato” questo sistema: ha separato geni sovrapposti, inattivato un promotore sepolto e collocato i pezzi chiave su cassette genetiche separate e pulite. Questo ha mostrato che la funzione fondamentale dell’origine poteva essere preservata semplificandone la disposizione, trasformando una parte modellata dall’evoluzione in qualcosa di più simile a una macchina modulare con componenti accessibili.
Sostituire con manopole di controllo sintetiche
Con la logica di controllo originale esposta, gli autori l’hanno poi rimpiazzata con regolatori completamente sintetici. Hanno collegato il primer di replicazione a interruttori RNA ingegnerizzati che funzionano come dimmer: piccoli RNA regolatori possono commutare questi interruttori per permettere o bloccare la produzione del primer e, di conseguenza, la copia del plasmide. Scegliendo varianti diverse degli interruttori e abbinandole a promotori di diversa intensità, hanno regolato il numero di copie dei plasmidi su più di due ordini di grandezza. Hanno anche esplorato differenti disposizioni fisiche delle cassette di controllo sul DNA, scoprendo configurazioni che miglioravano la stabilità e permettevano di ridurre la regione di replicazione a un nucleo compatto e funzionale, aggiungendo al contempo sistemi ausiliari naturali che prevengono intrecci problematici tra plasmidi.
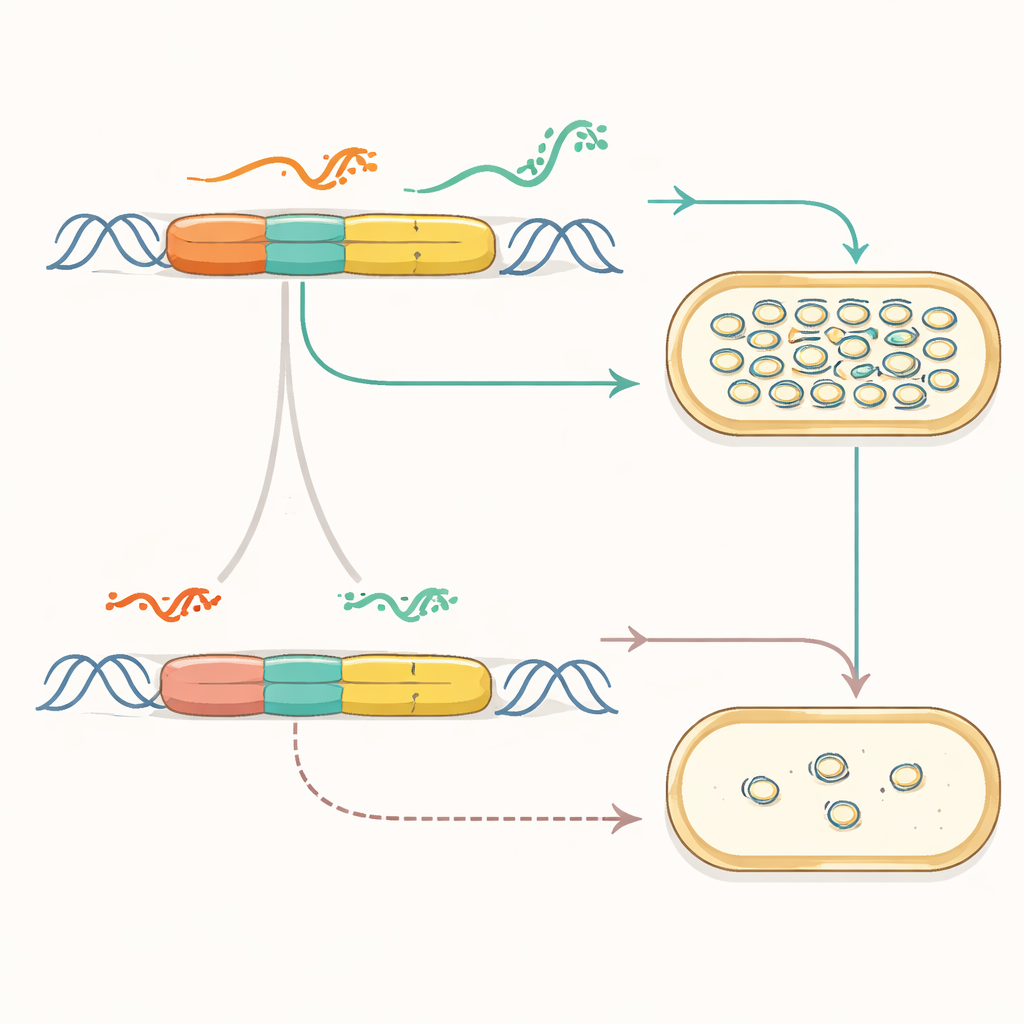
Trasformare segnali chimici in conteggi di DNA
Una volta che il motore di copia è diventato modulare, il team ha dimostrato che poteva essere collegato per sensibilizzare al mondo esterno. Hanno connesso l’origine sintetica a promotori inducibili e a strutture di RNA chiamate riboswitch, che cambiano forma in risposta a piccole molecole. In questi nuovi plasmidi, l’aggiunta di una sostanza chimica come IPTG o cumato faceva salire o scendere il numero di copie del plasmide — e quindi il segnale di un reporter. Più segnali potevano essere combinati in modo che una molecola stimolasse la copia mentre un’altra la frenava. I ricercatori hanno persino costruito coppie di plasmidi, ciascuno rispondente a una diversa sostanza chimica, e hanno monitorato i cambiamenti del numero di copie nello stesso batterio mediante sequenziamento del DNA, trasformando efficacemente i conteggi dei plasmidi in un codice a barre della storia ambientale.
Molti plasmidi personalizzati in una singola cellula
Un test chiave di questo approccio era verificare se diversi plasmidi controllati in modo indipendente potessero coesistere. Attingendo a una libreria di regolatori RNA ortogonali, il team ha costruito sei plasmidi diversi, ciascuno con la propria origine sintetica e marcatore per antibiotico, e ha introdotto tutti e sei contemporaneamente in E. coli. Il sequenziamento di interi plasmidi nel corso di diversi giorni ha confermato che tutti e sei rimanevano presenti, sebbene le loro abbondanze relative siano cambiate. I tentativi di fare lo stesso con sei plasmidi convenzionali sono falliti, sottolineando come il design rifattorizzato e i sistemi di stabilità aggiunti rendano i nuovi plasmidi più compatibili e robusti quando affollati nella stessa cellula.
Cosa significa per la biotecnologia futura
Per chi non è specialista, la conclusione è semplice: gli autori hanno trasformato i plasmidi da strumenti rigidi e universali in una piattaforma personalizzabile. Le loro origini di replicazione sintetiche funzionano come motori plug-and-play la cui velocità, sensibilità e ingressi possono essere scelti su richiesta. Questo rende possibile costruire batteri che registrano esposizioni chimiche come cambiamenti nel numero di copie del DNA, testare molti percorsi genetici in parallelo distribuendoli su più plasmidi o bilanciare con precisione crescita e produzione in ceppi industriali. Pur restando alcuni compromessi di stabilità, questo lavoro dimostra che la meccanica fondamentale della replicazione dei plasmidi non è più off-limits per l’ingegneria, aprendo nuovo spazio per l’innovazione nella biologia sintetica.
Citazione: Liu, B., Seet, Z.R.D., Peng, X. et al. Engineering plasmids with synthetic origins of replication. Nat Commun 17, 2255 (2026). https://doi.org/10.1038/s41467-026-68907-1
Parole chiave: plasmidi sintetici, origine di replicazione, regolatori a RNA, controllo del numero di copie, biologia sintetica