Clear Sky Science · it
Il recettore del succinato 1 limita l’ematopoiesi e previene la progressione della leucemia mieloide acuta
Quando il carburante cellulare va fuori controllo
Il nostro sangue viene rinnovato continuamente da una piccola popolazione di cellule staminali nascoste nel midollo osseo. Questo studio indaga come un comune prodotto metabolico di scarto, il succinato, e il suo sensore sulla superficie cellulare agiscano come un freno su questo sistema di rinnovo. Quando quel freno viene meno, l’equilibrio tra produzione ematica sana e crescita cancerosa può inclinarsi verso la leucemia mieloide acuta (LMA), un tumore ematologico aggressivo. Comprendere questo interruttore di controllo nascosto potrebbe portare a trattamenti più mirati che domano la malattia ripristinando le difese intrinseche dell’organismo.
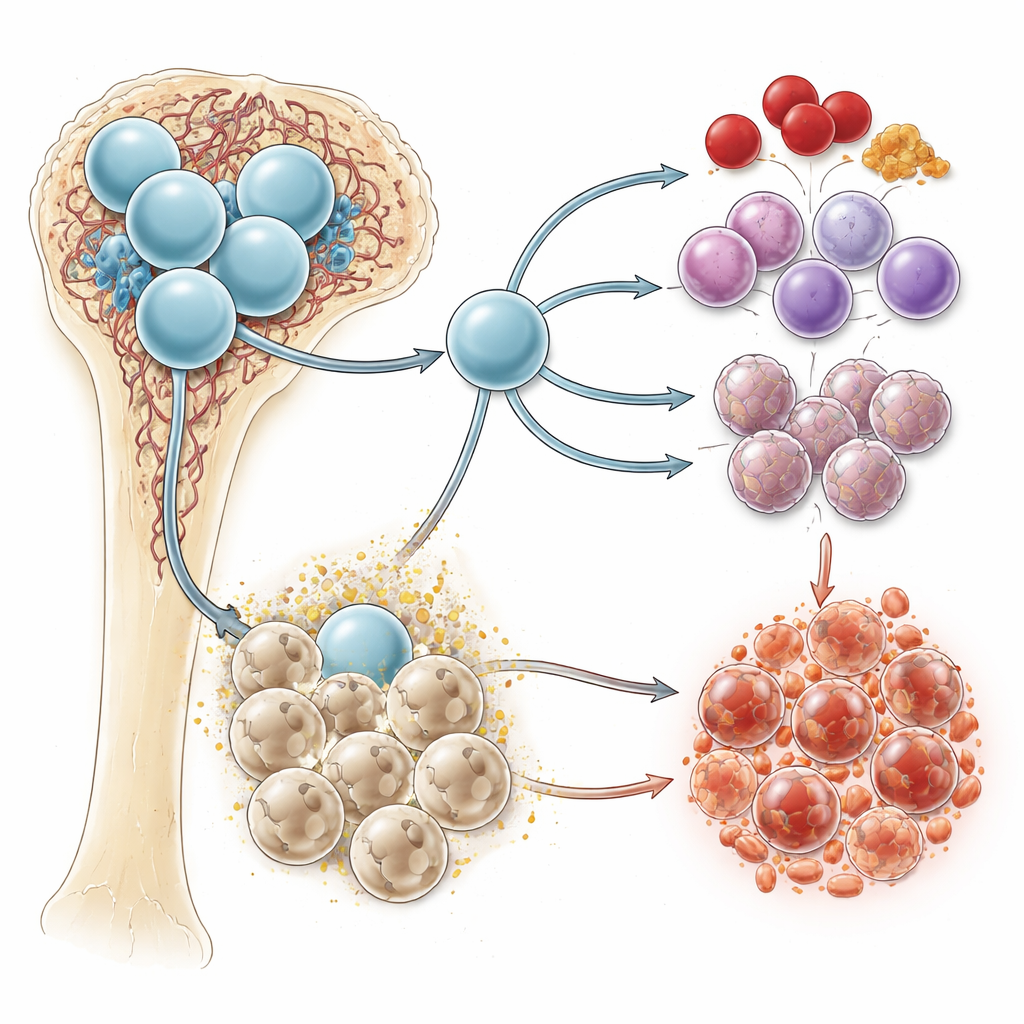
Un segnale chimico con una doppia vita
Il succinato è un prodotto di routine del modo in cui le cellule bruciano carburante, in particolare all’interno dei mitocondri, le centrali energetiche della cellula. In condizioni di bassa ossigenazione — come quelle del midollo osseo — il succinato tende ad accumularsi. Può agire all’interno delle cellule, modificando metabolismo e risposte infiammatorie, ma può anche uscire dalle cellule e fungere da segnale extracellulare. Sulla superficie cellulare, un recettore chiamato SUCNR1 rileva il succinato e trasmette la sua presenza all’interno. Studi precedenti avevano collegato succinato e SUCNR1 all’infiammazione e a microambienti favorevoli al cancro, ma il loro ruolo diretto nella formazione del sangue e nella leucemia era rimasto poco chiaro.
Un segnale d’allarme nei pazienti leucemici
I ricercatori hanno analizzato dati di espressione genica di centinaia di pazienti con LMA e hanno scoperto che i livelli di SUCNR1 variano molto tra gli individui. I pazienti le cui cellule leucemiche esprimevano livelli bassi di SUCNR1 avevano una sopravvivenza complessiva e una sopravvivenza senza progressione più brevi, anche tenendo conto di età, sesso e sottotipi clinici standard. Alcuni sottogruppi genetici di LMA tendevano a mostrare livelli particolarmente bassi di SUCNR1. Quando il team ha trapiantato cellule leucemiche umane prive di SUCNR1 in topi immunodeficienti e ha poi iniettato negli animali acido succinico (che nell’organismo diventa succinato), il carico leucemico nel midollo osseo è aumentato. Ciò suggerisce che, in tumori con basso SUCNR1, un eccesso di succinato può effettivamente alimentare la progressione della malattia anziché frenarla.
Il freno nascosto sulle cellule staminali ematiche
Per capire come SUCNR1 agisca nella formazione del sangue normale, gli scienziati si sono rivolti a topi geneticamente modificati. Quando SUCNR1 è stato eliminato nell’animale intero o solo nelle cellule ematopoietiche, il midollo osseo è diventato iperattivo. Le cellule staminali e progenitrici si sono espanse e sia le cellule mieloidi (come monociti e granulociti) sia le cellule B sono aumentate nel sangue e nella milza. Queste cellule di tipo staminale sopravvivevano meglio e formavano più colonie in coltura, sebbene fossero leggermente meno capaci di ristabilire la produzione ematica quando trapiantate in competizione con cellule normali. Una linea murina reporter speciale ha mostrato che solo un sottogruppo di cellule staminali e progenitrici esprime effettivamente SUCNR1; queste cellule SUCNR1-positive avevano un potenziale di engraftment particolarmente limitato. Nel complesso, il recettore agiva come una restrizione sulla dimensione e sull’attività del pool di cellule staminali.
Da una difesa bilanciata a un sovraccarico infiammatorio
Un profilo dettagliato dell’espressione genica nelle cellule staminali e progenitrici prive di SUCNR1 ha rivelato uno spostamento netto. Le firme tipiche delle cellule staminali primitive e quiescenti erano attenuate, mentre i geni legati all’infiammazione, alle specie reattive dell’ossigeno e alle cellule ematiche mature erano potenziati. Due molecole hanno spiccato: S100A8 e S100A9, una coppia di “alarmini” che amplificano la segnalazione infiammatoria. Questi fattori risultavano aumentati sia nel compartimento delle cellule staminali sia nel fluido circostante del midollo osseo. Quando il team ha trattato i topi privi di SUCNR1 con tasquinimod, un farmaco che blocca la segnalazione di S100A9, l’espansione eccessiva di cellule staminali e progenitrici, così come la sovrapproduzione di cellule mieloidi e B, è stata in gran parte invertita. In altre parole, gran parte del danno dovuto alla perdita di SUCNR1 poteva essere annullato interrompendo il circuito d’allarme S100A8/S100A9.
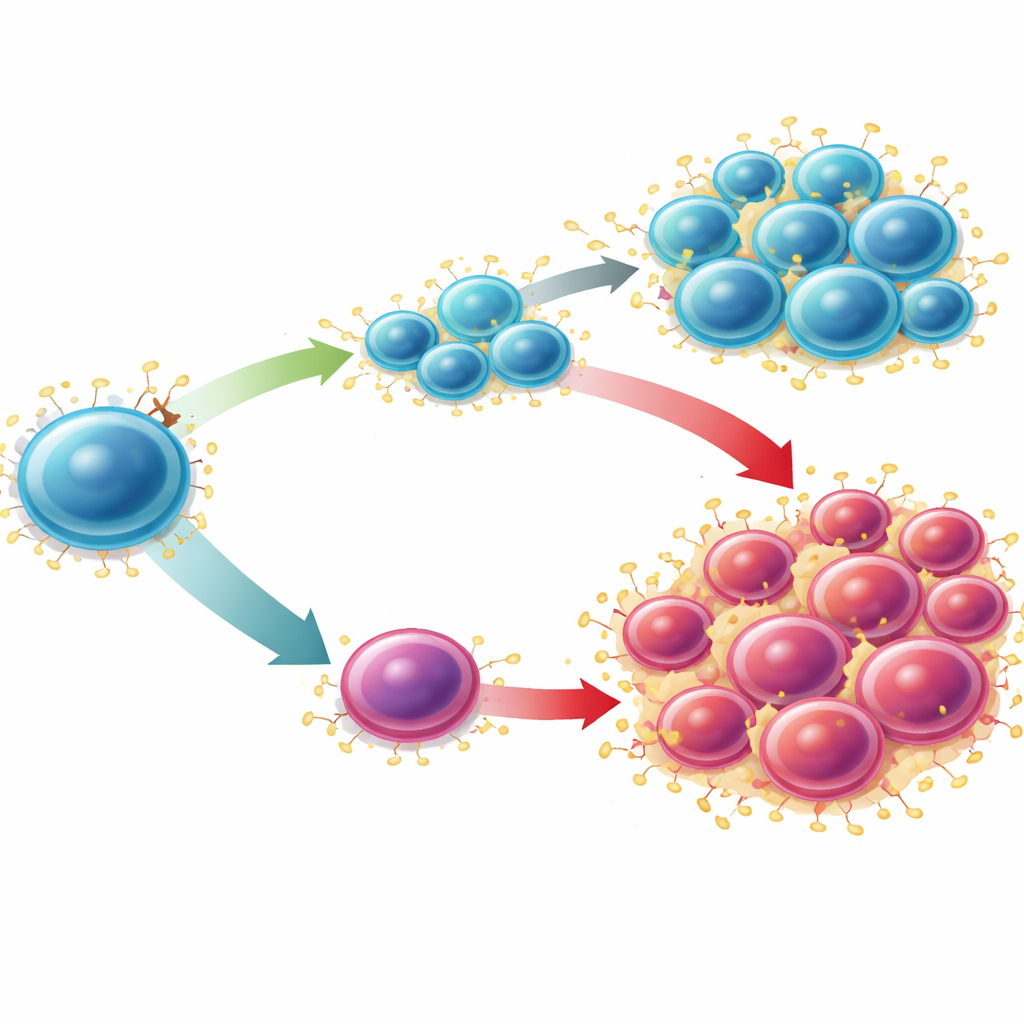
Trasformare una vulnerabilità in una strategia terapeutica
Gli scienziati hanno quindi valutato se questa via potesse essere sfruttata terapeuticamente nella LMA. In una leucemia murina aggressiva guidata dalla mutazione MLL-AF9 — dove i livelli di Sucnr1 sono molto bassi — bloccare S100A9 con tasquinimod, specialmente se combinato con un potente composto attivante SUCNR1, ha ridotto le cellule simili a staminali leucemiche e diminuito il carico di malattia in midollo osseo e milza. Analisi di dati di RNA a singola cellula da modelli umani di LMA trattati con il chemioterapico citarabina hanno mostrato che i cluster cellulari resistenti erano ricchi di S100A8 e S100A9, mentre SUCNR1 era scarso e associato a un sottogruppo metabolicamente attivo che si riduceva dopo il trattamento. In linee cellulari di leucemia umana, l’attivazione di SUCNR1 aumentava la morte cellulare indotta dalla chemioterapia e poteva innescare apoptosi da sola quando SUCNR1 veniva sovraespresso. Nel loro insieme, questi risultati collocano il basso SUCNR1 non solo come un marcatore di prognosi sfavorevole ma anche come una vulnerabilità: le cellule leucemiche che hanno perso questo freno possono dipendere fortemente dall’asse S100A8/S100A9 e risultare particolarmente sensibili a strategie che riattivano la segnalazione SUCNR1 o bloccano l’allarme a valle.
Una nuova leva per domare la leucemia
Per il lettore non specialistico, il messaggio centrale è che un prodotto metabolico apparentemente banale, il succinato, e il suo recettore SUCNR1 costituiscono un inaspettato sistema di sicurezza nella formazione del sangue. Quando SUCNR1 è presente e attivo, mantiene sotto controllo le cellule staminali e previene una crescita incontrollata. Quando SUCNR1 viene perso o è a livelli bassi — comune in alcuni pazienti con LMA — il succinato e gli alarmini infiammatori come S100A8 e S100A9 possono spingere cellule staminali e progenitrici verso un’eccessiva espansione e la leucemia. Combinando farmaci che attenuano questo allarme infiammatorio con agenti che ripristinano o mimano la segnalazione di SUCNR1, potrebbe essere possibile riportare il sistema a una produzione ematica bilanciata e migliorare l’efficacia delle chemioterapie esistenti.
Citazione: Cuminetti, V., Boet, E., Heugel, M. et al. Succinate receptor 1 restricts hematopoiesis and prevents acute myeloid leukemia progression. Nat Commun 17, 2403 (2026). https://doi.org/10.1038/s41467-026-68906-2
Parole chiave: leucemia mieloide acuta, recettore del succinato, cellule staminali ematopoietiche, metabolismo e cancro, segnalazione infiammatoria