Clear Sky Science · it
Ossidasi degli alcoli ingegnerizzate catalizzano la transesterificazione in mezzo acquoso senza idrolisi concorrente
Perché questa storia enzimatica è importante
Molti prodotti di uso quotidiano, dai farmaci e gli aromi alimentari al biodiesel, dipendono da un semplice tipo di legame chimico chiamato estere. Produrre e modificare questi esteri in modo efficiente, economico e rispettoso dell’ambiente è un obiettivo centrale della chimica verde. Il problema è che l’acqua, il solvente ideale dal punto di vista della sicurezza e della sostenibilità, di solito sabota queste reazioni degradando gli esteri appena formati. Questo studio svela un enzima ingegnerizzato che riesce a costruire esteri in acqua ignorando quasi del tutto l’acqua circostante, aprendo la strada a processi industriali più puliti.
Riprogrammare un enzima noto per un nuovo compito
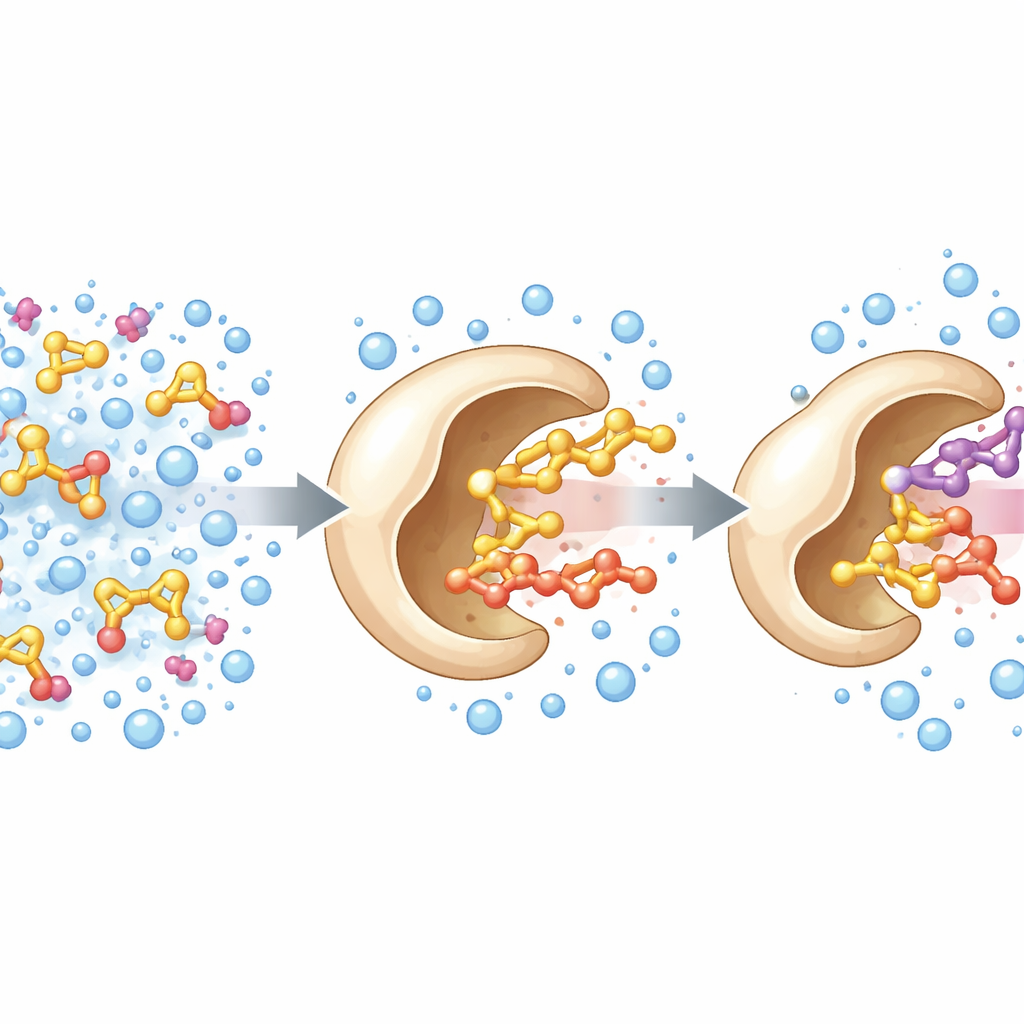
I ricercatori sono partiti da un enzima noto, un’alcool ossidasi proveniente da un fungo degradatore del legno. In natura questo enzima utilizza un cofattore flavinico per rimuovere elettroni da alcoli piccoli come il metanolo. Il gruppo ha cercato di ampliarne la portata in modo che potesse trattare alcoli più ingombranti, più rilevanti per chimica fine e aromi. Usando la struttura tridimensionale dell’enzima come mappa, si sono concentrati su tre amminoacidi che formano una sorta di porta d’ingresso nel sito attivo. Randomizzando queste posizioni e selezionando le varianti risultanti, hanno individuato un triplo mutante — chiamato PcAOx‑VPN — in grado di processare efficacemente alcoli più grandi come l’alcol benzilico, perdendo al contempo gran parte della sua attività originale verso quelli molto piccoli come il metanolo.
Talento inaspettato: costruire esteri in acqua
Durante i test di PcAOx‑VPN in miscele pensate per sciogliere substrati oleosi, il team ha notato picchi extra nelle analisi. Si sono rivelati prodotti acetilati: l’enzima stava trasferendo un gruppo acile da un donatore di estere attivato agli alcoli, una reazione nota come transesterificazione. Notevolmente, questo avveniva in tampone acquoso, condizione che normalmente favorisce una forte idrolisi concorrente, in cui l’acqua attacca e distrugge l’estere. Qui, PcAOx‑VPN univa efficacemente alcoli e donatori di acile come l’acetato di vinile per formare nuovi esteri, spesso con rese superiori all’80% e con effetti collaterali modesti. Lo stesso enzima poteva agire su una vasta gamma di alcoli, compresi quelli a catena retta, aromatici, chirali e contenenti zolfo, mostrando in diversi casi una marcata preferenza per una delle forme speculari.
Tenere l’acqua fuori dal gioco
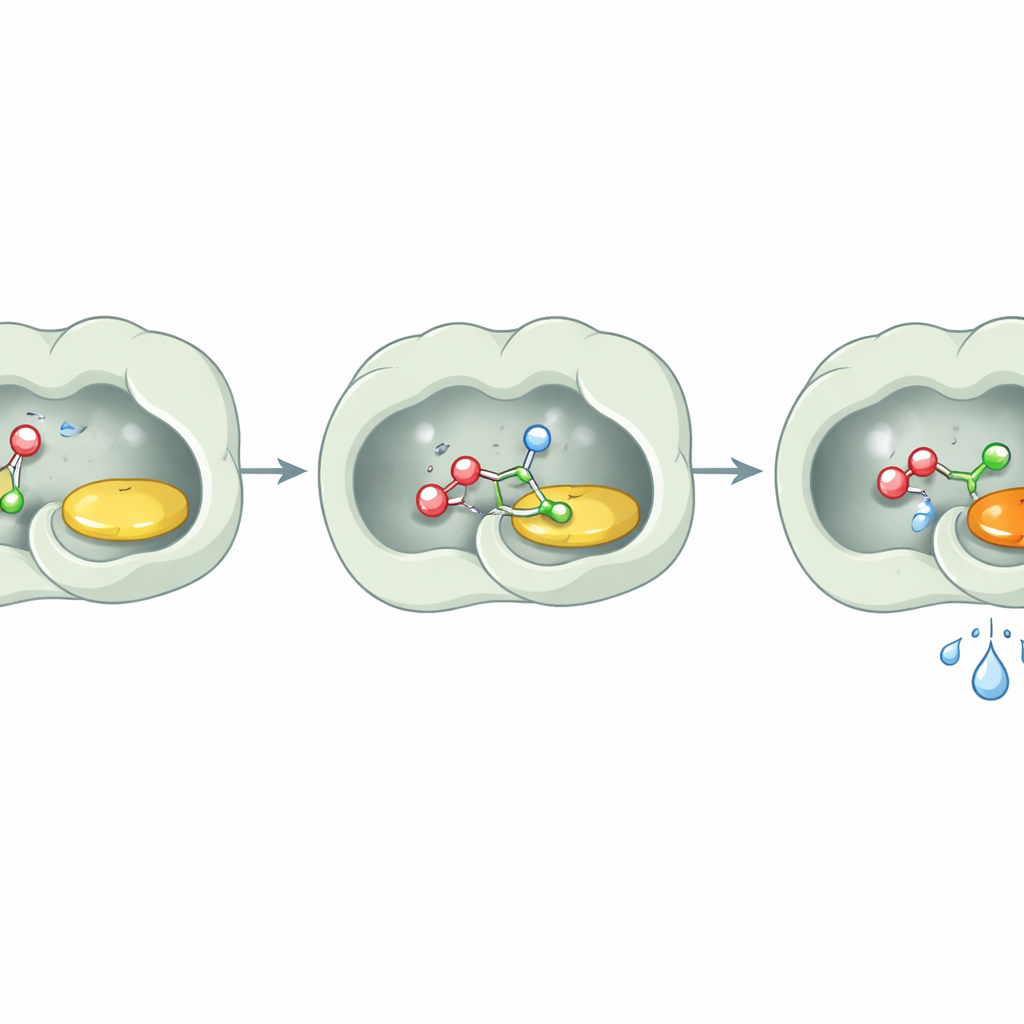
Una sorpresa chiave è stata ciò che l’enzima non faceva: non idrolizzava gli esteri in modo apprezzabile. Anche dopo lunghe incubazioni con substrati estere e acqua, PcAOx‑VPN li lasciava praticamente intatti a meno che non fosse fornito un ulteriore donatore di acile. Gli studi strutturali forniscono una spiegazione semplice. Il sito attivo è rivestito da amminoacidi per lo più oleosi e aromatici che creano una tasca altamente idrofobica. L’analisi dettagliata non ha mostrato molecole d’acqua vicine al cofattore flavinico, e strumenti computazionali hanno confermato che il canale d’ingresso al sito attivo è poco ospitale per l’acqua. In pratica, l’enzima crea una piccola stanza asciutta dentro un mondo acquoso. Alcoli e esteri attivati possono entrare e reagire, ma le molecole d’acqua vengono tenute a distanza e non hanno la possibilità di distruggere il prodotto.
Come funziona probabilmente la reazione all’interno
Esperimenti meccanicistici e analisi mutazionale hanno rivelato che due amminoacidi, un istidina e un asparagina, sono centrali sia per il ruolo ossidativo naturale dell’enzima sia per il nuovo talento nella transesterificazione. L’istidina agisce come base, aiutando a rimuovere un protone dall’alcol in ingresso rendendolo più reattivo, mentre l’asparagina stabilizza lo stato carico che ne risulta. Insieme favoriscono l’attacco dell’alcol sul donatore acile per formare un intermedio di breve durata che collassa nell’estere desiderato. Anche lo stato ossidato del cofattore flavinico è necessario: in condizioni prive di ossigeno, quando il flavinico si riduce, la transesterificazione si arresta e riprende solo con il reintrodursi dell’aria. Degno di nota, quando lo stesso trio di mutazioni è stato inserito in ossidasi correlate di altri funghi, quegli enzimi hanno guadagnato anch’essi una robusta attività di transesterificazione, suggerendo che questo comportamento è generalizzabile.
Cosa significa per una chimica più verde
Per i non specialisti, il messaggio centrale è che gli autori hanno insegnato a un enzima noto un nuovo trucco: costruire esteri utili direttamente in acqua, ignorando efficacemente la tendenza dell’acqua a disfarsene. Intagliando una tasca asciutta e favorevole agli oli all’interno di una proteina e sintonizzando pochi amminoacidi chiave, hanno creato un catalizzatore che privilegia gli alcoli rispetto all’acqua come partner di reazione. Poiché lo stesso principio di design funziona in enzimi correlati, questo approccio potrebbe essere esteso a una famiglia di catalizzatori per la produzione di aromi, fragranze, chimica fine e possibilmente biocarburanti in processi più sicuri e sostenibili, che fanno meno affidamento su solventi organici aggressivi e più sull’acqua.
Citazione: Wu, B., Ma, Y., Feng, C. et al. Engineered alcohol oxidases catalyse transesterification in aqueous media without competing hydrolysis. Nat Commun 17, 2183 (2026). https://doi.org/10.1038/s41467-026-68899-y
Parole chiave: ingegneria degli enzimi, biocatalisi, chimica verde, sintesi di esteri, flavoproteine