Clear Sky Science · it
La formazione di polaroni dipendente dal potenziale attiva il TiO2 per la reazione di evoluzione dell’idrogeno
Trasformare materiali simili alla ruggine in fabbriche di combustibile pulito
La scissione dell’acqua in idrogeno come combustibile spesso si basa su metalli preziosi costosi. Questo studio mostra che un ossido comune e stabile chiamato biossido di titanio (TiO2) può passare da lento a altamente attivo semplicemente modificando il potenziale elettrico applicato. La chiave è la creazione di piccole e reversibili tasche di carica chiamate polaroni sulla superficie, che aprono nuovi ed efficienti percorsi per la produzione di gas idrogeno.
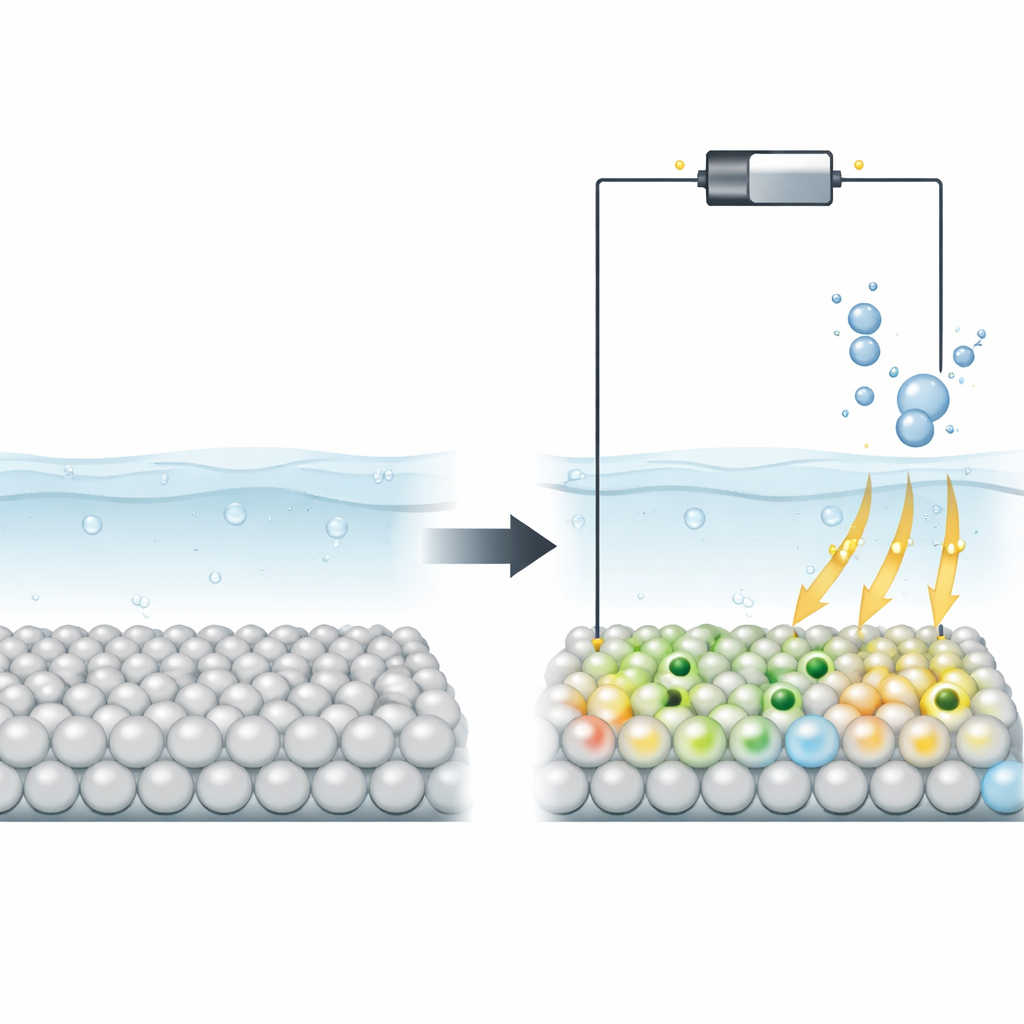
Perché i semiconduttori fanno fatica e come i difetti aiutano
I semiconduttori come il TiO2 sono attraenti per l’energia pulita perché sono economici, abbondanti e già ampiamente impiegati nelle tecnologie solari e fotocatalitiche. Tuttavia nella loro forma perfetta conducono male l’elettricità e spesso legano gli intermedi di reazione o troppo fortemente o troppo debolmente, rendendoli catalizzatori mediocri. I ricercatori hanno a lungo cercato di risolvere questo problema introducendo difetti — atomi mancanti o distorsioni — durante la sintesi. Questi cambiamenti permanenti possono migliorare le prestazioni ma sono difficili da controllare con precisione, e è rimasto poco chiaro, a livello atomico, come tali difetti modifichino la superficie per accelerare reazioni come l’evoluzione dell’idrogeno.
Creare tasche di carica commutabili con la tensione
Gli autori propongono una strategia diversa: usare lo stesso potenziale operativo per modellare in tempo reale la struttura elettronica del TiO2. Quando si applica un potenziale sufficientemente negativo, alcuni ioni titanio in superficie cambiano da uno stato di carica più alto a uno più basso e intrappolano elettroni extra in regioni localizzate note come polaroni. Utilizzando calcoli quantistici a potenziale costante avanzati insieme a misure spettroscopiche in situ, il gruppo dimostra che questi polaroni si formano solo in condizioni riducenti, sono confinati allo strato atomico più esterno e compaiono e scompaiono in modo reversibile quando il potenziale viene ciclato. Ciò significa che la superficie attiva del catalizzatore può essere sintonizzata dinamicamente durante il funzionamento, anziché essere fissata durante la fabbricazione.
Difetti, cariche mobili e rilascio d’idrogeno più rapido
Lo studio prosegue esaminando cosa accade quando la superficie di TiO2 contiene già vacanze di ossigeno — atomi di ossigeno mancanti, comuni nei materiali reali. Queste vacanze favoriscono la presenza di elettroni in prossimità di specifici atomi di titanio, rendendo più facile la formazione di polaroni a potenziali meno negativi. Le simulazioni rivelano che più polaroni possono allinearsi in catene e saltare tra atomi vicini, aumentando notevolmente la conducibilità superficiale. Esperimenti che monitorano segnali magnetici e trasferimento di carica confermano che il TiO2 difettoso accumula più di queste tasche di carica e trasporta gli elettroni più facilmente rispetto al TiO2 perfetto. Di conseguenza, gli elettrodi con vacanze di ossigeno guidano la reazione di evoluzione dell’idrogeno a sovratensioni molto più basse e con correnti molto più alte.
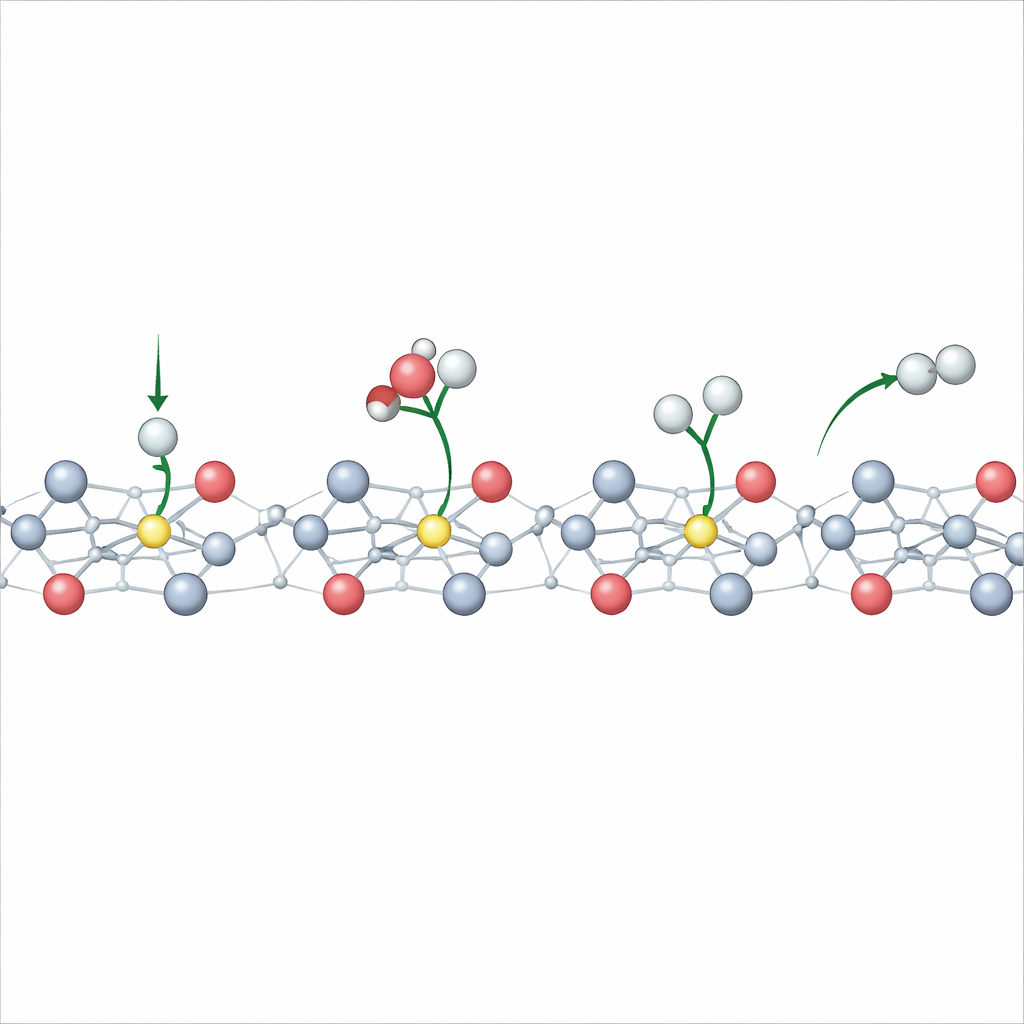
Riconsiderare le regole semplici per le energie di reazione
Negli elettrodi metallici, i chimici fanno spesso affidamento su regole lineari ordinate che collegano energie di reazione, barriere di attivazione e potenziale applicato. Gli autori mostrano che queste regole cominciano a rompersi sul TiO2 quando entrano in gioco i polaroni. L’energia per legare l’idrogeno sulla superficie non cambia più in modo regolare con il potenziale; al contrario, presenta pieghe e discontinuità quando si attivano nuovi stati di polarone. Sorprendentemente, nonostante questo semplice legame tensione–energia fallisca, rimane valida una relazione più generale che collega le barriere di reazione alle energie di reazione. Questo significa che, tenendo conto con cura di quando e dove compaiono i polaroni, è ancora possibile prevedere quanto velocemente si formerà l’idrogeno su queste superfici semiconduttrici.
Progettare catalizzatori più intelligenti e regolabili
Nel complesso, i risultati dipingono il TiO2 come un catalizzatore la cui prestazione non è fissata solo dalla composizione, ma può essere attivamente sintonizzata tramite il potenziale operativo. Combinando difetti incorporati come le vacanze di ossigeno con la formazione di polaroni controllata dalla tensione, la superficie può essere trasformata in una fitta rete di siti altamente attivi e conduttivi per l’evoluzione dell’idrogeno. Per il lettore non specialistico, il messaggio principale è che materiali semiconduttori poco costosi possono essere resi competitivi con i metalli nobili imparando a “accendere” e guidare queste piccole tasche di carica durante il funzionamento, aprendo nuove vie per una produzione di idrogeno efficiente e scalabile e per altre tecnologie elettrochimiche pulite.
Citazione: Wu, T., Guo, X., Zhang, G. et al. Potential-dependent polaron formation activates TiO2 for the hydrogen evolution reaction. Nat Commun 17, 2104 (2026). https://doi.org/10.1038/s41467-026-68892-5
Parole chiave: reazione di evoluzione dell’idrogeno, biossido di titanio, polaroni, elettrocatalisi dei semiconduttori, vacanze di ossigeno