Clear Sky Science · it
Inibizione della segnalazione TGF-β nei microglia stimola la neurogenesi adulta ippocampale e riduce i comportamenti di ansia nei topi adulti
Perché le cellule immunitarie cerebrali sono importanti per umore e memoria
La maggior parte di noi pensa alle cellule immunitarie come pattuglianti del corpo, non come modellatrici dei nostri pensieri e sentimenti. Questo studio mette in discussione tale visione mostrando che i microglia — le cellule immunitarie residenti nel cervello — possono influenzare in modo potente la nascita di nuovi neuroni nell’ippocampo, una regione importante per memoria ed emozione. Disattivando una specifica via di segnalazione nei microglia di topi adulti, i ricercatori hanno aumentato la produzione e la sopravvivenza dei nuovi neuroni e hanno osservato cambiamenti misurabili nel comportamento simile all’ansia.
Il tranquillo nido cerebrale per i nuovi neuroni
Nei mammiferi adulti, nuovi neuroni nascono ancora in alcune nicchie specializzate. Una delle più importanti è la zona subgranulare dell’ippocampo, che aiuta a separare ricordi simili, supporta l’apprendimento e contribuisce alla regolazione dell’umore. In condizioni normali, molte di queste cellule neonate muoiono prima di raggiungere la maturazione. Il loro numero può aumentare o diminuire in risposta a esercizio fisico, ambienti arricchiti, stress, ictus o epilessia. I microglia sorvegliano costantemente questo ambiente, ma non era chiaro se il loro stato reattivo, «infiammato», favorisca o ostacoli questa neurogenesi adulta.
Spegnere un freno chiave nei microglia
Il gruppo si è concentrato su una molecola di segnalazione chiamata TGF-beta, che normalmente mantiene i microglia in uno stato calmo e omeostatico. Utilizzando topi geneticamente modificati, hanno disabilitato selettivamente la segnalazione TGF-beta nei microglia in età adulta — rimuovendo il ligando TGF-beta stesso o i recettori (ALK5 o TβRII) che lo rilevano. Ciò ha spinto i microglia verso un profilo reattivo e pro-infiammatorio senza causare una perdita diffusa di neuroni. In questo stato i microglia sono aumentati in numero e hanno cambiato forma, indice di attivazione, mentre le cellule di supporto vicine chiamate astrociti sono rimaste in gran parte non interessate.
Piu nuovi neuroni, migliore sopravvivenza e ansia alterata
Quando la segnalazione TGF-beta è stata spenta nei microglia, la nicchia ippocampale ha prodotto un’ondata di neuroni immaturi contrassegnati dalla proteina DCX. Questo picco è apparso circa tre settimane dopo l’intervento genetico e ha portato a un aumento duraturo di neuroni pienamente maturi nelle settimane successive. Il monitoraggio accurato delle cellule in divisione ha mostrato che l’effetto principale è stato un miglioramento della sopravvivenza dei neuroni neonati, non semplicemente una divisione cellulare più rapida. Rimuovere completamente i microglia con un farmaco non ha replicato questo effetto, suggerendo che non è l’assenza di microglia a contare, ma il profilo reattivo specifico creato quando TGF-beta è silenziato. A livello comportamentale, i topi con microglia carenti di TGF-beta hanno trascorso più tempo nelle braccia aperte dei labirinti elevati, un segno comune di ridotta ansia o di disinibizione. Questi cambiamenti sono svaniti quando i microglia in alcuni modelli sono tornati a uno stato più normale, ma sono persisti in altri modelli in cui i microglia sono rimasti reattivi.
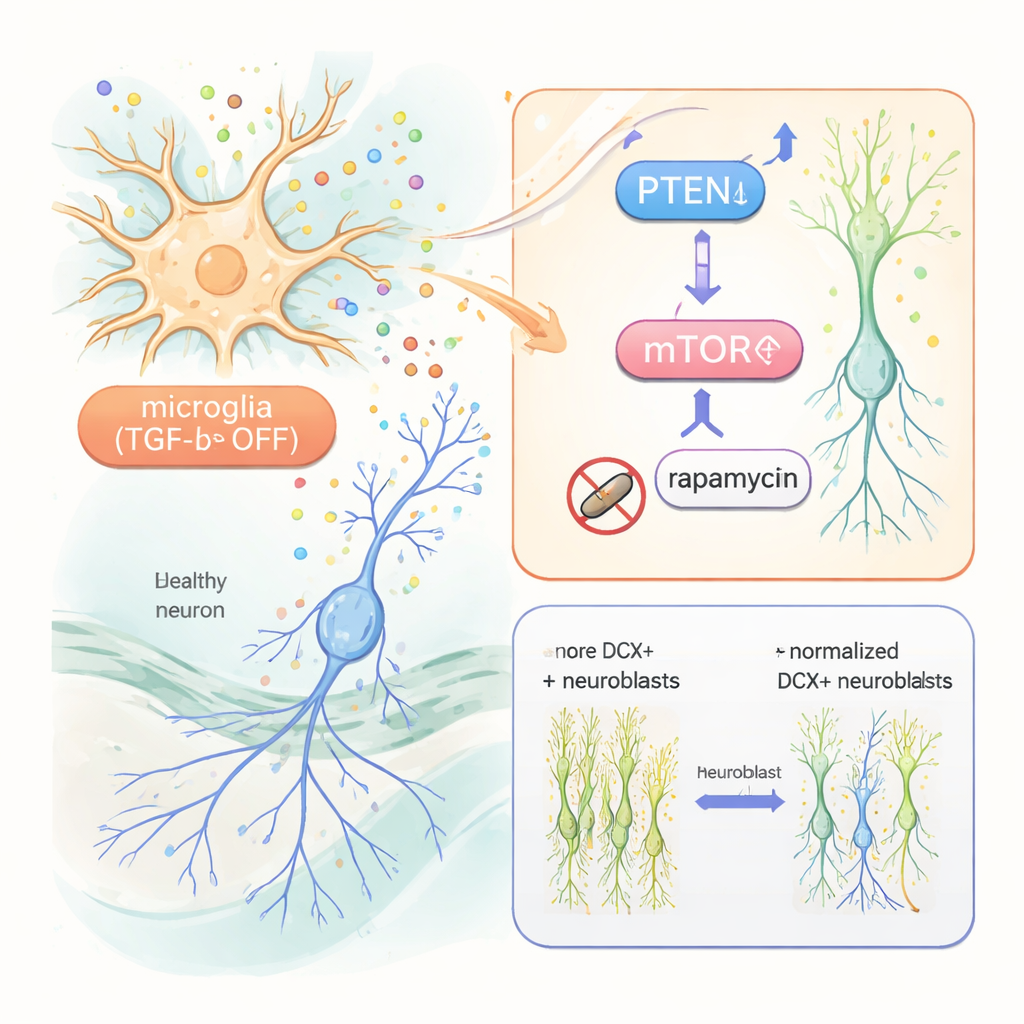
Scoprire la via all’interno dei neuroni neonati
Per capire come i microglia alterati comunicano con i neuroni neonati, i ricercatori hanno usato il sequenziamento dell’RNA a singola cellula sulle cellule ippocampali. Hanno trovato cambiamenti ampi nell’attività genica non solo nei microglia ma anche nei neuroni immaturi. Tra i più rilevanti c’è stata una riduzione di PTEN, una proteina che normalmente frena la crescita cellulare, e segnali di aumento dell’attività nella via mTOR, che promuove la sopravvivenza e la crescita cellulare. È interessante che fattori di crescita ben noti come IGF‑1 e TNF‑alpha, pur elevati nei microglia reattivi, si siano rivelati non necessari: anche quando questi sono stati rimossi geneticamente, l’aumento della neurogenesi è rimasto. Al contrario, quando il team ha trattato i topi con rapamicina, un farmaco che blocca mTOR, l’eccesso di neuroni immaturi e il loro ramificarsi esuberante sono tornati alla normalità. I neuroni neonati mostravano anche livelli più alti di un marcatore a valle di mTOR, che la rapamicina ha ridotto.
Cosa potrebbe significare per la salute cerebrale
Nel complesso, i risultati suggeriscono che quando la segnalazione TGF-beta nei microglia viene spenta, queste cellule assumono uno stato reattivo che favorisce la sopravvivenza e l’integrazione dei neuroni ippocampali neonati tramite una via PTEN–mTOR all’interno di quei neuroni. Questo, a sua volta, è collegato a una riduzione del comportamento simile all’ansia nei topi, sebbene possa accompagnarsi a cambiamenti nell’apprendimento e nella memoria. Per un pubblico non specialistico, il messaggio chiave è che le cellule immunitarie del cervello possono modulare quanti nuovi neuroni si uniscono ai circuiti della memoria — e che modulare con cura questo sistema potrebbe un giorno aiutare a potenziare la neurogenesi benefica o a contenere neuroni che si ramificano eccessivamente in condizioni come l’epilessia o dopo un danno cerebrale.
Citazione: Ware, K., Peter, J., Yazell, J. et al. Inhibition of TGF-β signaling in microglia stimulates hippocampal adult neurogenesis and reduces anxiety-like behavior in adult mice. Nat Commun 17, 1440 (2026). https://doi.org/10.1038/s41467-026-68885-4
Parole chiave: neurogenesi adulta, microglia, ippocampo, comportamento d’ansia, segnalazione TGF-beta