Clear Sky Science · it
L’adattamento post‑traduzionale mediato da PRMT3 al digiuno regola la flessibilità metabolica
Perché il momento dei pasti e il carburante corporeo contano
Molte persone provano il digiuno o il consumo alimentare a tempo limitato per perdere peso o migliorare la glicemia, ma i risultati possono essere contrastanti. Questo studio scende sotto il cofano del nostro metabolismo per capire il perché. Concentrandosi sul grasso addominale nei topi e su campioni umani, i ricercatori scoprono un interruttore molecolare che aiuta il tessuto adiposo a decidere se bruciare o immagazzinare combustibile, e mostrano come sia la tempistica dei pasti sia un farmaco possano voltare quell’interruttore verso una salute migliore.
Un motore flessibile all’interno del nostro grasso
I nostri corpi funzionano al meglio quando sanno passare agevolmente dal bruciare grasso durante il digiuno al bruciare zuccheri dopo i pasti. Questa “flessibilità metabolica” spesso si perde nell’obesità, rendendo più difficile gestire le oscillazioni dell’offerta e della domanda di energia. Il gruppo ha studiato il grasso bianco viscerale — il grasso profondo dell’addome fortemente associato a diabete e malattie cardiache — e ha scoperto che tag molecolari specifici sulle proteine, chiamati gruppi metile, variano con il pasto e il digiuno. In topi e in esseri umani, due di questi segni, MMA e ADMA, aumentano nel grasso viscerale con l’aumentare del peso corporeo e dell’indice di massa corporea, suggerendo che siano marcatori di un metabolismo lento e meno adattabile.
Un segnale alimentare che irrigidisce il metabolismo
I ricercatori si sono concentrati su un enzima nelle cellule adipose chiamato PRMT3, che aggiunge questi segni metilici. Nei topi, i livelli di PRMT3 nel grasso viscerale aumentano di notte quando gli animali mangiano e calano di giorno quando digiunano, seguendo da vicino il profilo di MMA e ADMA. Questo ritmo dipende dall’insulina e da una proteina di segnalazione chiave, AKT: quando il cibo o l’insulina iniettata attivano AKT, PRMT3 si attiva e viene maggiormente modificato, il che a sua volta aumenta la quantità di proteine metilate. Bloccare AKT o inibire direttamente PRMT3 appiattisce rapidamente questo segnale di metilazione, mimando persino l’effetto di un digiuno molto più lungo.
Riconfigurare le cellule adipose dallo stoccaggio al consumo
Cosa fa realmente questa marcatura chimica? Lo studio mostra che PRMT3 stabilizza un trasportatore proteico chiamato SLC25A1 nei mitocondri — le centrali energetiche della cellula. SLC25A1 sposta il citrato, un intermedio metabolico chiave, fuori dai mitocondri nel fluido cellulare dove alimenta la sintesi del nuovo grasso. PRMT3 metila due siti specifici di arginina su SLC25A1, rendendo il trasportatore più stabile e favorendo l’esportazione di citrato e la formazione di grasso. Quando PRMT3 è bloccato, i livelli di SLC25A1 diminuiscono, l’esportazione di citrato cala e le cellule adipose si spostano verso la degradazione degli zuccheri invece che la produzione di nuovo grasso. Nei topi alimentati con una dieta ricca di grassi, un farmaco che blocca PRMT3 riduce il grasso corporeo, migliora il controllo glicemico e aumenta una misura chiamata rapporto di scambio respiratorio, dimostrando che gli animali passano più facilmente al consumo di carboidrati.
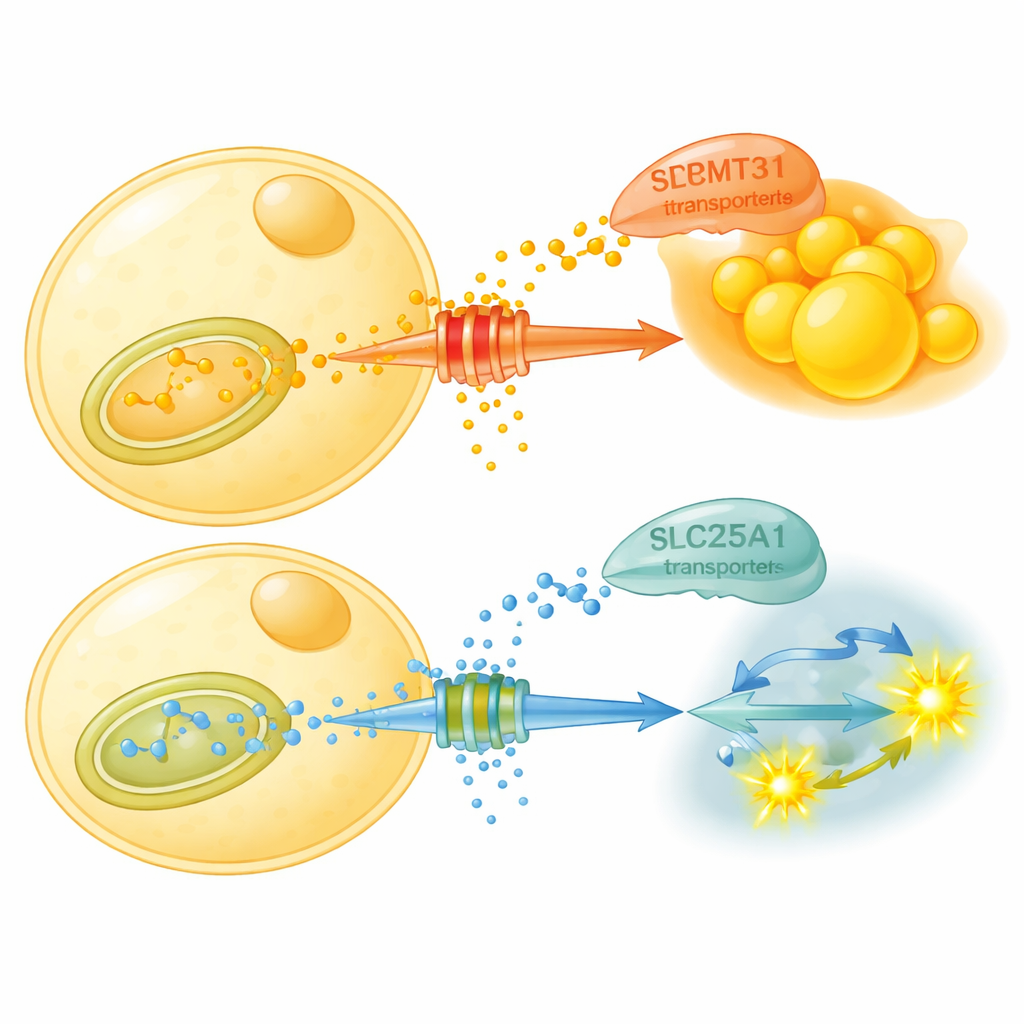
I ritmi del digiuno e le modifiche genetiche indicano la stessa via
I ricercatori hanno poi chiesto se gli schemi comuni di digiuno usino lo stesso interruttore. Con un protocollo 16:8 a tempo limitato — 16 ore di digiuno e 8 ore di alimentazione — i topi hanno perso peso e gestito meglio il glucosio senza mangiare meno in totale. Il loro grasso viscerale mostrava livelli inferiori di PRMT3, SLC25A1 e proteine metilate, e il loro uso di carburante è diventato più flessibile, specialmente di notte quando normalmente mangiano. Sorprendentemente, somministrare il farmaco inibitore di PRMT3 in momenti specifici del giorno ha prodotto molti degli stessi benefici del protocollo 16:8. La rimozione genetica di SLC25A1 solo nelle cellule adipose ha inoltre protetto i topi dall’iperglicemia e dalla steatosi epatica indotte dalla dieta, ancora potenziando la degradazione degli zuccheri e l’uso energetico nel grasso, anche senza ridurre la massa grassa.
Cosa significa per le terapie future
Complessivamente, i risultati suggeriscono che il grasso profondo dell’addome contiene un interruttore sensibile alla temporizzazione, controllato da insulina, AKT, PRMT3 e SLC25A1, che determina se i nostri corpi rimangono metabolicamente agili o si bloccano in una modalità di accumulo. L’alimentazione a tempo limitato sembra spingere questo interruttore verso la flessibilità abbassando PRMT3 e i suoi effetti a valle. Un farmaco che inibisce PRMT3 può riprodurre molti di questi vantaggi nei topi obesi, suggerendo una futura terapia che renda più accessibili i benefici metabolici del digiuno. Per i lettori comuni, il messaggio è che quando mangiamo, non solo ciò che mangiamo, può rimodellare il modo in cui il tessuto adiposo gestisce il carburante — con conseguenze importanti per il peso, la glicemia e la salute a lungo termine.
Citazione: Huang, Z., Liu, X., Chen, X. et al. PRMT3-mediated post-translational adaptation to fasting regulates metabolic flexibility. Nat Commun 17, 2264 (2026). https://doi.org/10.1038/s41467-026-68883-6
Parole chiave: flessibilità metabolica, alimentazione a tempo limitato, grasso viscerale, metilazione delle proteine, metabolismo del glucosio