Clear Sky Science · it
Un nanodispositivo a base di DNA rileva il segnale purinergico e guida un interruttore immunitario per la risoluzione dell’infiammazione
Abbassare il sistema d’allarme del corpo
Quando i nostri tessuti vengono danneggiati, le cellule rilasciano un’ondata di “segnali d’allarme” chimici che richiamano le cellule immunitarie per combattere le infezioni e rimuovere i detriti. Questa risposta è vitale, ma se l’allarme suona troppo forte o per troppo tempo può causare infiammazione dannosa nei polmoni, nei reni e in altri organi. Questo studio descrive un minuscolo dispositivo programmabile a base di DNA che può rilevare quando il segnale d’allarme è eccessivo e ridurlo in modo silenzioso, aiutando il sistema immunitario a passare dalla modalità d’attacco a quella di riparazione.
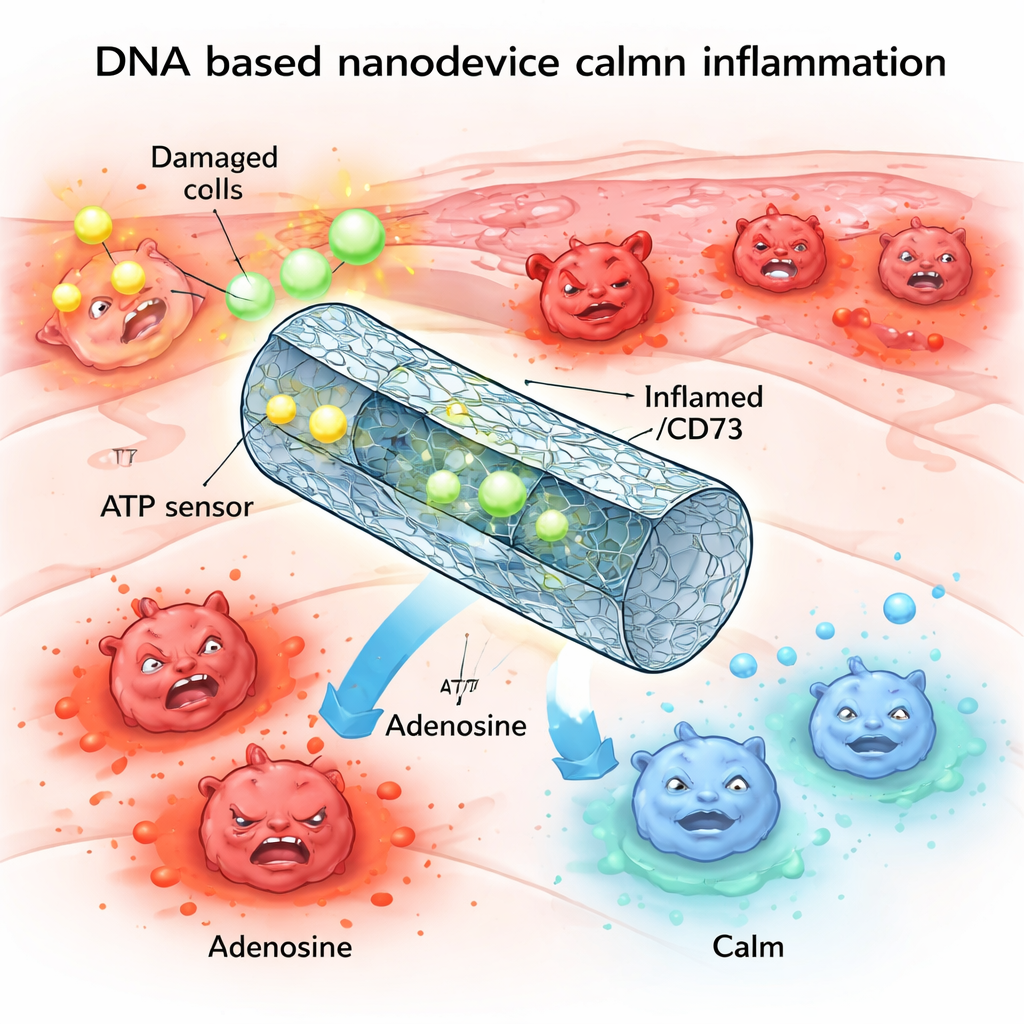
Un allarme chimico che può sfuggire al controllo
Uno dei principali messaggeri d’allarme dell’organismo è l’ATP, noto soprattutto come “moneta energetica” all’interno delle cellule. In caso di lesione o stress, grandi quantità di ATP fuoriescono dalle cellule danneggiate nello spazio circostante. Lì, questo ATP extracellulare funge da segnale di pericolo, legandosi a recettori sulle cellule immunitarie e spingendole verso uno stato altamente infiammatorio. In condizioni sane, enzimi sulla superficie cellulare degradano rapidamente l’eccesso di ATP in adenosina, una molecola correlata con effetti calmanti e anti-infiammatori. Ma in molte malattie infiammatorie croniche o gravi, questo sistema di degradazione è compromesso, lasciando livelli alti di ATP, bassi di adenosina e tessuti intrappolati in un ciclo di danno.
Costruire un tubo intelligente di DNA
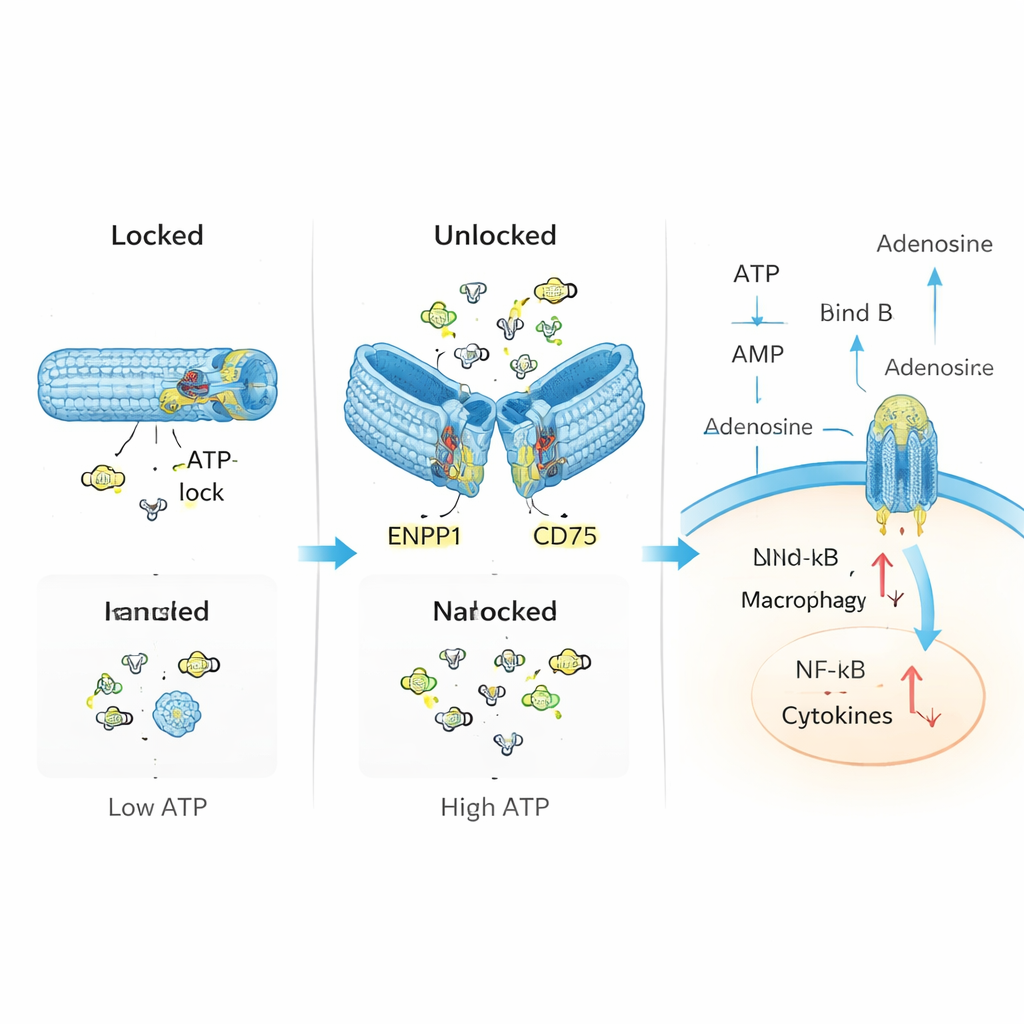
I ricercatori hanno voluto imitare e riparare questo sistema di controllo naturale usando la nanotecnologia del DNA. Hanno costruito un tubo cavo di DNA, ripiegato in modo simile all’origami, e lo hanno dotato di due componenti principali: “sensori” che riconoscono l’ATP e enzimi che convertono l’ATP in adenosina. Nel suo stato di riposo, bloccato, il tubo è tenuto chiuso da brevi segmenti di DNA che fungono anche da sensori per l’ATP. Quando i livelli di ATP superano una certa soglia tipica dei tessuti lesionati, l’ATP si lega a questi segmenti, facendo aprire il tubo ed esponendo gli enzimi ENPP1 e CD73 al suo interno. Questi poi degradano l’eccesso di ATP e producono adenosina, spostando delicatamente l’equilibrio chimico locale dal pericolo alla risoluzione.
Dimostrare che l’interruttore funziona
In test di laboratorio controllati, il team ha confermato che il loro tubo di DNA resta chiuso a bassi livelli di ATP ma si apre in modo affidabile quando l’ATP diventa abbondante, proprio come una valvola di emergenza. Una volta sbloccato, il dispositivo converte costantemente l’ATP in prodotti intermedi e infine in adenosina, senza compromettere in modo significativo l’attività degli enzimi. Nelle cellule immunitarie esposte ad alti livelli di ATP, questo nanodispositivo ha ridotto prodotti secondari tossici nei mitocondri, diminuito l’attivazione di vie infiammatorie come NF-κB e l’inflammasoma NLRP3, e aumentato segnali collegati agli effetti calmanti dell’adenosina. In altre parole, il dispositivo non si è limitato a eliminare l’ATP; ha effettivamente rimodulato il comportamento cellulare da infiammatorio a regolatorio.
Fare autostop verso i siti di lesione
Progettare un interruttore intelligente è una cosa; portarlo nel punto giusto del corpo è un’altra. Per risolvere questo problema di consegna, i ricercatori hanno attaccato i loro tubi di DNA alla superficie dei monociti circolanti, un tipo di globuli bianchi che si dirige naturalmente verso i tessuti infiammati. Usando un’ancora di DNA legata al colesterolo, hanno “parcheggiato” un gran numero di nanodispositivi sulla membrana di ciascuna cellula, dove i dispositivi sono rimasti per lo più in superficie anziché essere internalizzati. Nei modelli murini di danno acuto ai polmoni e ai reni, questi monociti decorati si sono accumulati negli organi danneggiati molto più efficacemente dei dispositivi liberi, e i nanodispositivi hanno continuato a rispondere in modo specifico all’elevato ATP nei tessuti lesionati.
Favorire la guarigione dei tessuti
Nei topi con lesioni polmonari o renali indotte chimicamente, il trattamento con il dispositivo di DNA ha ridotto il danno tissutale, l’accumulo di cellule immunitarie e i messaggeri infiammatori. La versione trasportata dai monociti ha funzionato meglio, offrendo una protezione più forte rispetto sia al dispositivo libero sia agli enzimi da soli. Analisi genetiche e metaboliche più approfondite del tessuto polmonare hanno mostrato che questo approccio non solo attenuava i geni infiammatori, ma aiutava anche a ristabilire il metabolismo energetico alterato nelle cellule. È importante sottolineare che i dispositivi hanno mostrato bassa tossicità e non hanno scatenato reazioni immunitarie dannose negli animali sani.
Perché questo è importante per le terapie future
Per un pubblico non specializzato, il messaggio chiave è che questo lavoro dimostra un “termostato” molecolare programmabile per l’infiammazione. Costruito con DNA ed enzimi naturali, il nanodispositivo rileva quando un segnale di pericolo è troppo forte e lo converte automaticamente in un segnale calmante, aiutando le cellule immunitarie a calmarsi e i tessuti a ripararsi. Pur essendo ancora in una fase sperimentale iniziale, questa strategia suggerisce una nuova classe di trattamenti che non si limitano a bloccare le vie immunitarie ovunque, ma riequilibrano localmente i segnali chimici nei siti di lesione, offrendo potenzialmente un controllo preciso dell’infiammazione dannosa in molte malattie.
Citazione: Li, W., Liu, S., Zhou, X. et al. A DNA-based nanodevice senses purinergic signaling and drives an immune switch for resolving inflammation. Nat Commun 17, 2030 (2026). https://doi.org/10.1038/s41467-026-68879-2
Parole chiave: nanodispositivo di DNA, ATP extracellulare, infiammazione, segnalazione dell’adenosina, nanomedicina