Clear Sky Science · it
Immunoterapia anti-TLR2 modula la propagazione neuronale verso oligodendrociti della α-sinucleina in modelli murini e umani
Perché questa ricerca è importante
L’atrofia sistemica multipla (MSA) è una malattia cerebrale rara ma rapidamente progressiva che combina problemi motori simili al Parkinson con alterazioni dell’equilibrio e del sistema autonomo, come cali della pressione sanguigna. I medici possono alleviare i sintomi, ma al momento non sono in grado di rallentare la malattia stessa. Questo studio rivela come una proteina mal ripiegata si diffonde tra le cellule cerebrali danneggiando l’“isolamento dei fili” del cervello e mostra che un trattamento con anticorpi mirati può interrompere questo processo in modelli animali e cellulari. Il lavoro indica una strategia concreta, simile a un farmaco, che un giorno potrebbe cambiare il corso della MSA invece di limitarsi a trattarne i sintomi.
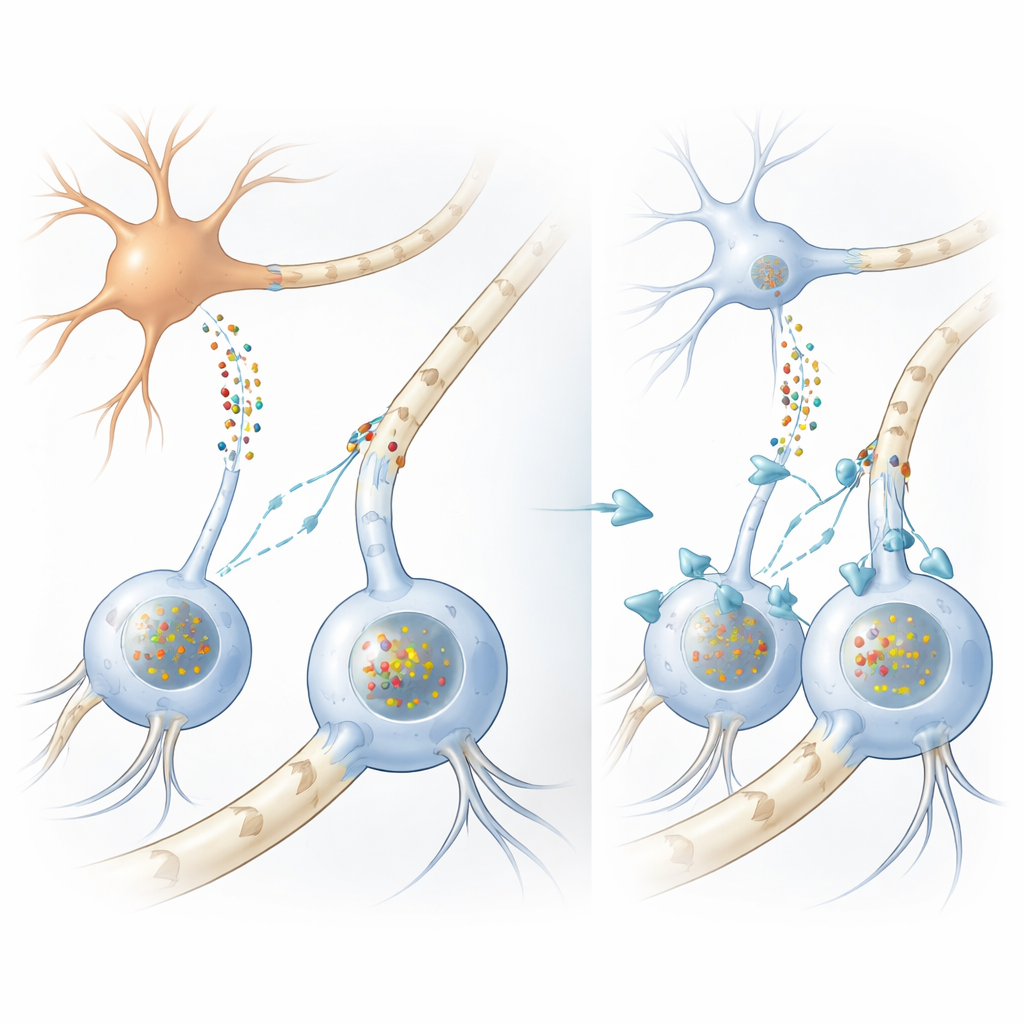
Come si guasta il cablaggio cerebrale
In molti disturbi del movimento, incluso il morbo di Parkinson, si accumulano aggregati di una proteina chiamata alpha-sinucleina all’interno dei neuroni. Nella MSA, però, gli aggregati più evidenti si formano all’interno delle cellule di supporto chiamate oligodendrociti, che normalmente avvolgono le fibre nervose con guaine di mielina ricche di lipidi per accelerare la conduzione elettrica. È strano perché gli oligodendrociti producono pochissima alpha-sinucleina, lasciando un enigma di lunga data: da dove provengono i massicci depositi proteici in queste cellule? Gli autori hanno innanzitutto confermato, usando campioni cerebrali umani e ampie analisi di RNA, che gli oligodendrociti producono effettivamente molto meno alpha-sinucleina rispetto ai neuroni, rafforzando l’idea che la proteina dannosa debba arrivare dall’esterno.
Proteina passata dal neurone alla cellula di supporto
Per verificare questa ipotesi, il gruppo ha costruito diversi modelli complementari. In colture cellulari hanno differenziato cellule simili a oligodendrociti da cellule staminali neurali e le hanno esposte al mezzo raccolto da cellule simili a neuroni ingegnerizzate per rilasciare grandi quantità di alpha-sinucleina. Le cellule di supporto hanno assorbito questa proteina e sviluppato aggregati molto simili alle inclusioni gliali osservate nei cervelli di pazienti con MSA, completi dei medesimi marcatori chimici e proteine ausiliarie. Quando i ricercatori hanno esaminato un ceppo murino che esprime la alpha-sinucleina umana mutata solo nei neuroni, hanno nuovamente trovato aggregati della proteina umana all’interno degli oligodendrociti della sostanza bianca, nonostante queste cellule non esprimessero il gene umano. Nel loro insieme, questi esperimenti mostrano che la alpha-sinucleina può spostarsi dai neuroni agli oligodendrociti e formare lì inclusioni simili a quelle della malattia.
La porta sulla superficie cellulare
Successivamente, gli scienziati hanno indagato come la proteina entri negli oligodendrociti. Lavori precedenti avevano identificato il recettore Toll-like 2 (TLR2), un sensore immunitario sulla superficie cellulare, come sito di binding per la alpha-sinucleina nei neuroni e nelle microglia. Analizzando dataset di espressione genica provenienti da cervelli di pazienti con MSA, il team ha scoperto che gli oligodendrociti dei pazienti presentavano livelli insolitamente alti di TLR2 rispetto ai controlli, e che un livello maggiore di TLR2 era associato a livelli inferiori di geni correlati alla mielina, come la proteina basica della mielina. Tale relazione non è emersa in diversi dataset indipendenti sul Parkinson, suggerendo che la sensibilità degli oligodendrociti alla alpha-sinucleina mediata da TLR2 è una caratteristica distintiva della MSA piuttosto che un tratto comune a tutti i disordini da sinucleina.
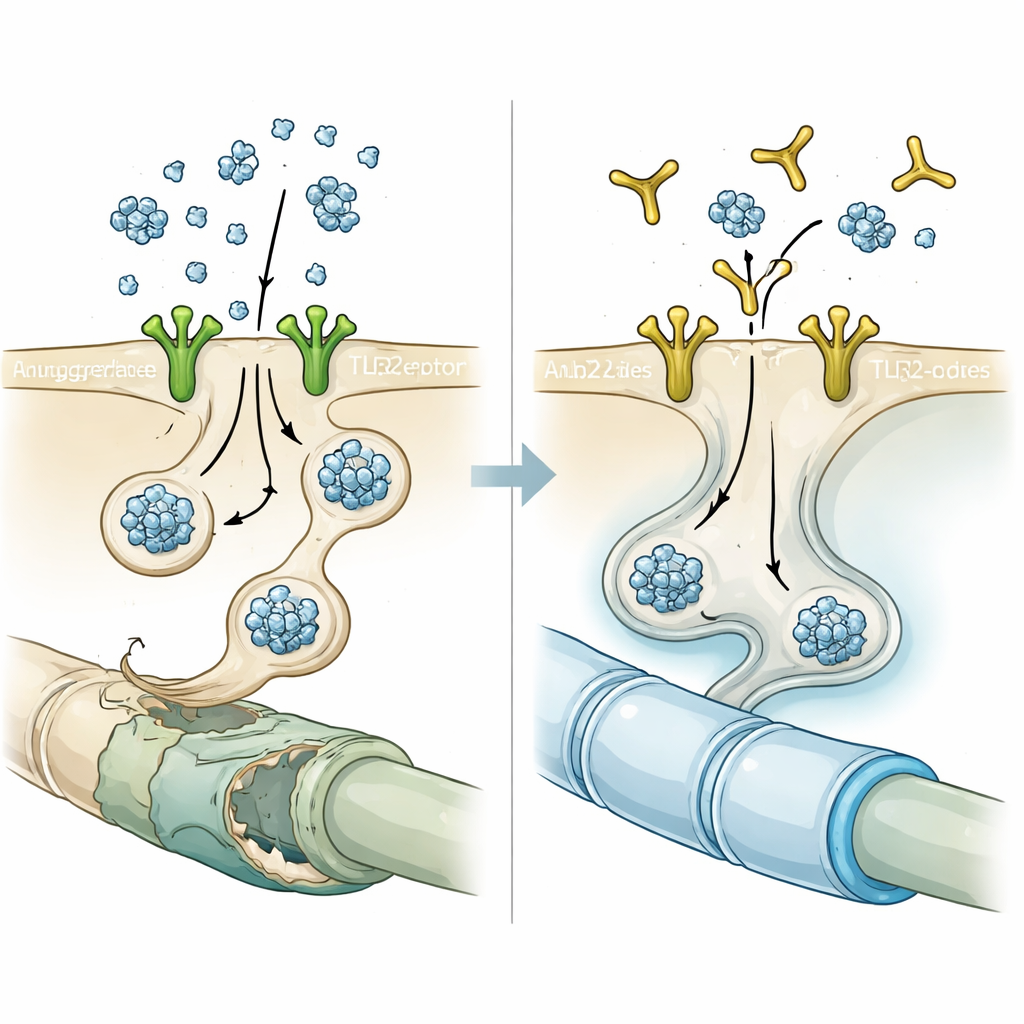
Bloccare la porta con un anticorpo
Partendo da questo indizio, i ricercatori hanno testato NM-101, un anticorpo progettato per legarsi a TLR2 e impedirne l’attivazione. Nelle colture cellulari, un breve pre-trattamento degli oligodendrociti con NM-101 prima dell’aggiunta di alpha-sinucleina di origine neuronale ha ridotto nettamente il numero e l’intensità degli aggregati simili a inclusioni. Nei topi che sovraesprimevano la alpha-sinucleina neuronale o che avevano ricevuto iniezioni di fibrille preformate di alpha-sinucleina, infusioni settimanali di NM-101 hanno ridotto la proteina aggregata nella sostanza bianca, attenuato le risposte infiammatorie di microglia e astrociti e diminuito l’attivazione di un enzima infiammatorio chiamato caspasi-1 all’interno degli oligodendrociti. Gli animali trattati hanno vissuto più a lungo e ottenuto risultati migliori nei test motori, suggerendo che gli effetti protettivi dell’anticorpo erano funzionalmente rilevanti e non solo curiosità microscopiche.
Riparare l’isolamento danneggiato
Poiché gli oligodendrociti sono i produttori di mielina del cervello, il team ha esaminato se il trasferimento di alpha-sinucleina danneggiasse la mielina e se il blocco di TLR2 potesse aiutare. Il sequenziamento dell’RNA a singola cellula di oligodendrociti derivati da tessuto umano esposti a alpha-sinucleina condizionata da neuroni ha rivelato ampi spostamenti lontano da uno stato maturo produttore di mielina verso un profilo più immaturo, simile a progenitore, con molti geni chiave della mielina ridotti. Studi paralleli sull’espressione genica di oligodendrociti catturati al laser da pazienti con MSA e dal modello murino hanno mostrato una firma condivisa: ridotta espressione di geni coinvolti nella formazione e nel mantenimento della mielina. Al microscopio elettronico, la sostanza bianca nei topi con alpha-sinucleina mostrava guaine mieliniche più sottili e disorganizzate. Il trattamento con NM-101 ha invertito molte di queste modifiche, ispessendo la mielina, ripristinando i livelli delle proteine mieliniche e normalizzando l’espressione dei geni necessari alla maturazione degli oligodendrociti.
Cosa significa tutto questo per i trattamenti futuri
Lo studio sostiene una linea narrativa chiara: nella MSA, la alpha-sinucleina prodotta dai neuroni può diffondersi negli oligodendrociti attraverso il TLR2 sulla loro superficie, dove si accumula, innesca infiammazione, devia il programma di sviluppo delle cellule ed erode il rivestimento mielinico del cablaggio cerebrale. Bloccando TLR2 con un anticorpo mirato, i ricercatori sono riusciti a interrompere questa catena di eventi in topi e modelli cellulari umani, riducendo le inclusioni tossiche, calmando l’infiammazione, riparando la mielina e migliorando la sopravvivenza e la funzione motoria. Pur richiedendo ancora rigorosi test clinici sull’uomo per NM-101, il lavoro stabilisce il trasferimento proteico dipendente da TLR2 come un motore centrale della patologia simile alla MSA e indica l’immunoterapia anti-TLR2 come una strategia promettente per rallentare o prevenire questa devastante malattia.
Citazione: Bae, EJ., Ham, S., Jeong, Y.W. et al. Anti-TLR2 immunotherapy modulates neuron-to-oligodendrocyte propagation of α-synuclein in mouse and human models. Nat Commun 17, 2175 (2026). https://doi.org/10.1038/s41467-026-68870-x
Parole chiave: atrofia sistemica multipla, alpha-sinucleina, oligodendrociti, danno alla mielina, immunoterapia