Clear Sky Science · it
Olig2 agisce come una barriera inducibile nella conversione in vivo da astrociti a neuroni
Trasformare le cellule di supporto del cervello in neuroni
Il cervello adulto ha una capacità limitata di sostituire i neuroni perduti, un ostacolo importante in patologie come l’ictus, l’Alzheimer e le lesioni del midollo spinale. Un’idea promettente è convertire direttamente in loco le cellule di “supporto” vicine, chiamate astrociti, in nuovi neuroni mediante terapia genica. Questo studio pone una domanda chiave: cosa impedisce a questa conversione di funzionare in modo efficiente all’interno del cervello vivente — e si possono rimuovere quei freni?
Un freno nascosto al cambiamento d’identità cellulare
Gli astrociti normalmente nutrono i neuroni, mantengono l’equilibrio chimico cerebrale e rispondono alle lesioni. In alcuni stati patologici, possono comportarsi un po’ come cellule staminali, alimentando la speranza di poterli riprogrammare in neuroni sul posto. Gli scienziati sanno già che una classe di geni chiamati fattori di trascrizione proneurali — come Ngn2, Ascl1 e NeuroD1 — può spingere gli astrociti verso un’identità neuronale. Tuttavia, negli animali questa conversione da astrociti a neuroni resta frustrantemente inefficiente. Gli autori hanno ipotizzato che, oltre alle difese preesistenti, gli astrociti possano attivare una nuova barriera inducibile quando viene scatenata la riprogrammazione.
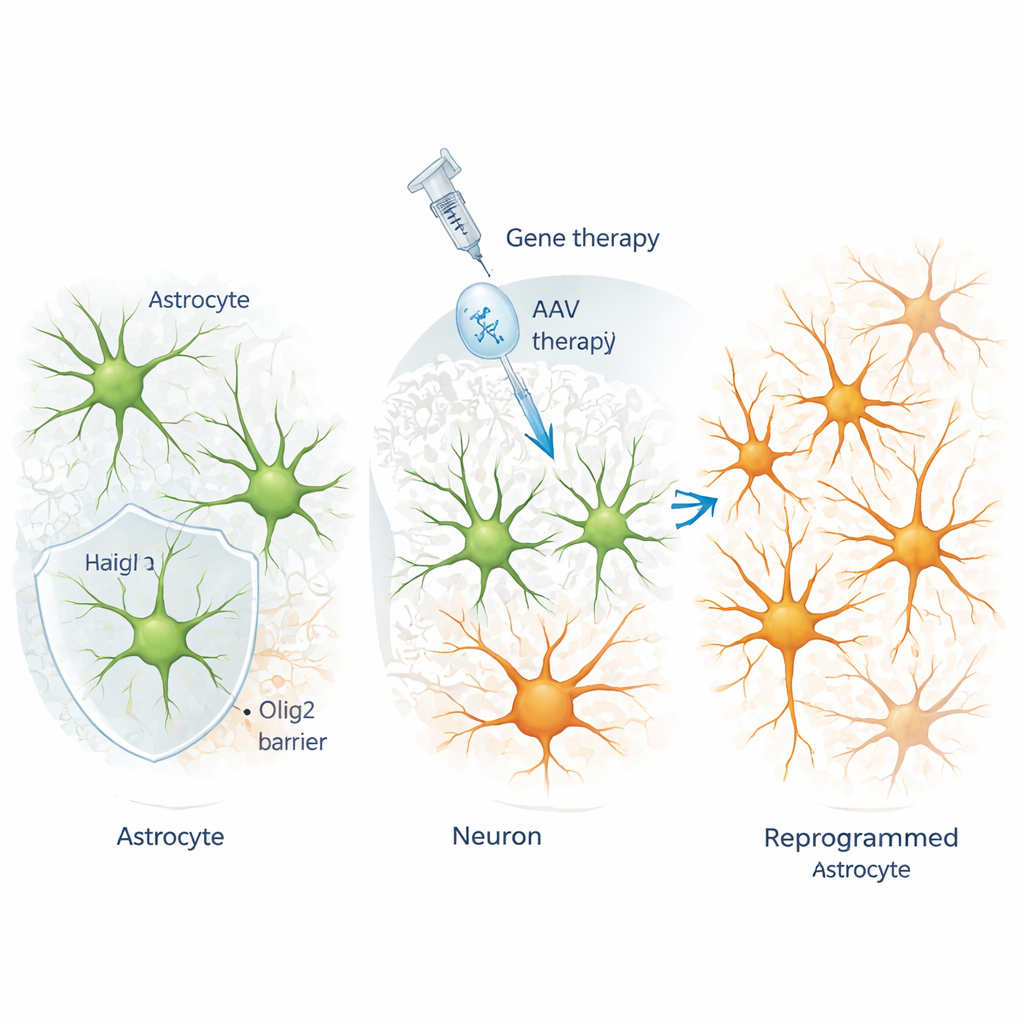
Una proteina chiamata Olig2 interviene per resistere al cambiamento
Lavorando nella corteccia del topo adulto, i ricercatori hanno introdotto fattori di riprogrammazione negli astrociti usando virus ingegnerizzati altamente selettivi per queste cellule. Hanno scoperto che ogni volta che un fattore bHLH (basic helix–loop–helix) come Ngn2, Ascl1 o NeuroD1 veniva forzato negli astrociti, un’altra proteina bHLH, Olig2, veniva drammaticamente attivata. In condizioni normali Olig2 si trova nelle cellule della linea degli oligodendrociti, non negli astrociti corticali maturi. Esperimenti di tracciamento accurati hanno mostrato che le cellule extra positive per Olig2 dopo il trattamento non derivavano dalla proliferazione di precursori oligodendrocitari: erano invece gli stessi astrociti bersaglio della conversione ad attivare Olig2 in risposta al segnale di riprogrammazione.
Rimuovere il freno triplica la conversione e produce neuroni funzionanti
Per verificare se Olig2 sia davvero una barriera, il team ha usato RNA a forcina corta (shRNA) per abbassare specificamente Olig2 negli astrociti ai quali era stato anche fornito Ngn2. Silenziare Olig2 ha ridotto quasi a zero i livelli proteici in queste cellule e ha avuto un effetto notevole: la percentuale di astrociti etichettati che è diventata neurone è aumentata di circa tre volte rispetto a Ngn2 da solo. Nel corso di alcune settimane molte cellule hanno attraversato uno stadio intermedio, perdendo marcatori tipici degli astrociti prima di acquisire completamente marcatori neuronali. Registrazioni elettriche su fette di cervello hanno mostrato che le cellule convertite generavano potenziali d’azione e, in circa la metà dei casi, ricevevano input sinaptici eccitatori e inibitori — caratteristiche tipiche dell’integrazione funzionale nei circuiti locali.
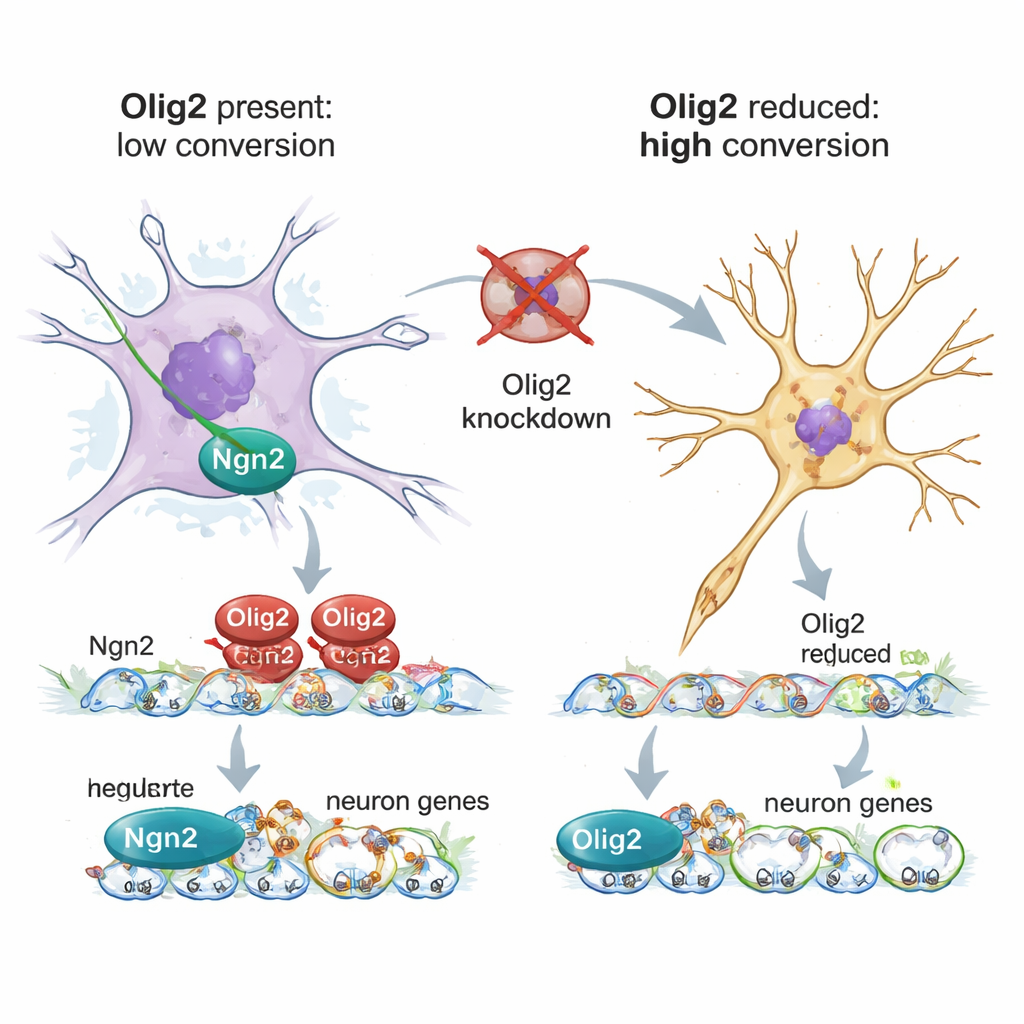
Come Olig2 blocca l’avvio del programma neuronale
Utilizzando RNA-seq a cellula singola, gli autori hanno profilato migliaia di singoli astrociti esposti a Ngn2, con o senza il knockdown di Olig2. Quando Olig2 era presente, gli astrociti mutavano solo parzialmente l’espressione genica: alcuni percorsi metabolici e di sintesi proteica risultavano alterati, ma i geni chiave degli astrociti restavano attivi e molti geni coinvolti nella costruzione neuronale restavano silenziati. Quando Olig2 era ridotto, gli astrociti sopprimevano più completamente il loro programma di cellule di supporto mature e sovraregolavano geni associati a cellule staminali neurali, neurogenesi e crescita assonale. Un metodo complementare, CUT&Tag, ha mappato dove Olig2 si lega al DNA in questi astrociti riprogrammati. Olig2 si è legato a regioni regolatorie di molti geni pro-neurogenici — incluso lo stesso Ngn2 — coerente con un ruolo di repressore diretto che attenua il fattore di riprogrammazione e mantiene spenti i geni neuronali.
Rimodellare l’identità cellulare sollevando una difesa inducibile
Nel complesso, il lavoro rivela che gli astrociti attivano una difesa attiva e inducibile contro la loro conversione in neuroni: una volta introdotto un fattore proneurale come Ngn2, questo induce Olig2, che a sua volta frena Ngn2 e blocca geni neuronali chiave. Disabilitare Olig2 non risolve ogni problema — le efficienze di conversione rimangono moderate — ma aumenta sostanzialmente il rendimento di nuovi neuroni funzionali e sposta il metabolismo e l’espressione genica degli astrociti verso uno stato più simile a quello neuronale. Per il lettore non specialista, la conclusione è che la riparazione cerebrale di successo potrebbe richiedere non solo di accelerare con fattori pro-neuronali, ma anche di rimuovere freni recentemente scoperti come Olig2 che le cellule usano per proteggere la propria identità.
Citazione: Lai, C., Hou, K., Li, W. et al. Olig2 acts as an inducible barrier to in vivo astrocyte-to-neuron conversion. Nat Commun 17, 2033 (2026). https://doi.org/10.1038/s41467-026-68869-4
Parole chiave: conversione da astrociti a neuroni, riprogrammazione cellulare, Olig2, terapia genica, neurorigenerazione