Clear Sky Science · it
Impilamento antiparallelo dei pili Csu guida l'assemblaggio 3D del biofilm di Acinetobacter baumannii
Come i germi ospedalieri costruiscono città protette
Alcuni dei più resistenti germi ospedalieri sopravvivono agli antibiotici nascondendosi in comunità viscide e tridimensionali chiamate biofilm. Questo studio pone una domanda semplice ma cruciale: come si intrecciano i singoli batteri per formare strutture stratificate così robuste? Ingrandendo con microscopi elettronici avanzati, i ricercatori hanno scoperto un «Velcro» microscopico costituito da filamenti simili a capelli che permette al patogeno pericoloso Acinetobacter baumannii di tessersi in ammassi 3D protettivi. Comprendere questo impalcato nascosto potrebbe aprire nuove vie per smantellare i biofilm e rendere più efficaci i farmaci esistenti.
Peli microscopici che tengono insieme i batteri
A. baumannii, una delle principali cause di infezioni ospedaliere difficili da trattare, è ricoperto di sottili peli di superficie chiamati pili Csu. Lavori precedenti avevano dimostrato che questi pili sono essenziali per formare biofilm robusti a cupola, ma non si sapeva come effettivamente intrecciassero le cellule in una struttura 3D. Utilizzando diverse tecniche di microscopia elettronica, gli autori hanno prima confermato che in colture liquide i pili sporgono per lo più singolarmente da ciascun batterio, come aculei di una bardana. Nelle colonie dense cresciute su superfici, però, il quadro cambia drasticamente: molti pili si raggruppano strettamente, formando ampie bande piatte che corrono tra le cellule vicine, creando una rete estesa e dall'aspetto delicato ma strutturalmente complessa in tre dimensioni. 
Scale piatte costruite da filamenti appaiati
Per capire come si formano queste bande, il gruppo ha purificato i pili Csu e osservato il loro comportamento autonomo. Nel giro di giorni o settimane, singoli filamenti cominciavano ad accoppiarsi per poi fondersi in «superimpilamenti» multi-filamento, formando infine una rete gelatinosa che riproduceva da vicino le strutture viste nei biofilm reali. La crio-microscopia elettronica ad alta risoluzione ha rivelato il progetto sottostante. Ogni pilus non è un tubo liscio, ma una asta a zigzag. Quando due aste giacciono affiancate in direzioni opposte, si toccano in punti angolari ripetuti, formando giunzioni laterali stabili. Molte di queste coppie antiparallele possono poi allinearsi in una pila sottilissima a forma di foglio—essenzialmente una scala o un nastro microscopico spesso un solo filamento ma largo molti filamenti.
Una pianta integrata per la crescita 3D
Le strutture dettagliate mostrano che questa capacità di impilamento è incisa nella geometria stessa dei pili. Il motivo a zigzag si ripete su distanze molto brevi, creando numerosi punti di contatto potenziali lungo ciascun filamento. Di conseguenza, una volta che due pili si incontrano nella giusta orientazione, può formarsi una catena di giunzioni come una cerniera, estendendo rapidamente il foglio. È significativo che l'orientamento delle aste favorisca i contatti tra pili provenienti da cellule diverse, non dalla stessa, il che promuove naturalmente il collegamento cellula–cellula. Le pile restano flessibili ed elastiche, così il biofilm in crescita può assorbire sollecitazioni fisiche senza rompersi. I ricercatori hanno osservato che durante la divisione cellulare, le nuove cellule figlie spesso si trovano con i pili posizionati faccia a faccia, condizione che favorisce la formazione delle pile esattamente dove serve per legare le cellule in un ammasso 3D. 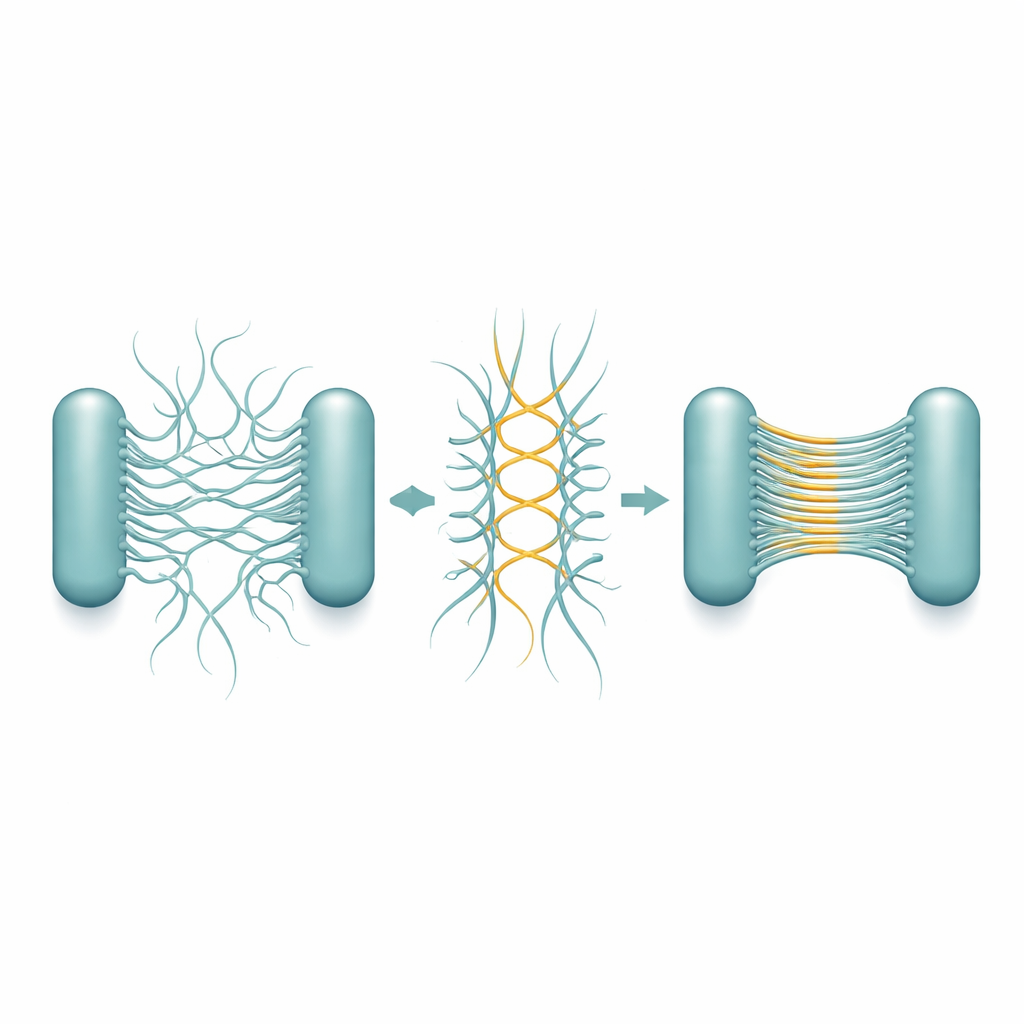
Colla, riempitivo e impalcatura iniziale
Lo studio ha anche esaminato come altri componenti del biofilm contribuiscano alla struttura. Un polimero zuccherino chiamato PNAG e DNA libero proveniente da cellule rotte sono noti per accumularsi nei biofilm maturi. La microscopia ha rivelato queste sostanze a riempire gli spazi stretti tra i batteri e ad avvolgere le pile di pili, molto simili al calcestruzzo versato attorno a barre d'acciaio. Tuttavia, quando il gruppo ha rimosso PNAG e DNA, i batteri hanno comunque formato zattere organizzate tenute insieme solo dagli impilamenti dei pili Csu. Ciò dimostra che i pili costruiscono l'impalcatura primaria, mentre il materiale circostante la cementa e la stabilizza successivamente.
Nuovi punti deboli nelle fortezze batteriche
In termini semplici, questo lavoro spiega come A. baumannii usa i suoi peli di superficie per annodarsi in ammassi resistenti e multilivello che farmaci e cellule immunitarie fanno fatica a penetrare. I pili agiscono prima come uncini per agganciarsi alle superfici e poi come cinghie flessibili che si impilano in fogli piatti, legando le cellule vicine in tutte le direzioni. Polimeri zuccherini e DNA poi riempiono gli spazi, trasformando questa rete di cinghie in una fortezza solida. Identificando il modo preciso in cui i pili aderiscono tra loro, lo studio evidenzia un nuovo bersaglio: farmaci o molecole che bloccano i contatti pilus–pilus potrebbero indebolire l'impalcatura del biofilm dall'interno, rendendo più facile eliminare infezioni batteriche persistenti.
Citazione: Malmi, H., Pakharukova, N., Paul, B. et al. Antiparallel stacking of Csu pili drives Acinetobacter baumannii 3D biofilm assembly. Nat Commun 17, 2508 (2026). https://doi.org/10.1038/s41467-026-68860-z
Parole chiave: biofilm, Acinetobacter baumannii, pili, resistenza agli antibiotici, crio-microscopia elettronica