Clear Sky Science · it
Risposte cGAS-IFN-I estraendo DNA nucleare da cellule in morte tramite nucleocitosi
Come il nostro sistema immunitario legge il DNA dei morti
Quando le nostre cellule muoiono durante infezioni, tumori o per il normale logorio, i loro resti devono essere smaltiti senza provocare troppa infiammazione. Questo articolo rivela un modo sorprendente in cui le cellule immunitarie possono effettivamente penetrare nei nuclei delle cellule morenti, estrarne il DNA e usarlo come segnale di pericolo. Capire questo sistema nascosto di pulizia e allarme potrebbe cambiare il modo in cui pensiamo ai farmaci antivirali, alle malattie autoimmuni, alla terapia del cancro e agli effetti collaterali dei farmaci.
Un allarme del DNA nascosto nelle cellule immunitarie
Le nostre cellule possiedono un sensore chiamato cGAS che riconosce il DNA nel posto sbagliato — che galleggia nel citoplasma invece di essere riposto in sicurezza nel nucleo o nei mitocondri. Quando cGAS incontra questo DNA, attiva un potente programma di allarme che produce interferoni di tipo I, proteine chiave antivirali e regolatrici della risposta immunitaria. Gli scienziati sapevano che i virus possono introdurre il loro materiale genetico nelle cellule per attivare questa via e che frammenti del nostro stesso DNA possono talvolta fuoriuscire e causare malattie autoimmuni. Ma rimaneva un enigma fondamentale: come può una grande quantità del nostro DNA, in particolare quello proveniente da cellule morte, raggiungere cGAS senza essere semplicemente digerita negli “stomaci” cellulari chiamati lisosomi?
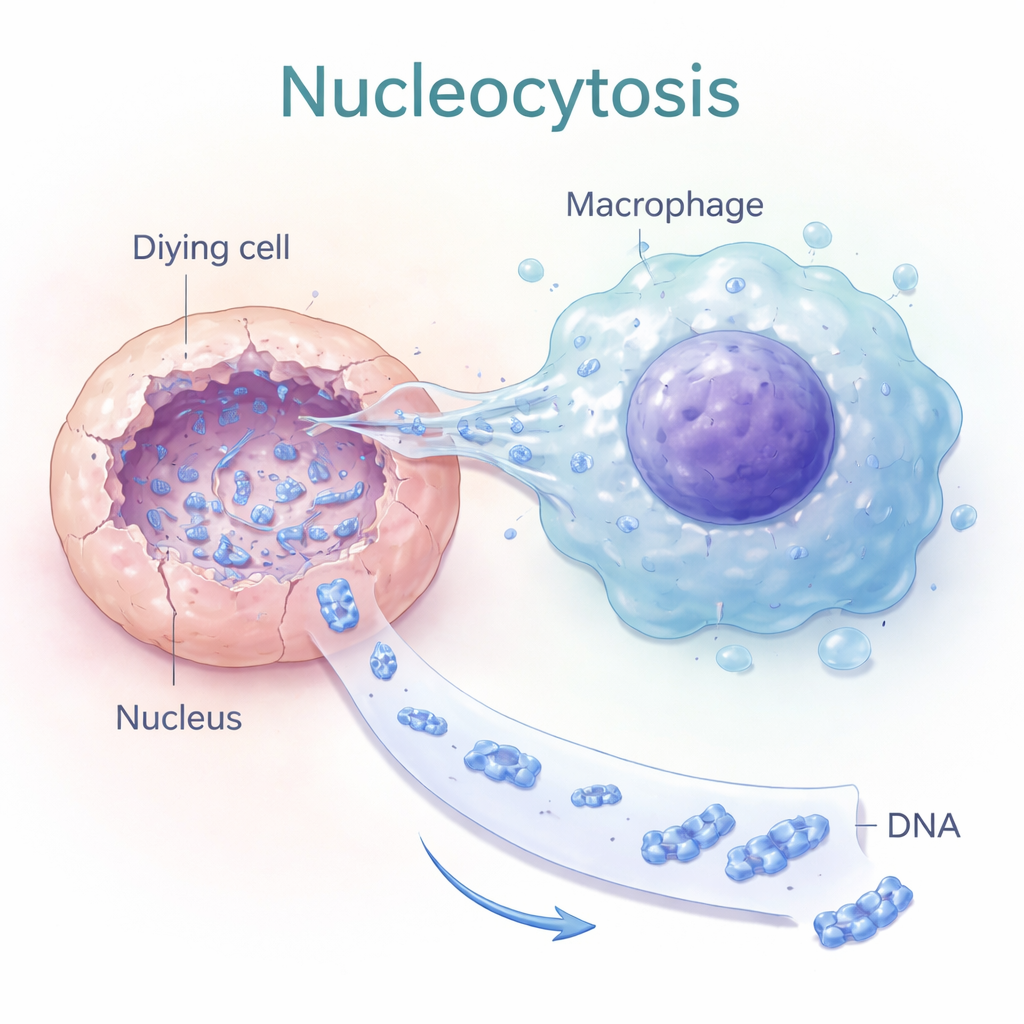
Nucleocitosi: scavare nei nuclei delle cellule morte
Gli autori hanno scoperto un processo che chiamano “nucleocitosi”, in cui alcuni macrofagi — cellule immunitarie che normalmente inglobano i detriti — fanno qualcosa di molto più mirato. Invece di inghiottire l’intera cellula morta, estendono sottili protrusioni simili a dita direttamente nel nucleo della cellula in morte. L’imaging in cellule vive ha mostrato una diminuzione dell’intensità del DNA all’interno del nucleo della cellula morta mentre aumentava all’interno del macrofago adiacente, indicando un’estrazione attiva del DNA nucleare. Questo trasferimento dipendeva dallo scheletro interno della cellula (actina) e da molecole di segnalazione che controllano la forma cellulare, suggerendo che la nucleocitosi sia un comportamento meccanico intenzionale, non una fuoriuscita passiva.
Quando i farmaci antivirali attivano l’allarme del DNA
Durante la pandemia di COVID-19, farmaci come l’idrossiclorochina sono stati ampiamente testati come antivirali, sebbene le loro azioni precise nell’organismo rimanessero poco chiare. I ricercatori hanno trovato che l’idrossiclorochina e diversi farmaci correlati, detti “anfifilici cationici”, possono attivare fortemente la via cGAS–STING–interferone — ma solo in un sottogruppo di macrofagi. Questi farmaci disturbano i lisosomi innalzandone il pH e bloccando un enzima chiamato PPT1, che aiuta a rimuovere gruppi grassi dalle proteine. L’effetto combinato spinge alcune cellule verso una forma speciale di morte in cui una proteina chiamata calreticulina si accumula nel nucleo. I macrofagi quindi tendono a estendere protrusioni verso questi nuclei ricchi di calreticulina, estrarre DNA tramite nucleocitosi e scatenare una intensa produzione di interferone in poche cellule — sufficiente a creare un forte segnale antivirale locale senza inondare l’intero organismo.
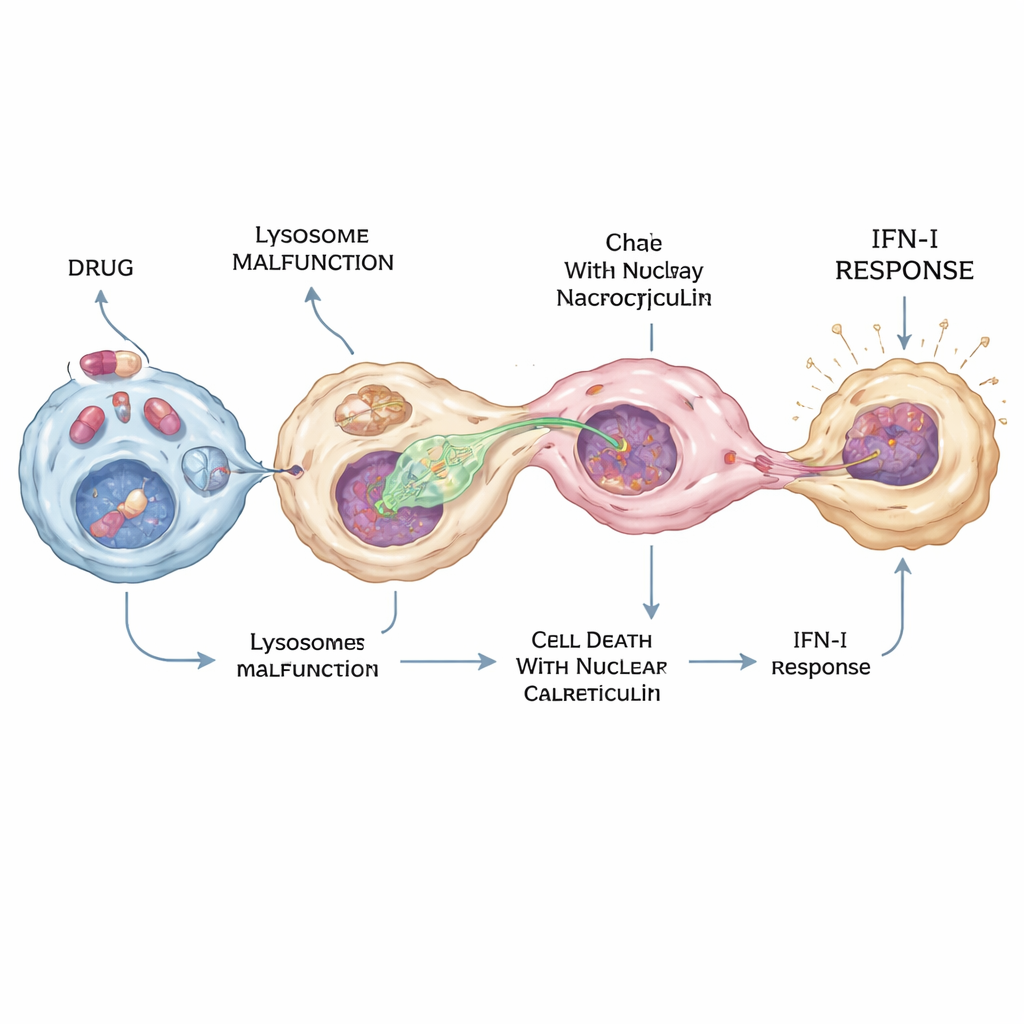
Dalla difesa locale alla malattia e agli effetti collaterali
Studiando sia colture cellulari sia polmoni di topo, il gruppo ha dimostrato che i macrofagi trattati con farmaci possono innescare una risposta interferonica dipendente da STING che rimane per lo più locale — per esempio nel polmone — invece di diventare sistemica. Ciò aiuta a spiegare perché farmaci come l’idrossiclorochina potrebbero mostrare benefici antivirali o antitumorali in alcuni tessuti, ma anche perché possono causare effetti collaterali specifici d’organo come tossicità oculare o cardiaca in uso prolungato. Lo stesso processo di nucleocitosi potrebbe plausibilmente contribuire a malattie autoimmuni o infiammatorie ogni volta che cellule morte e stress lisosomiale coincidono, perché offre un percorso diretto perché il DNA self accenda l’allarme cGAS.
Perché questo conta per i trattamenti futuri
Per un non specialista, il messaggio chiave è che le cellule immunitarie non si limitano a fagocitare passivamente le cellule morte; possono attivamente estrarre DNA dai loro nuclei e usarlo come segnale di aiuto. Questa via di nucleocitosi spiega come il nostro DNA possa attivare in sicurezza potenti difese antivirali in modo mirato e locale, evidenziando al contempo come i farmaci che disturbano i lisosomi o PPT1 possano involontariamente attivare questo interruttore. Imparando a modulare la nucleocitosi — sia aumentando che diminuendo la sua attività, progettando antivirali e terapie oncologiche più intelligenti o evitando segnali di self-DNA indesiderati nelle malattie autoimmuni — i ricercatori sperano di sfruttare questo meccanismo appena scoperto per terapie più sicure e precise.
Citazione: Negishi, H., Wada, Y., Shirasaki, Y. et al. cGAS-IFN-I responses by extracting nuclear DNA from dying cells via nucleocytosis. Nat Commun 17, 1658 (2026). https://doi.org/10.1038/s41467-026-68839-w
Parole chiave: nucleocitosi, cGAS-STING, idrossiclorochina, interferone di tipo I, macrofagi