Clear Sky Science · it
Evoluzione della fotoredox catalisi al manganese a bassa energia luminosa a partire dalla fotocatalisi con luce visibile ad alta energia
Abbassare la luce, mantenere la chimica
Gli chimici spesso impiegano luce intensa e ad alta energia—come lampade blu intense o ultraviolette—per guidare reazioni che costruiscono molecole complesse. Ma questa luce “dura” può sprecare energia, danneggiare porzioni delicate delle molecole ed è difficile da usare in profondità nei tessuti o in reattori di grandi dimensioni. Questo studio mostra come sali di manganese semplici ed economici possano essere assemblati direttamente nella fiasca di reazione per lavorare con luce molto più tenue, rossa e nel vicino infrarosso, pur eseguendo una potente chimica di formazione di legami utile per la scoperta di farmaci e la scienza dei materiali.
Perché la luce più lieve è importante
La luce ad alta energia è un po’ come usare una cannello per accendere una candela: porta a termine il lavoro, ma può anche bruciare tutto ciò che sta intorno. Nelle reazioni chimiche questo può portare a reazioni eccessive, distruzione di gruppi sensibili e scarso controllo. La luce più dolce—in particolare il rosso e il vicino infrarosso, che trasportano meno energia—penetra più in profondità attraverso liquidi e anche tessuti biologici ed è generalmente più compatibile con molecole complesse e fragili. La sfida è che la maggior parte dei catalizzatori guidati dalla luce esistenti è tarata per assorbire luce ad energia più alta, e riprogettarli richiede solitamente sintesi lunghe e complesse. Gli autori si sono posti l’obiettivo di ridurre il “budget di fotoni” di tali reazioni senza dover ricostruire i catalizzatori da zero.
Costruire il catalizzatore sul posto
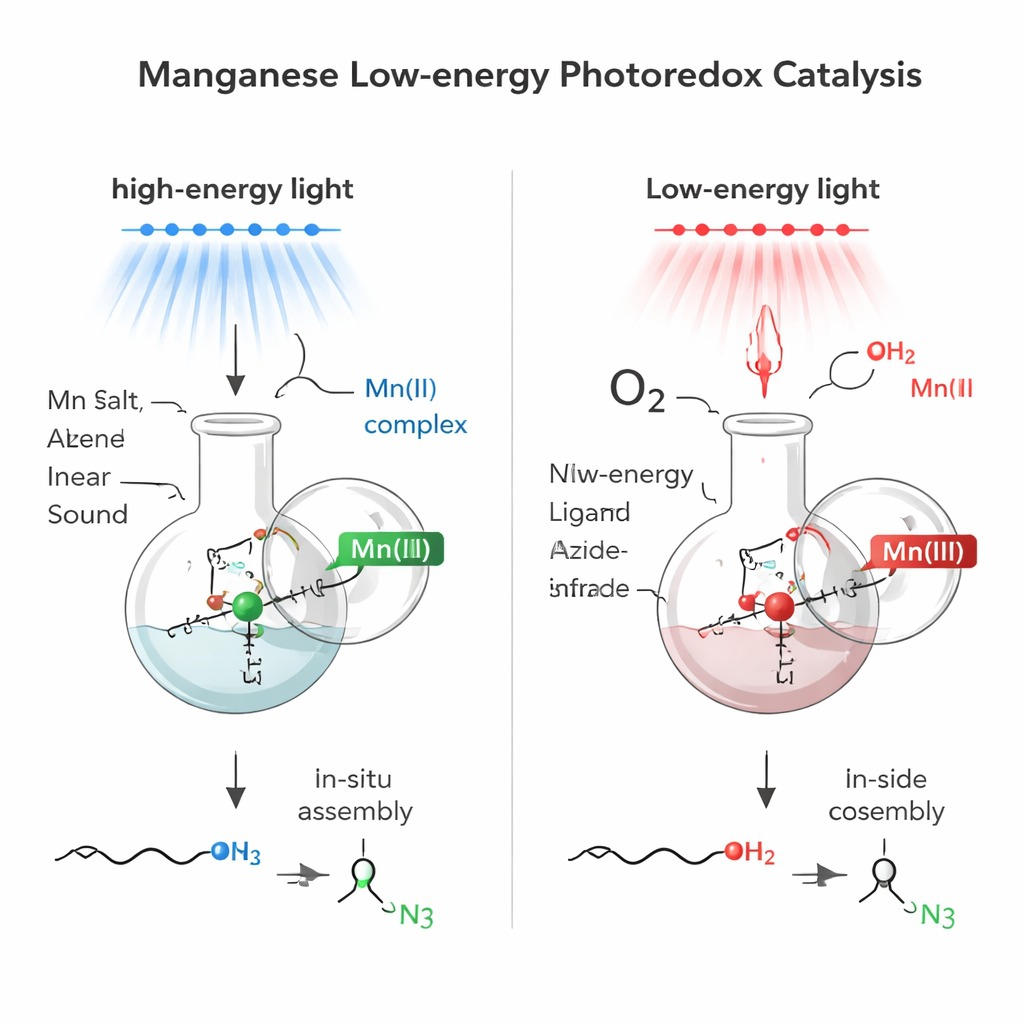
Invece di preparare complessi metallici elaborati in anticipo, il gruppo ha adottato una strategia in-situ: ha semplicemente miscelato sali di manganese commerciali con una piccola molecola ausiliaria (un ligando) e una fonte di azide direttamente nella miscela di reazione. Questo autoassemblaggio ha creato un sistema assorbente basato sul manganese. Con un sale di manganese(II), la miscela assorbiva fortemente la luce blu e poteva generare “radicali azido” a vita breve da un reagente comune chiamato TMSN3. Questi frammenti reattivi si addizionavano poi attraverso doppi legami carbonio‑carbonio semplici (alcheni), inserendo un gruppo azido (N3) all’estremità meno sostituita del doppio legame—uno schema noto come addizione anti‑Markovnikov. Notevolmente, acqua semplice fungeva da sorgente di idrogeno, rendendo il processo sia semplice che efficiente in termini di atomi.
Passare dal blu al rosso profondo
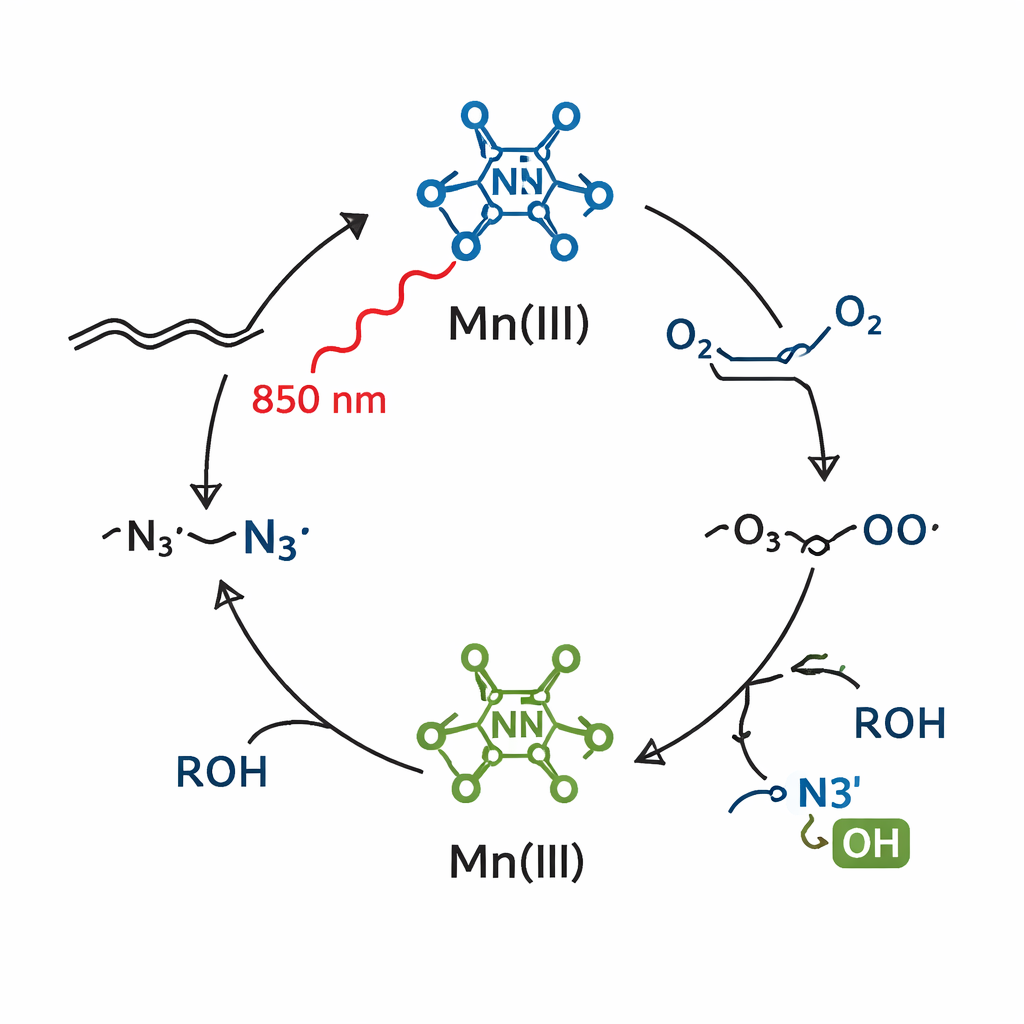
I ricercatori si sono quindi chiesti se un sistema di manganese strettamente correlato potesse funzionare con luce a energia molto più bassa, nella regione del rosso profondo e del vicino infrarosso. Spostandosi dal manganese(II) al manganese(III) e ottimizzando il mezzo di reazione, hanno creato una nuova miscela che assorbiva la luce fino a circa 850 nanometri—ben nel vicino infrarosso. Sotto questa luce delicata, il complesso di manganese(III) produceva ancora radicali azido, ma ora in presenza di aria (come fonte di ossigeno) e di un semplice alcol, la reazione installava in un solo passaggio sia un azido sia un gruppo alcolico attraverso l’alchene. Il risultato è un 2‑azidoalcole (beta‑azidoalcole), un blocco di costruzione particolarmente utile perché contiene due funzionalità estremamente versatili—N3 e OH—su atomi di carbonio adiacenti.
Da alcheni semplici a molecole complesse simili a farmaci
Con entrambi i sistemi, a luce blu e a bassa energia, a disposizione, il gruppo ha testato una vasta gamma di alcheni. Hanno convertito molti materiali di partenza differenti in azidi alchilici o beta‑azidoalcoli con rese da moderate ad elevate, anche quando le molecole portavano gruppi che tipicamente interferiscono con i catalizzatori metallici, come ammine e alcoli non protetti, gruppi contenenti zolfo e sistemi ad anello complessi. Hanno inoltre dimostrato la “funzionalizzazione in fase tardiva” modificando molecole avanzate simili a farmaci, trasformando farmaci esistenti in nuovi derivati con l’aggiunta di azidi e, in alcuni casi, gruppi alcolici. Queste nuove funzioni possono poi essere convertite in altre strutture ricche di azoto o connesse con click chemistry a bersagli biologici, ampliando la cassetta degli attrezzi per la chimica farmaceutica.
Chimica che risparmia energia con promesse pratiche
Il lavoro dimostra che è possibile “evolvere” una reazione a luce blu ad alta energia in un processo a bassa energia nel vicino infrarosso semplicemente cambiando il modo in cui un sale metallico comune si assembla in soluzione. I sistemi di manganese costruiti in situ evitano la sintesi laboriosa di catalizzatori, usano un metallo abbondante e relativamente poco tossico, e possono persino essere alimentati dalla luce solare naturale. Per i non specialisti, il messaggio chiave è che non abbiamo sempre bisogno di luce più dura o di metalli rari e costosi per eseguire chimica impegnativa. Progettando catalizzatori che si formano da pezzi semplici e che rispondono a luce più gentile, questo approccio indica strade verso metodi più efficienti dal punto di vista energetico, scalabili e compatibili con sistemi biologici per creare le molecole complesse su cui dipendono la medicina moderna e i materiali.
Citazione: Yang, W., Song, Y., Yu, X. et al. Evolution of manganese low-energy photoredox catalysis from high-energy visible light photocatalysis. Nat Commun 17, 2062 (2026). https://doi.org/10.1038/s41467-026-68837-y
Parole chiave: fotoredox catalisi, catalisi al manganese, luce a bassa energia, funzionalizzazione degli alcheni, radicali azido