Clear Sky Science · it
Priming versus propagating: effetti immunitari distinti di radiofarmaci emettitori di particelle alfa rispetto a beta in combinazione con l’inibizione dei checkpoint immunitari nei topi
Trasformare la radiazione in un alleato immunitario
I medici oncologi cercano sempre più spesso di reclutare il sistema immunitario per combattere i tumori, ma molte neoplasie continuano a ignorare o resistere a questi farmaci. Questo studio pone una domanda attuale: diversi tipi di radiazione mirata possono essere utilizzati non solo per ridurre direttamente i tumori, ma anche per addestrare il sistema immunitario a fare meglio — e la scelta del radiofarmaco modifica il modo in cui avviene questo addestramento?
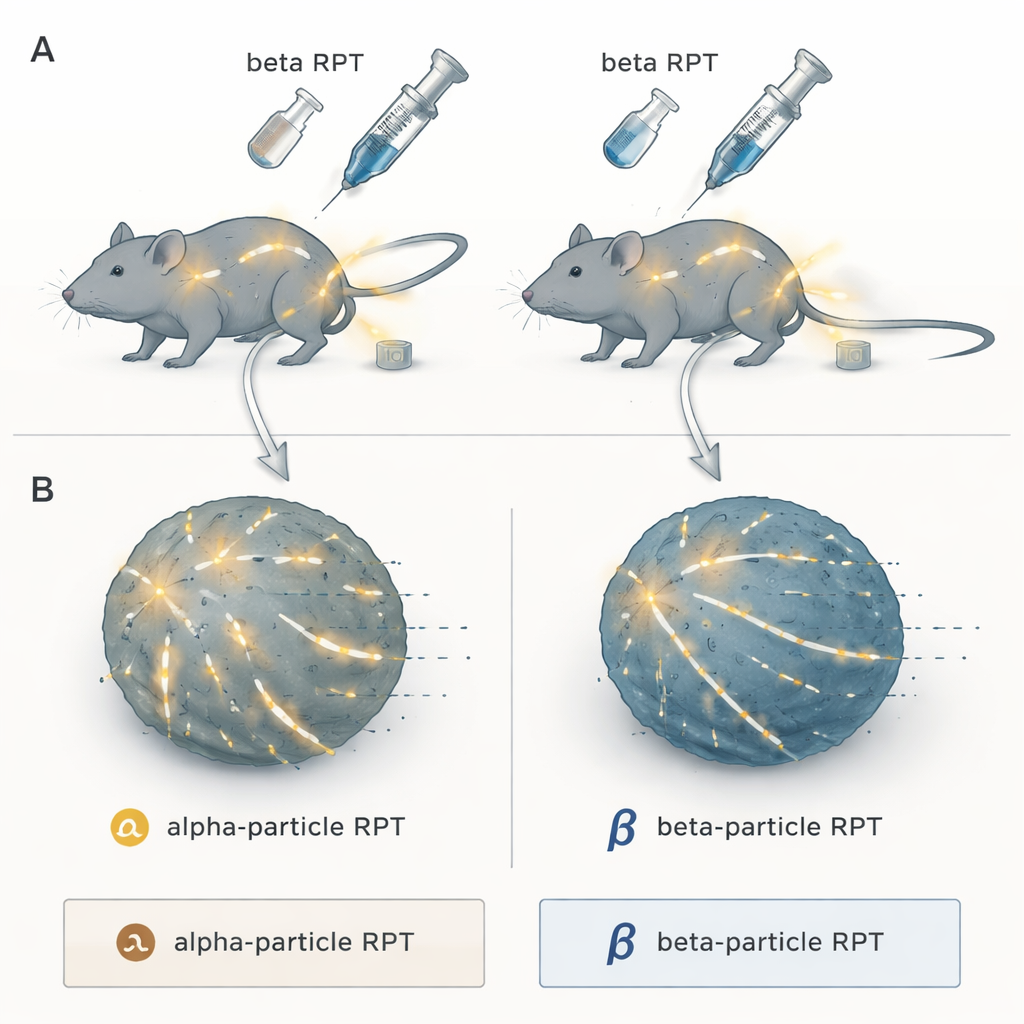
Due sfumature di radiazione di precisione
I ricercatori si sono concentrati sulla terapia con radiofarmaci, un approccio “cerca e distruggi” in cui un carico radioattivo è legato a una molecola che si dirige naturalmente verso i tumori. Una volta iniettato, circola nell’organismo e fornisce radiazione alle sedi tumorali ovunque si nascondano, cosa che la radioterapia esterna convenzionale non può facilmente fare per malattie diffuse. Il team ha confrontato due categorie principali: emettitori di particelle alfa, che rilasciano raffiche di energia estremamente dense su distanze molto brevi, ed emettitori di particelle beta, che emettono radiazione a densità inferiore che si propaga più lontano nei tessuti. Tutti erano legati allo stesso composto che cerca il tumore, NM600, in modo che l’unica differenza fosse il tipo di radiazione — non il bersaglio.
Abbinare la radiazione agli inibitori dei checkpoint immunitari
Da soli, i farmaci inibitori dei checkpoint come anti‑PD‑L1 e anti‑CTLA4 possono togliere i freni alle cellule immunitarie, ma funzionano meglio quando il tumore è già visibile al sistema immunitario. In modelli murini di melanoma, cancro alla prostata e cancro colorettale, gli scienziati hanno somministrato una dose di radiazione attentamente scelta, bassa, ottenuta con NM600 a base alfa o beta, con o senza una combinazione di inibitori dei checkpoint. Hanno anche variato il momento di somministrazione dei farmaci immunitari — prima, subito dopo o molto tempo dopo il trattamento radioattivo — per vedere come il timing influenzasse risultati come crescita tumorale, sopravvivenza e memoria immunitaria a lungo termine.
Quando la radiazione beta funziona: potenziare una risposta esistente
In un modello di cancro colorettale “immune‑hot” che già risponde all’immunoterapia, i migliori risultati sono stati ottenuti con NM600 emettitore beta, soprattutto quando i farmaci immunitari sono stati iniziati precocemente o in un intervallo intermedio di tempo. I tumori si sono ridotti di più, i topi hanno vissuto più a lungo e gli animali guariti spesso hanno respinto lo stesso tumore quando è stato reintrodotto mesi dopo. L’analisi immunologica dettagliata ha mostrato che il trattamento a base beta più il blocco dei checkpoint non tanto ha creato una nuova risposta quanto ha amplificato una risposta già presente: le cellule T citotossiche specifiche per il tumore esistenti si sono espanse, si sono attivate maggiormente e hanno prodotto più segnali d’attacco. In breve, gli emettitori beta sono stati eccellenti nel propagare una risposta immunitaria in corso.
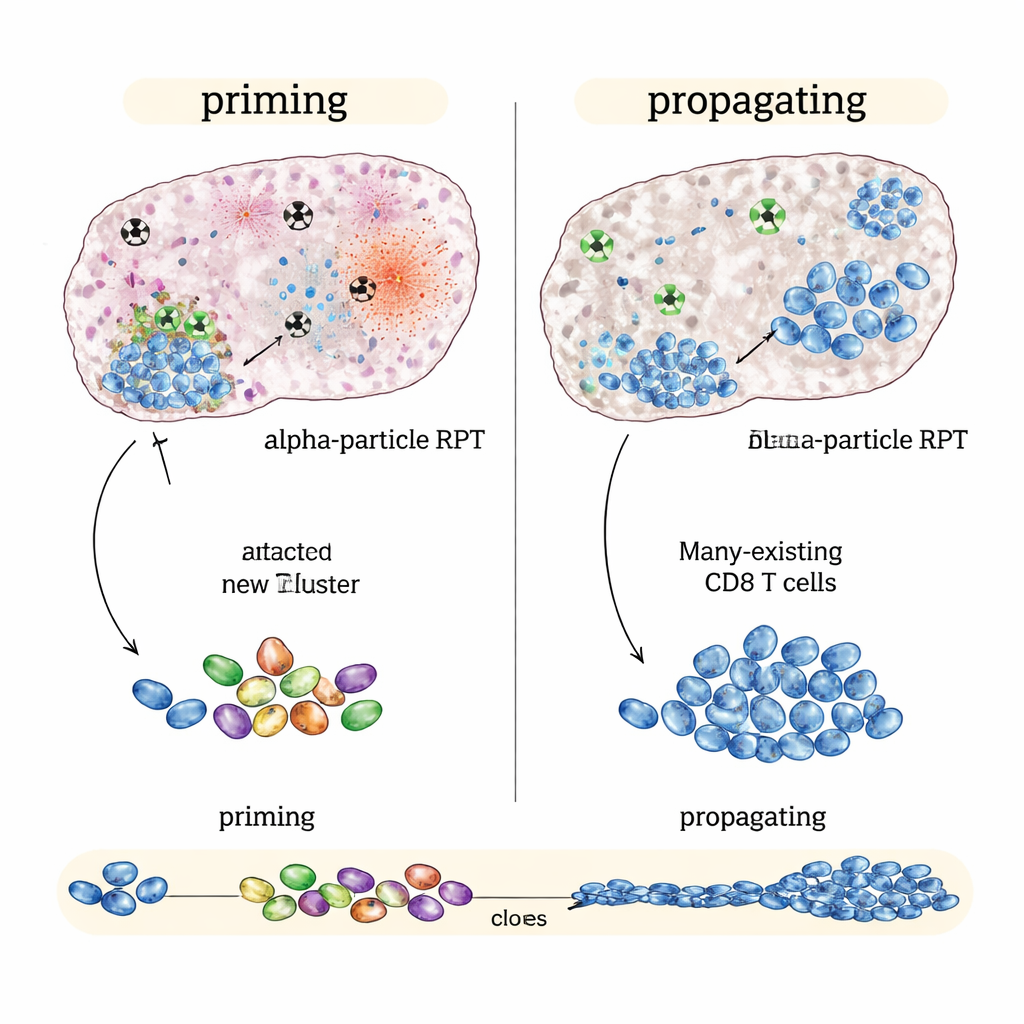
Quando la radiazione alfa funziona: innescare un nuovo attacco immunitario
Al contrario, in tumori “immune‑cold” come un modello di melanoma e uno di cancro alla prostata che rispondono poco ai soli checkpoint, la versione emettitrice alfa ha dato risultati migliori rispetto agli emettitori beta alla stessa dose media tumorale. La terapia a base alfa più i farmaci immunitari ha rallentato maggiormente la crescita tumorale e ha prolungato ulteriormente la sopravvivenza. Analisi genetiche a singola cellula suggeriscono il motivo: la radiazione alfa ha provocato un danno intenso e localizzato che sembrava generare forti segnali di allarme all’interno del tumore salvaguardando le strutture immunitarie vicine. Questo quadro è stato associato a risposte delle cellule T più ampie e diverse e a segnali che indicavano la formazione di nuove cellule T citotossiche in grado di riconoscere il tumore e di collegarsi a cellule della memoria a lunga durata — prove di priming immunitario piuttosto che di semplice amplificazione.
Perché contano il tipo e il momento della radiazione
Nei vari modelli, una somministrazione precoce o a intervallo intermedio degli inibitori dei checkpoint — più o meno coincidente con il picco dei segnali di pericolo indotti dalla radiazione — ha costantemente dato risultati migliori rispetto al trattamento ritardato. Il lavoro suggerisce una regola pratica: nei tumori già visibili al sistema immunitario, radiofarmaci a bassa dose basati su emettitori beta possono essere partner ideali degli inibitori dei checkpoint perché propagano e rafforzano l’immunità esistente. Nei tumori più resistenti dal punto di vista immunitario, emettitori alfa ad alto impatto potrebbero essere più adatti a primare nuove risposte delle cellule T e trasformare un tumore “freddo” in “caldo”. Per i pazienti, questo significa che non tutti i radiofarmaci sono intercambiabili; abbinare l’isotopo e il programma alla personalità immunitaria del tumore potrebbe rendere la radio‑immunoterapia combinata più efficace e più duratura.
Citazione: Kerr, C.P., Jin, W.J., Liu, P. et al. Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice. Nat Commun 17, 2044 (2026). https://doi.org/10.1038/s41467-026-68834-1
Parole chiave: terapia con radiofarmaci, radiazione alfa vs beta, inibitori dei checkpoint immunitari, immunoterapia del cancro, microambiente tumorale