Clear Sky Science · it
Sicurezza e attività biologica di un recettore T bispecifico mirato al Gag di HIV in uomini con HIV: uno studio first‑in‑human
Perché questo nuovo studio sull'HIV è importante
Le persone che convivono con l'HIV oggi possono aspettarsi un’aspettativa di vita pressoché normale grazie alle moderne combinazioni farmacologiche. Ma questi farmaci, chiamati terapia antiretrovirale (ART), non eliminano il virus; lo tengono semplicemente sotto controllo. Rimanono nicchie nascoste di HIV nell’organismo che possono riattivare l’infezione se il trattamento viene interrotto. Questo studio testa un nuovo tipo di immunoterapia di precisione—costruita a partire da un recettore T sintetico—che mira ad addestrare il sistema immunitario a cercare e distruggere in sicurezza quei nascondigli in persone già ben controllate con ART.
Il virus nascosto che non se ne va
Anche quando gli esami del sangue mostrano un virus “non rilevabile”, l’HIV permane sotto forma di materiale genetico nascosto all’interno di cellule a lunga vita, principalmente un tipo di globuli bianchi chiamati cellule T CD4. Queste cellule serbatoio contengono virus silenti ma intatti che possono riattivarsi, costringendo le persone a prendere pillole ogni giorno per tutta la vita. Cancellare completamente ogni cellula infetta è estremamente difficile ed è stato raggiunto soltanto in una manciata di persone sottoposte a trapianti di midollo osseo rischiosi per tumore. Molti ricercatori mirano invece a una “guarigione funzionale”: ridurre il serbatoio a sufficienza perché le difese naturali dell’organismo possano tenere l’HIV sotto controllo senza terapia continua.
Una molecola progettata per reindirizzare le cellule T
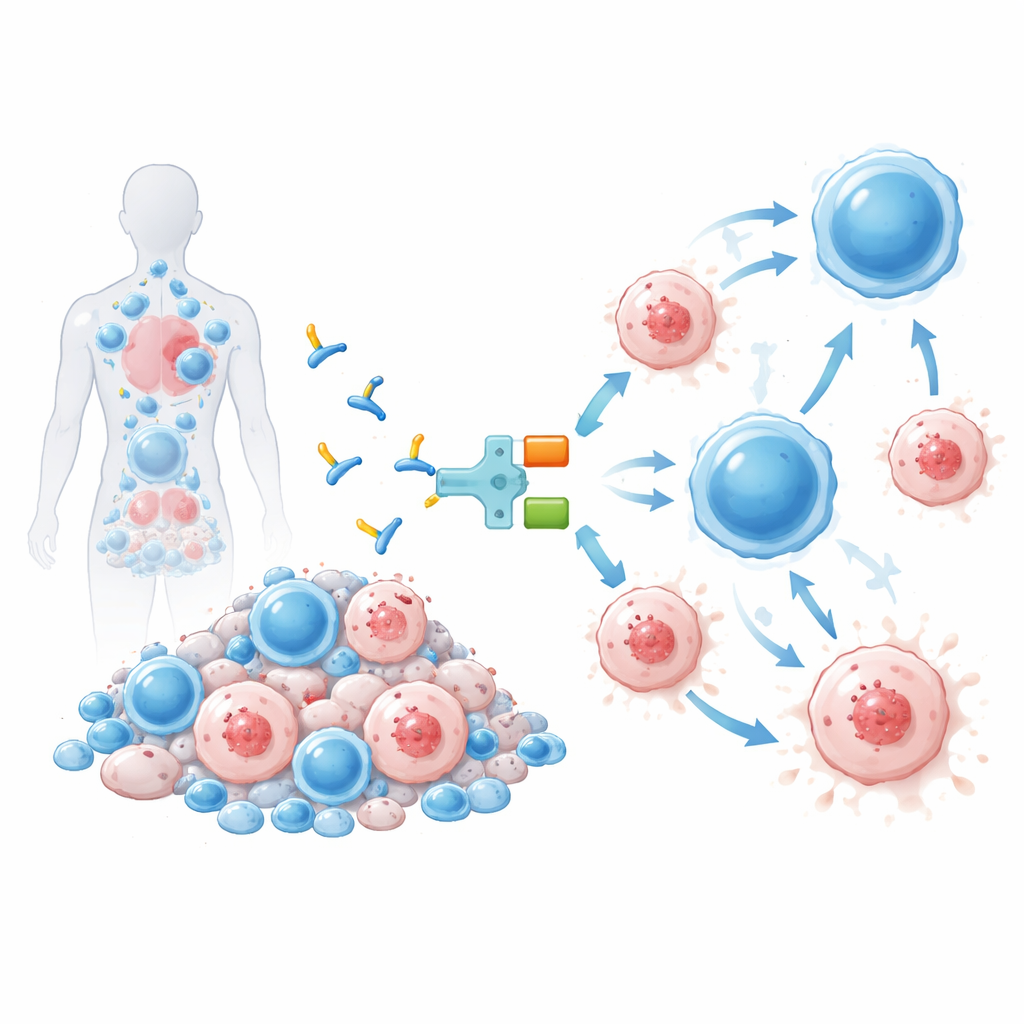
La terapia testata qui, chiamata IMC‑M113V, è una piccola proteina che funziona come un adattatore molecolare tra le cellule infette e il sistema immunitario. Un’estremità di IMC‑M113V è un recettore T ingegnerizzato che riconosce un frammento minuscolo di HIV derivato dalla proteina Gag esposto sulla superficie delle cellule infette nel contesto di un marcatore immunitario comune (HLA‑A*02:01). L’altra estremità si ancora al CD3, una struttura presente su tutte le cellule T. Quando IMC‑M113V si lega a entrambe le estremità contemporaneamente, avvicina le cellule T ordinarie a una cellula infetta da HIV e ne innesca l’eliminazione. Nei test di laboratorio, questa molecola si è dimostrata estremamente sensibile, rilevando solo poche copie del frammento virale sulla superficie di una cellula ed eliminando efficacemente cellule infettate da diverse varianti comuni di HIV, senza mostrare un’attivazione significativa contro un pannello di cellule umane sane.
Primo test in persone con HIV
Per valutare se questo approccio sia sicuro negli esseri umani, i ricercatori hanno condotto uno studio di fase precoce su dodici uomini adulti con HIV nel Regno Unito, in Belgio e in Spagna. Tutti i partecipanti avevano infezione ben controllata con ART, conteggi di CD4 elevati e possedevano il tipo HLA richiesto. Ciascuna persona ha ricevuto una singola dose endovenosa di IMC‑M113V a uno dei tre livelli di dose bassi e poi è stata strettamente monitorata per un mese. L’obiettivo principale a questo stadio era la sicurezza: ricercare effetti collaterali come febbre, infiammazione grave o problemi neurologici, che possono verificarsi con altri potenti farmaci che coinvolgono le cellule T impiegati nel trattamento del cancro.
Cosa hanno osservato i ricercatori in clinica
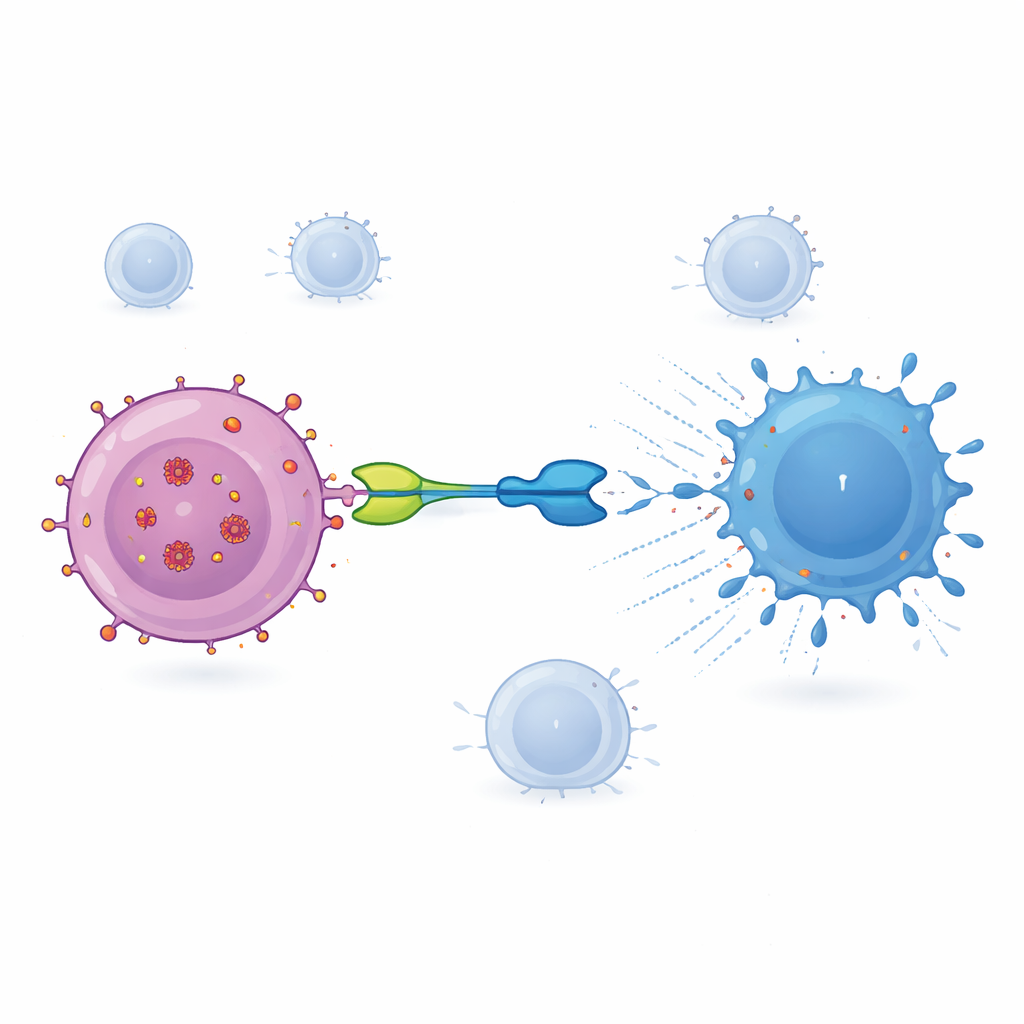
Considerando tutte le dosi, IMC‑M113V è stato generalmente ben tollerato. Metà dei partecipanti ha riportato alcuni effetti collaterali, per lo più lievi come affaticamento o irritazione cutanea, e nessuno ha sviluppato problemi seri come la sindrome da rilascio di citochine o neurotossicità. Gli esami del sangue hanno mostrato che i livelli del farmaco aumentavano e diminuivano nell’arco di circa un giorno, con un’emivita di circa 15–22 ore. Alla dose più alta (15 microgrammi), diversi partecipanti hanno mostrato aumenti temporanei di molecole infiammatorie, in particolare l’interleuchina‑6, e segni che le loro cellule T erano divenute attivate e più capaci di produrre proteine con attività citotossica. Questi cambiamenti immunitari sono stati più marcati nei volontari i cui virus portavano varianti di Gag a cui IMC‑M113V può legarsi in modo particolarmente stretto, suggerendo che il farmaco stava agendo sui bersagli previsti nell’organismo. Tuttavia, dopo una singola dose non si è osservata una riduzione misurabile della dimensione del serbatoio virale nel sangue, valutata tramite RNA virale e DNA virale intatto all’interno delle cellule CD4.
Cosa significa per il futuro del trattamento dell'HIV
Per un lettore non specialista, il messaggio principale è che questo studio fornisce una prima prova di principio importante: una molecola immunitaria «ponte» altamente mirata può essere somministrata in sicurezza a persone con HIV ben controllato e può risvegliare le cellule T perché riconoscano le cellule che ospitano il virus. Non ha curato l’HIV né permesso di interrompere l’ART, ma questo non era l’obiettivo di questo trial first‑in‑human. I risultati supportano la prova di dosi più alte e ripetute, possibilmente in combinazione con farmaci che inducano più cellule infette a rivelarsi, ed estendendo l’approccio ad altri tipi immunitari oltre HLA‑A*02:01. Se studi futuri confermeranno che questa strategia può ridurre in modo affidabile i serbatoi virali senza effetti collaterali pericolosi, potrebbe diventare una componente chiave di terapie combinate mirate a un controllo a lungo termine dell’HIV senza farmaci.
Citazione: Vandekerckhove, L., Fox, J., Mora-Peris, B. et al. Safety and biologic activity of a bispecific T cell receptor targeting HIV Gag in males living with HIV: a first-in-human trial. Nat Commun 17, 2207 (2026). https://doi.org/10.1038/s41467-026-68833-2
Parole chiave: Guarigione dall'HIV, Terapia con cellule T, serbatoio virale, recettore bispecifico, studio clinico