Clear Sky Science · it
Approfondimenti meccanicistici sull’apertura guidata da PCBP1 di i‑motif DNA selezionati al checkpoint G1/S
Piegature del DNA che funzionano come semafori
All’interno delle nostre cellule, il codice genetico è più di una semplice scala diritta di DNA. Parti di esso possono ripiegarsi in forme insolite che agiscono come piccoli interruttori, contribuendo a controllare quando le cellule copiano il loro DNA e si dividono. Questo studio si concentra su una di queste forme, chiamata i‑motif, e su una proteina denominata PCBP1 che può riconoscere e aprire queste strutture proprio mentre la cellula si prepara a replicare il proprio DNA. Comprendere questa interazione fa luce su come le cellule mantengono stabile il loro genoma e su cosa potrebbe andare storto nel cancro.
Strani nodi di DNA in regioni collegate al cancro
La maggior parte delle persone impara che il DNA forma la famosa doppia elica, ma alcuni tratti ricchi della lettera C (per citosina) possono ripiegarsi in un groviglio a quattro filamenti noto come i‑motif. Queste strutture tendono a comparire nelle regioni di controllo di geni che guidano la crescita cellulare, come cMYC e BCL2. Per anni gli scienziati hanno discusso se gli i‑motif si formino davvero nelle cellule viventi, perché sono più facili da osservare in condizioni acide in provetta rispetto alle condizioni quasi neutre dell’organismo. Usando anticorpi specializzati che riconoscono gli i‑motif, lavori recenti, incluso lo studio presente, hanno confermato che essi compaiono nei nuclei cellulari—e spesso si raggruppano vicino a geni chiave per crescita e cancro.
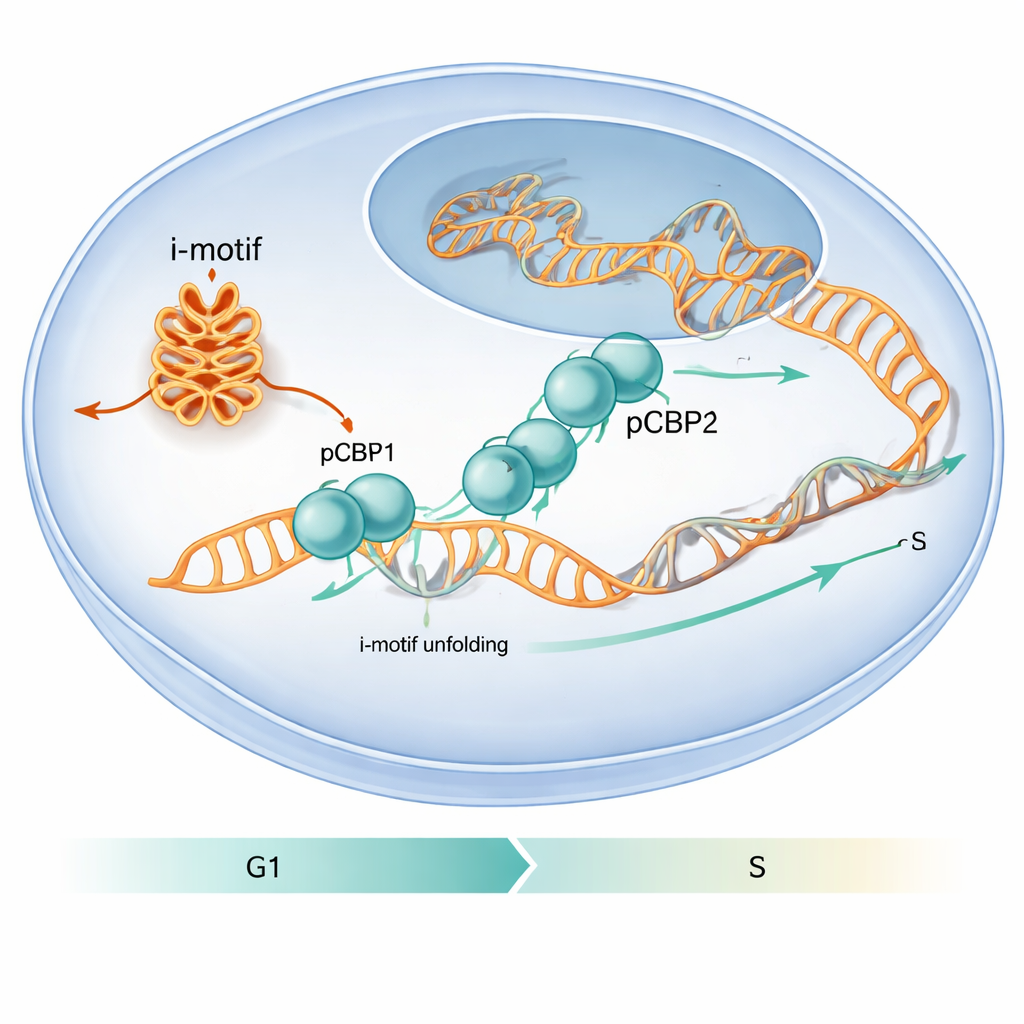
Una proteina che riconosce piegature di DNA speciali
Gli autori hanno cercato di scoprire come le proteine nella cellula gestiscano queste piegature di DNA insolite. Si sono concentrati su PCBP1, una proteina già nota per legare tratti ricchi di C di DNA e RNA e per influenzare il ciclo cellulare. Analizzando mappe genomiche di legame a livello globale esistenti e conducendo esperimenti mirati, hanno scoperto che PCBP1 si trova frequentemente su regioni ricche di C che possono formare i‑motif, specialmente attorno ai siti di inizio dei geni. In esperimenti cellulari su linee tumorali umane, sequenze provenienti dai promotori di cMYC, BCL2 e dalla sequenza ILPR legata all’insulina hanno mostrato sia segnali i‑motif forti sia un elevato occupamento di PCBP1, suggerendo che PCBP1 è un guardiano dedicato di queste strutture.
Come PCBP1 afferra e svolge il groviglio
In saggi in vitro, i ricercatori hanno confrontato quanto bene PCBP1 lega gli i‑motif ripiegati rispetto allo stesso DNA in forma non ripiegata. Hanno regolato l’acidità in modo che il DNA rimanesse o meno ripiegato, mantenendo stabile la proteina. PCBP1 ha sempre preferito l’i‑motif ripiegato, legandolo circa due volte più fortemente rispetto alla stessa sequenza in forma rilassata, e legando solo debolmente forme di DNA non correlate. Una volta legato, PCBP1 poteva attivamente promuovere l’apertura, permettendo alla catena dell’i‑motif di appaiarsi con la sua complementare. Tuttavia, non tutti gli i‑motif si comportavano allo stesso modo: alcuni, come la struttura nel promotore di cMYC, si sono disfatti rapidamente, mentre altri, come quelli in BCL2, hanno resistito e si sono aperti solo lentamente. Caratteristiche aggiuntive come forchette a capuccio nel DNA e il grado di protonazione delle citosine (il carico positivo aggiunto) potevano favorire o ostacolare l’attività di srotolamento di PCBP1.
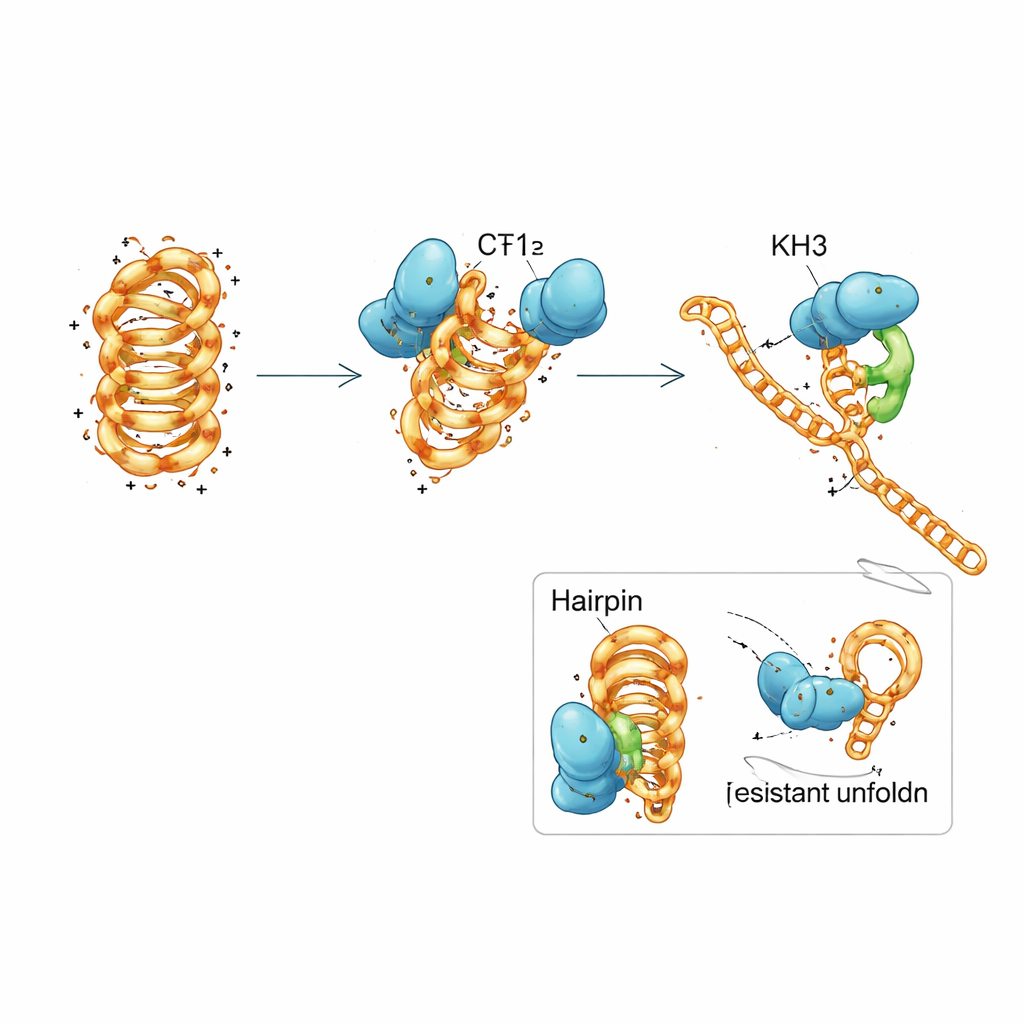
Uno sforzo di squadra all’interno di una singola proteina
PCBP1 è composto da tre moduli ripetuti chiamati domini KH, motivi comuni che afferrano brevi tratti di acidi nucleici. Il gruppo ha sezionato PCBP1 in frammenti e ha scoperto che nessun singolo dominio KH poteva riprodurre completamente il comportamento della proteina intera. I primi due domini insieme potevano legare sia il DNA ripiegato sia quello non ripiegato e spingere l’i‑motif verso una forma meno stabile, ma favorivano l’apertura completa solo lentamente. Il terzo dominio da solo legava a malapena. Quando tutti e tre i domini erano presenti e potevano lavorare insieme, la proteina recuperava la sua forte preferenza per gli i‑motif ripiegati e la sua efficiente capacità di aprirli. Misurazioni biofisiche dettagliate e simulazioni al computer suggeriscono un meccanismo a passi: KH1 e KH2 si posizionano per primi su regioni a loop flessibili dell’i‑motif e interrompono parzialmente paia di basi selezionate, permettendo così a KH3 di ingaggiare e guidare la struttura verso uno stato aperto, pronto per la replicazione.
Mantenere il ciclo cellulare nei tempi giusti
Il lavoro mostra anche che questa danza molecolare ha rilevanza per il comportamento cellulare. Quando i ricercatori hanno ridotto i livelli di PCBP1 in cellule umane, sono comparse più strutture i‑motif in specifici promotori genici, sono aumentati i marcatori di danno al DNA e le cellule si sono arrestate al critico checkpoint G1/S—il momento subito prima che inizi la replicazione del DNA. In condizioni normali, la presenza di PCBP1 nelle regioni capaci di formare i‑motif raggiunge il picco intorno a questo checkpoint, poi diminuisce all’inizio della fase S quando gli i‑motif vengono risolti. Questo timing suggerisce che PCBP1 funzioni da custode: si lega e apre particolari i‑motif al momento giusto affinché la replicazione del DNA possa procedere senza intoppi e il genoma resti intatto. Per il lettore non specialista, il messaggio è che le piegature insolite del DNA possono comportarsi come ostacoli temporanei, e PCBP1 è uno degli strumenti specializzati che la cellula usa per rimuoverli, contribuendo a prevenire errori che altrimenti potrebbero favorire il cancro.
Citazione: Sengupta, P., Gillet, N., Obi, I. et al. Mechanistic insights into PCBP1-driven unfolding of selected i-motif DNA at G1/S checkpoint. Nat Commun 17, 1149 (2026). https://doi.org/10.1038/s41467-026-68822-5
Parole chiave: i-motif DNA, proteina PCBP1, checkpoint del ciclo cellulare, stabilità del genoma, struttura secondaria del DNA