Clear Sky Science · it
La trascrittomica single-cell guidata dalla chimica rivela il rimodellamento dello scheletro mediato da sulfotransferasi nella biosintesi della securinina
Perché conta la chimica di un arbusto
Gli alcaloidi securinega sono molecole potenti presenti in un piccolo arbusto ornamentale, Flueggea suffruticosa, studiato da tempo per potenziali terapie contro il cancro e le malattie neurologiche. Tuttavia, fino a oggi, non si sapeva veramente come questa pianta costruisca questi composti così complessi. Questo studio combina la moderna lettura genica cellula per cellula con esperimenti chimici ingegnosi per rivelare, passo dopo passo, come la pianta assembla e rimodella queste molecole — e scopre lungo il percorso un nuovo, sorprendente ruolo per un tipo comune di enzima. 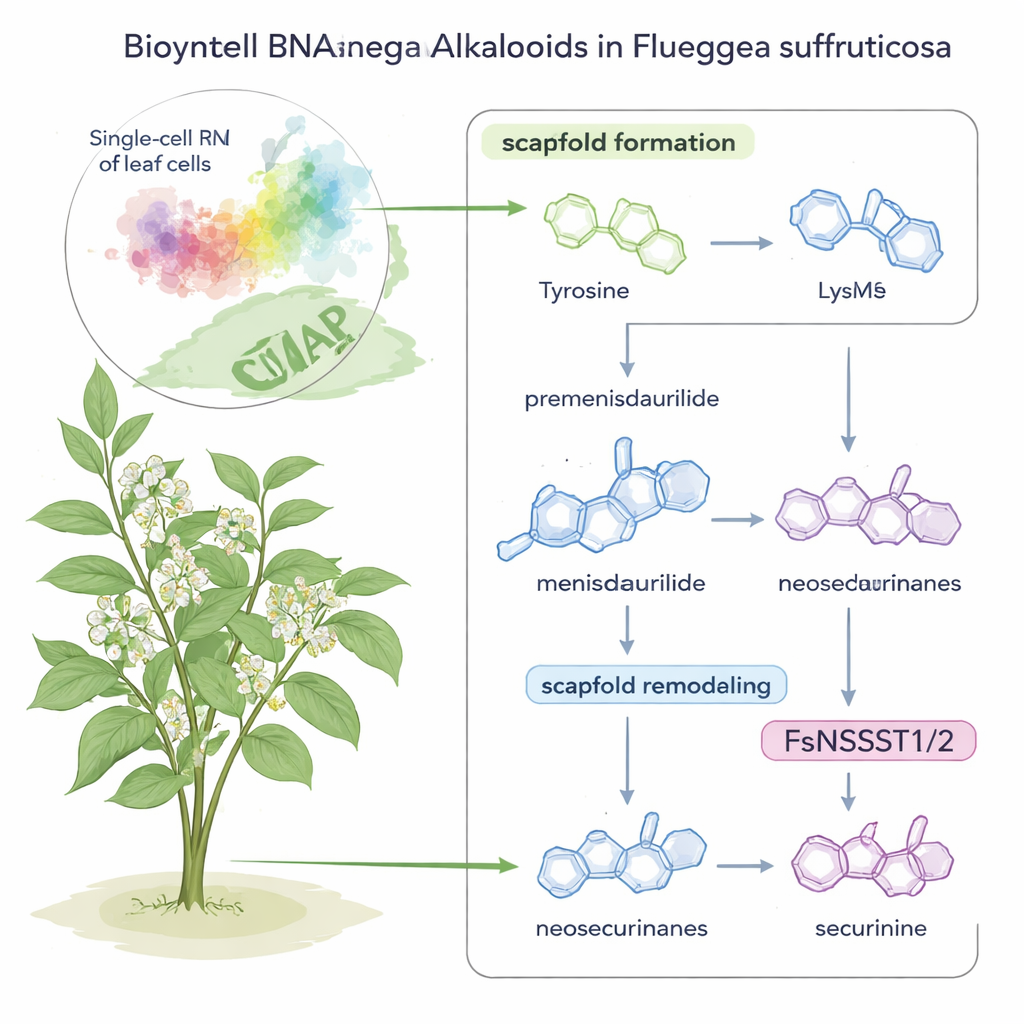
Mattoni di partenza da amminoacidi comuni
La storia inizia con due nutrienti familiari: gli amminoacidi tirosina e lisina. In F. suffruticosa, la tirosina viene trasformata in una singolare molecola ciclica chiamata premenisdaurilide, che viene poi ridotta a menisdaurilide da un enzima di nuova scoperta che gli autori chiamano FsMS (per “menisdaurilide synthase”). Parallelamente, la lisina è convertita in un piccolo anello contenente azoto chiamato 1-piperideina da un altro enzima, FsPS, scoperto in lavori precedenti. Quando menisdaurilide e 1-piperideina si incontrano in condizioni leggermente basiche e acquose, si fondono spontaneamente per formare alcaloidi “neosecurinane” — strutture intermedie sulla strada verso i composti medicinali finali.
Osservare la chimica in tempo reale
Per dimostrare che questi passaggi proposti non sono solo teorici, il gruppo ha sintetizzato versioni degli intermedi sospetti marcate con atomi di carbonio pesante. Somministrando queste molecole etichettate ad estratti della pianta, gli scienziati hanno potuto tracciare esattamente dove finivano gli atomi. Hanno osservato la conversione del menisdaurilide etichettato in neosecurinane etichettati, e poi in noti alcaloidi come allosecurinine e securinine, confermando che questi intermedi esistono realmente lungo la via naturale. È importante che alcune delle reazioni chiave di formazione degli anelli siano avvenute anche in estratti portati a ebollizione, mostrando che parti del percorso possono procedere senza enzimi, guidate semplicemente dalla chimica intrinseca delle molecole stesse.
Concentrarsi sulle cellule giuste
Sapere quali molecole compaiono dove è solo metà del rompicapo; identificare i geni che controllano ogni passaggio richiede sapere quali cellule svolgono il lavoro. I ricercatori hanno sequenziato l’RNA di migliaia di singole cellule prelevate dalle foglie di F. suffruticosa, raggruppandole in tipi cellulari distinti in base ai modelli di espressione genica. Un cluster, associato alle vene fogliari, è emerso in modo particolare: esprimeva fortemente i geni noti della via e molti enzimi collegati al metabolismo di tirosina, lisina e zolfo. Esaminando quali geni variavano in sincronia con gli enzimi della via all’interno di questo cluster, il team ha individuato FsMS e due sulfotransferasi, FsNSST1 e FsNSST2, come candidati principali per i passaggi mancanti. 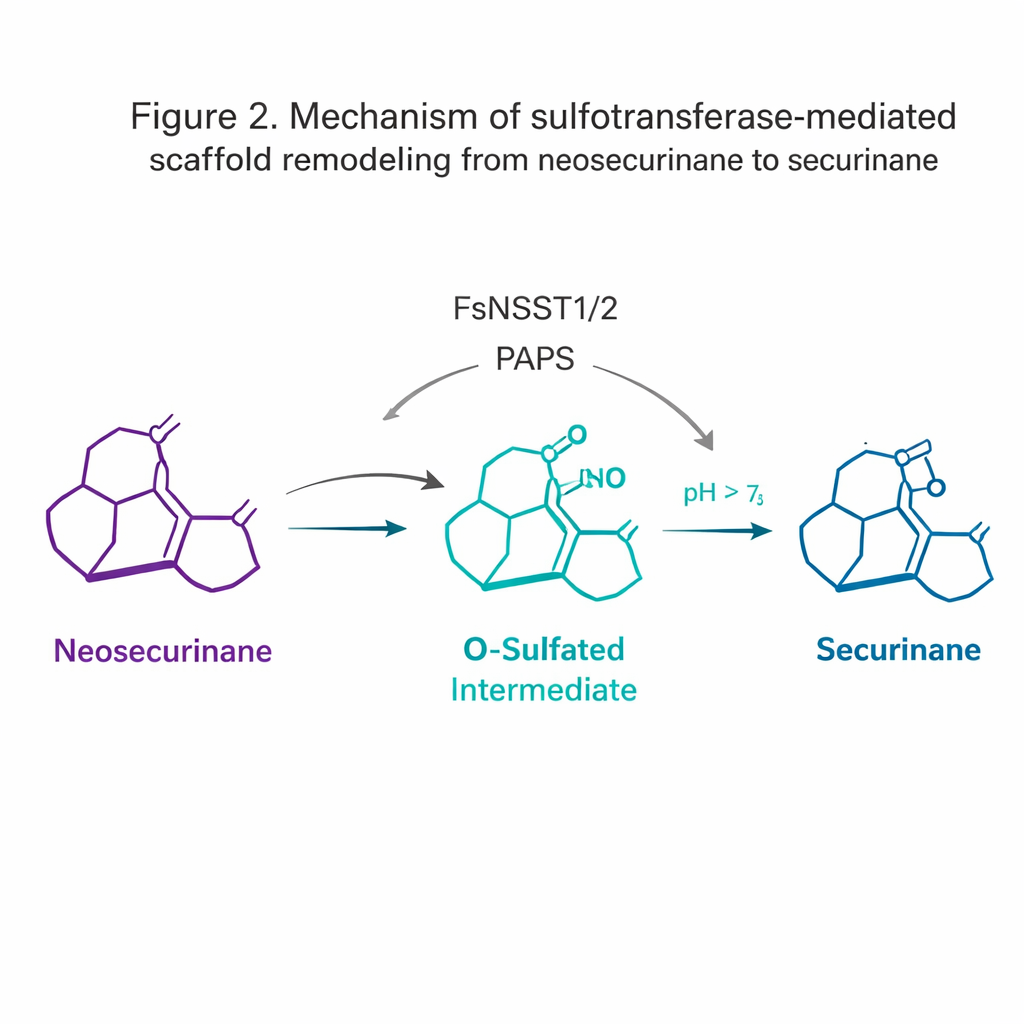
Un enzima che rimodella lo scheletro molecolare
La scoperta più sorprendente è venuta dalle sulfotransferasi. Le sulfotransferasi di solito aggiungono un gruppo solfato alle molecole per migliorarne la solubilità o segnarle per la degradazione. Qui, FsNSST1 e FsNSST2 agiscono invece da interruttori: legano un solfato allo scheletro neosecurinane, trasformandolo temporaneamente in un intermedio ad alta energia “O-solfatato”. Questa forma attivata subisce quindi uno spostamento amminico 1,2 spontaneo — un piccolo riarrangiamento in cui un atomo di azoto migra — convertendo l’impalcatura biciclica [2.2.2] del “neosecurinane” nell’impalcatura [3.2.1] del “securinane”. Questo sottile rimodellamento è ciò che dà origine al distintivo nucleo tetraciclico degli alcaloidi biologicamente attivi.
Perché questa via è importante
Per un non specialista, il messaggio chiave è che la pianta assembla gli alcaloidi securinega in due fasi principali: prima costruisce un sistema ad anello preliminare a partire da amminoacidi comuni; poi rimodella chimicamente quello scheletro in una forma più complessa usando un “innesco” solfato. Combinando il profilo genico cellula per cellula con la chimica a isotopi marcati, gli autori mappano in dettaglio questa via e rivelano che le sulfotransferasi — enzimi presenti in tutte le forme di vita — possono fare più che decorare le molecole; possono innescare riarrangiamenti profondi della loro forma. Comprendere questa via non solo chiarisce come una promettente classe di molecole simili a farmaci è prodotta in natura, ma apre anche la strada all’ingegnerizzazione di colture o microrganismi per produrre nuovi medicinali ispirati alle securinega.
Citazione: Choung, S., Kang, G., Kim, T. et al. Chemically guided single-cell transcriptomics reveals sulfotransferase-mediated scaffold remodeling in securinine biosynthesis. Nat Commun 17, 1954 (2026). https://doi.org/10.1038/s41467-026-68816-3
Parole chiave: alcaloidi vegetali, biosintesi, trascrittomica single-cell, sulfotransferasi, chimica dei prodotti naturali