Clear Sky Science · it
La metilazione del tRNA dipendente da ALKB-1 è necessaria per l’eliminazione efficiente dei mitocondri paterni
Perché i mitocondri dei padri scompaiono silenziosamente
Ogni essere umano, il verme e la maggior parte degli altri animali ereditano le loro centrali cellulari—i mitocondri—quasi interamente dalla madre. I mitocondri paterni entrano nell’uovo insieme allo spermatozoo ma vengono rapidamente rimossi, una pulizia biologica che aiuta a prevenire il passaggio di DNA mitocondriale danneggiato. Questo studio in piccoli nematodi rivela un «controllo di stress» molecolare che contribuisce a decidere se i mitocondri paterni vengono eliminati in modo efficiente, offrendo indizi che un giorno potrebbero collegarsi ad alcuni casi di infertilità e a malattie mitocondriali.
Le fabbriche di energia che ereditiamo da mamma
I mitocondri generano l’energia che mantiene vive le cellule e possiedono un piccolo anello di DNA proprio. Nel corso della vita questo DNA mitocondriale può accumulare mutazioni dannose. Se entrambi i genitori trasmettessero regolarmente i loro mitocondri, questi difetti potrebbero mescolarsi e accumularsi nelle generazioni successive. Per evitarlo, la maggior parte degli animali si affida all’ereditarietà materna: l’embrione conserva i mitocondri della madre ed elimina quasi del tutto quelli del padre poco dopo la fecondazione. Sebbene siano note diverse vie di smaltimento—come i sistemi di riciclo cellulare e gli enzimi che tagliano il DNA—gli scienziati non avevano ancora compreso appieno come segni chimici sottili su DNA e RNA possano influenzare questa eliminazione dei mitocondri paterni.
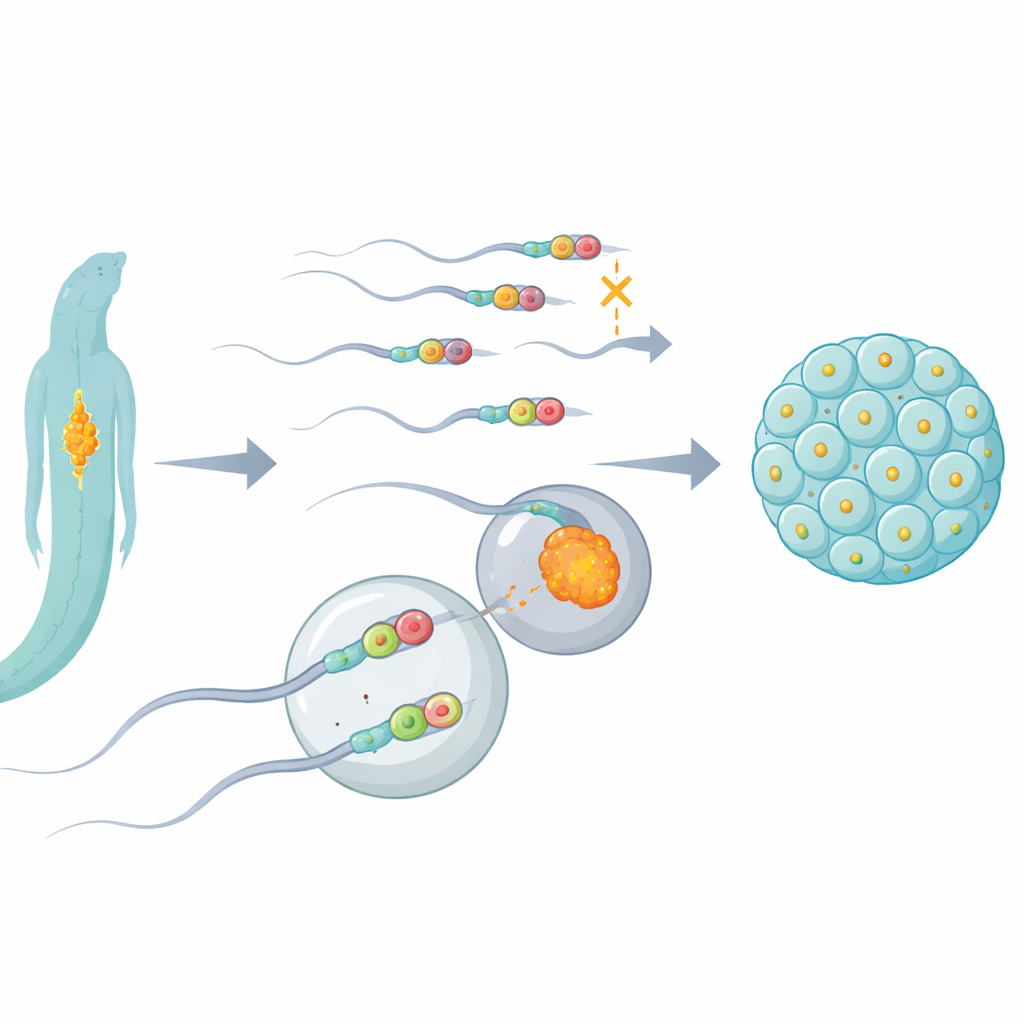
Una cancellatrice molecolare con un ruolo chiave nella riproduzione
I ricercatori si sono concentrati su una proteina chiamata ALKB-1 nel nematode Caenorhabditis elegans, un organismo molto usato in genetica. ALKB-1 è una specie di cancellatrice molecolare che può rimuovere gruppi metilici—piccoli segni chimici—da DNA e RNA. Disabilitando selettivamente ALKB-1 o riducendone i livelli, il gruppo ha seguito che cosa succedeva ai mitocondri spermatici e al loro DNA dopo la fecondazione. Hanno scoperto che quando l’attività «cancellatrice» di ALKB-1 veniva persa, i mitocondri paterni e il loro DNA persistevano in modo anormale negli embrioni in sviluppo, invece di essere rapidamente eliminati. Questo ritardo si osservava soprattutto quando ALKB-1 mancava negli spermatozoi, e si accompagnava a spermatozoi contenenti un numero insolitamente elevato di mitocondri e DNA mitocondriale.
Come modificare la chimica del tRNA sconvolge i mitocondri
Approfondendo, gli scienziati hanno cercato di capire quali segni chimici fossero davvero importanti per ALKB-1. I test sul DNA suggerivano che le sole modifiche della metilazione del DNA non potevano spiegare il problema di eliminazione. L’attenzione si è quindi spostata sui tRNA, piccole molecole adattatrici che aiutano a tradurre i messaggi genetici in proteine. Nei vermi normali, ALKB-1 rimuove un marchio specifico—chiamato m1A—da un sottoinsieme di tRNA. In assenza di ALKB-1, questi marchi si accumulavano. Questo cambiamento sottile nella chimica del tRNA alterava in modo diffuso l’efficienza della produzione di molte proteine: la sintesi proteica nel fluido cellulare aumentava, mentre la sintesi all’interno dei mitocondri rallentava. Il risultato era una discrepanza tra le proteine destinate ai mitocondri e la capacità degli organelli di gestirle, portando a aggregati di proteine mal gestite e a segnali di stress mitocondriale.
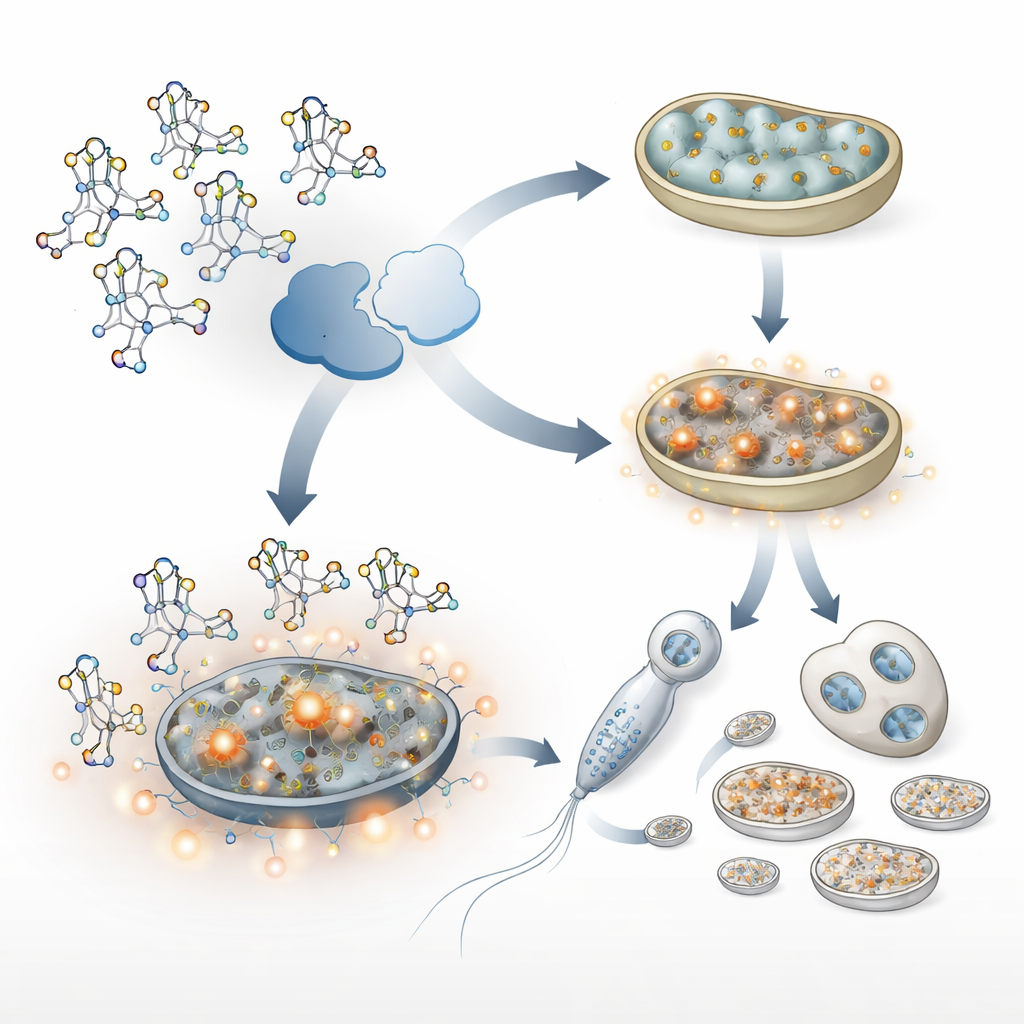
Segnali di stress che proteggono—e involontariamente preservano—i mitocondri paterni
I mitocondri sotto stress spesso producono più specie reattive dell’ossigeno, sottoprodotti chimicamente aggressivi del metabolismo. Nei vermi privi di ALKB-1 queste molecole reattive aumentavano notevolmente. Ciò, a sua volta, attivava due programmi chiave di risposta allo stress: uno mediato da un fattore simile al Nrf2 umano (chiamato SKN-1 nei vermi) e un altro noto come risposta alle proteine mitocondriali non ripiegate. Insieme, queste vie aumentavano la produzione di nuovi mitocondri e la copia del DNA mitocondriale, in particolare negli spermatozoi. Pur aiutando le cellule a fronteggiare il danno, questa risposta aveva anche un effetto collaterale involontario: si accumulavano più mitocondri paterni e più DNA mitocondriale, che risultavano più difficili da eliminare dopo la fecondazione. Bloccare queste vie di stress o ridurre il danno ossidativo con antiossidanti ripristinava una rimozione più normale dei mitocondri paterni.
Quando la pulizia fallisce, ne soffrono fertilità ed embrioni
Il ritardo nell’eliminazione dei mitocondri paterni non era solo una curiosità microscopica. I vermi maschi privi della normale attività di ALKB-1 generavano meno discendenti, e gli embrioni che contribuivano a formare morivano più spesso. Tuttavia i loro spermatozoi si formavano in numero normale e apparivano strutturalmente integri, suggerendo che il problema principale fosse nel controllo di qualità mitocondriale più che nella produzione degli spermatozoi. Lo studio propone che i marchi sui tRNA controllati da ALKB-1 agiscano come un checkpoint epigenetico: quando questo sistema funziona, l’equilibrio delle proteine mitocondriali è mantenuto, lo stress è contenuto e i mitocondri paterni vengono eliminati in sicurezza. Quando fallisce, mitocondri paterni stressati e sovrabbondanti persistono, danneggiando fertilità e sviluppo precoce. Sebbene questi esperimenti siano stati condotti nei vermi, illuminano un principio fondamentale—che piccole modifiche chimiche all’RNA possono indirizzare come ereditiamo le nostre centrali cellulari e, infine, influenzare la salute riproduttiva in animali più complessi, compresi gli esseri umani.
Citazione: Luo, Z., Li, Y., He, C. et al. ALKB-1-dependent tRNA methylation is required for efficient paternal mitochondrial elimination. Nat Commun 17, 2144 (2026). https://doi.org/10.1038/s41467-026-68813-6
Parole chiave: ereditarietà mitocondriale, mitocondri paterni, metilazione del tRNA, stress ossidativo, fertilità maschile