Clear Sky Science · it
Un atlante di quantificazione assoluta degli RNA non codificanti di piccole dimensioni attraverso diversi tessuti e linee cellulari di mammiferi
Perché le molecole di RNA piccole sono importanti
All'interno di ogni cellula, flotte di minuscole molecole di RNA contribuiscono a decidere quali geni vengono accesi o spenti. Questi piccoli RNA non codificanti funzionano come dimmer per i nostri programmi genetici, modellando lo sviluppo, la funzione degli organi e le malattie. Eppure, nonostante le potenti tecnologie di sequenziamento, gli scienziati hanno faticato a misurare con precisione quante di queste molecole siano presenti in diversi tipi cellulari e tessuti. Questo studio introduce un metodo più accurato per contarle e costruisce un atlante dettagliato che mostra la loro reale abbondanza in numerosi tessuti di mammiferi e in linee cellulari di laboratorio comuni.
Un modo più chiaro per contare i piccoli RNA
I metodi tradizionali per il sequenziamento dei piccoli RNA si basano su enzimi che aggiungono adattatori prima della lettura delle molecole. Quegli enzimi preferiscono certe conformazioni e terminazioni chimiche, perciò alcuni RNA vengono catturati in modo efficiente mentre altri sono persi o sottostimati. Questo bias è particolarmente grave per classi specifiche come le piRNA e i piccoli RNA delle piante, che portano cappucci chimici protettivi alle estremità. Gli autori hanno creato un nuovo protocollo, chiamato 4NBoost, che riprogetta gli adattatori e le condizioni di reazione per uniformare queste preferenze e aggiunge codici a barre molecolari integrati per distinguere le molecole vere dalle copie generate durante l'amplificazione.
Trasformare un protocollo in uno strumento di misura
Per trasformare 4NBoost da un semplice valore relativo a uno strumento di misura reale, il team ha aggiunto RNA sintetici “spike‑in” progettati con cura a concentrazioni note che coprono un intervallo molto ampio. Confrontando quante volte ciascun spike‑in è stato letto dal sequenziatore con quanto ne era stato originariamente aggiunto, hanno costruito curve standard che convertono i conteggi di lettura in numeri assoluti di molecole. Test con differenti miscele di spike‑in e RNA di controllo hanno dimostrato che 4NBoost può tracciare l'abbondanza con precisione su diversi ordini di grandezza, includendo anche RNA con modifiche chimiche problematiche. Anche partendo da appena un nanogrammo di RNA totale, il metodo catturava fedelmente il profilo dei piccoli RNA.
Costruire un atlante attraverso tessuti e linee cellulari
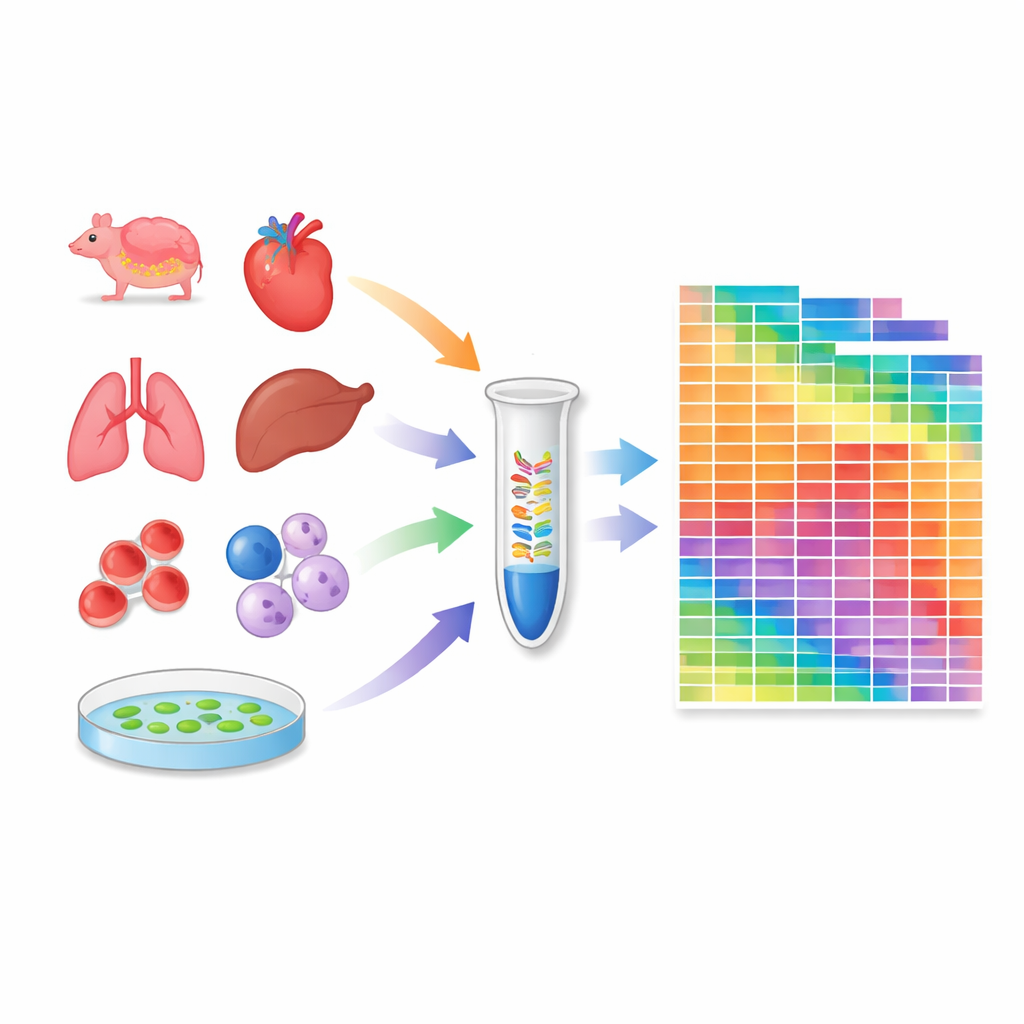
Con questo protocollo calibrato, i ricercatori hanno profilato 259 campioni: 20 tessuti da topi, 18 da macachi crab‑eating, 24 linee cellulari umane e murine ampiamente usate e diversi tessuti della pianta modello Arabidopsis. Per ogni campione hanno stimato il numero assoluto di molecole per migliaia di microRNA e piRNA. Ciò ha rivelato quante diverse specie di microRNA sono presenti in ciascun contesto e come i loro quantitativi totali variano tra tessuti e specie. Alcune linee cellulari e organi presentano repertori di microRNA particolarmente ricchi, mentre altri, come le cellule del sangue, sono dominati da poche specie altamente abbondanti. L'atlante ha inoltre evidenziato differenze sostanziali tra tessuti di topo e di scimmia, sottolineando che la regolazione mediante piccoli RNA può essere specifica per specie.
Correggere i dati precedenti e rivedere le assunzioni comuni
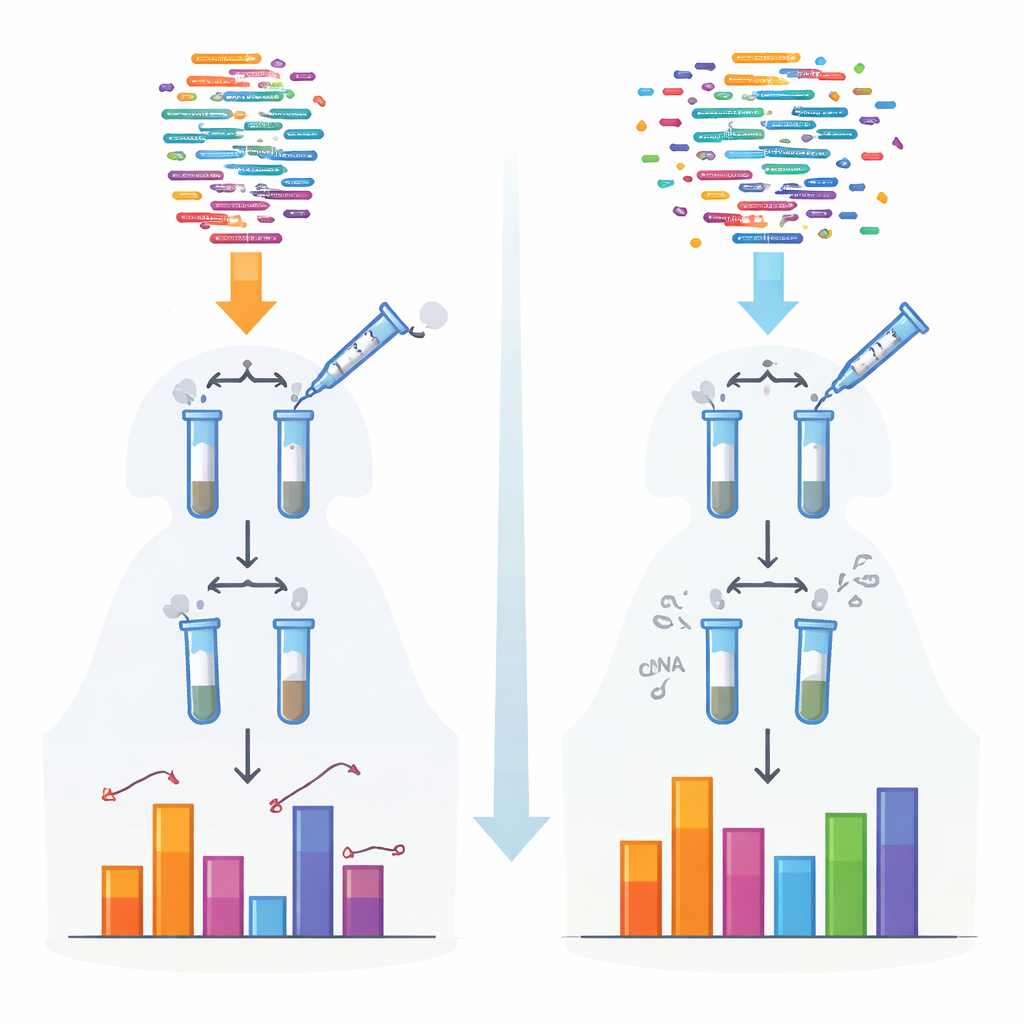
Quando il nuovo atlante è stato confrontato con banche dati di piccoli RNA costruite con metodi convenzionali, sono emerse incongruenze sorprendenti. Diverse famiglie di microRNA importanti — come miR‑19 e miR‑29 — sono risultate molto più abbondanti di quanto si pensasse, mentre altre — come le largamente studiate famiglie let‑7 e miR‑10 — sono spesso state sovrastimate. Lo studio ha anche riesaminato quale “braccio” di ciascun precursore a forcina sia effettivamente utilizzato nelle cellule, scoprendo casi in cui le annotazioni correnti indicano la catena principale sbagliata. Per recuperare la ricchezza degli insiemi di dati esistenti affetti da bias, gli autori hanno addestrato un modello di machine learning che apprende come le misurazioni convenzionali deviano da 4NBoost e poi le corregge matematicamente per riflettere meglio le abbondanze reali.
Una risorsa pubblica per esplorare i piccoli RNA
Tutte le misurazioni 4NBoost e il modello di correzione sono resi liberamente disponibili tramite una piattaforma online chiamata SmRNAQuant. I ricercatori possono navigare o scaricare i livelli assoluti di piccoli RNA per tessuti, linee cellulari o microRNA specifici, e possono caricare i propri dati preparati con un kit comune per ottenere valori corretti dal bias. Per i non specialisti, il messaggio chiave è che il conteggio conta: piccole differenze nel numero di copie di un piccolo RNA possono decidere se la regolazione genica è attiva o non ha alcun effetto. Offrendo numeri più affidabili e un modo per correggere i dati più vecchi, questo lavoro pone una base quantitativa più solida per capire come i piccoli RNA modellano la biologia normale e la malattia.
Citazione: Xiao, W., Zheng, Y., Zhang, H. et al. An absolute quantification atlas of small non-coding RNAs across diverse mammalian tissues and cell lines. Nat Commun 17, 2314 (2026). https://doi.org/10.1038/s41467-026-68812-7
Parole chiave: quantificazione dei microRNA, piccoli RNA non codificanti, bias nel sequenziamento dell'RNA, atlante di espressione tissutale, correzione tramite machine learning