Clear Sky Science · it
Il panorama funzionale dello splicing alternativo nell'impegno delle linee ematopoietiche
Come piccole modifiche nei geni modellano il nostro sangue
Ogni secondo il tuo corpo produce milioni di nuove cellule del sangue. Dietro questo silenzioso miracolo c’è un sistema molecolare di editing che può tagliare e incollare porzioni dei messaggi genetici in modi diversi, creando versioni leggermente differenti della stessa proteina. Questo studio esplora come quel processo di editing, chiamato splicing alternativo, aiuti a indirizzare le cellule staminali immature verso la trasformazione in globuli rossi, globuli bianchi o altri tipi di cellule ematiche — e cosa accade quando viene meno un singolo segmento modificato.
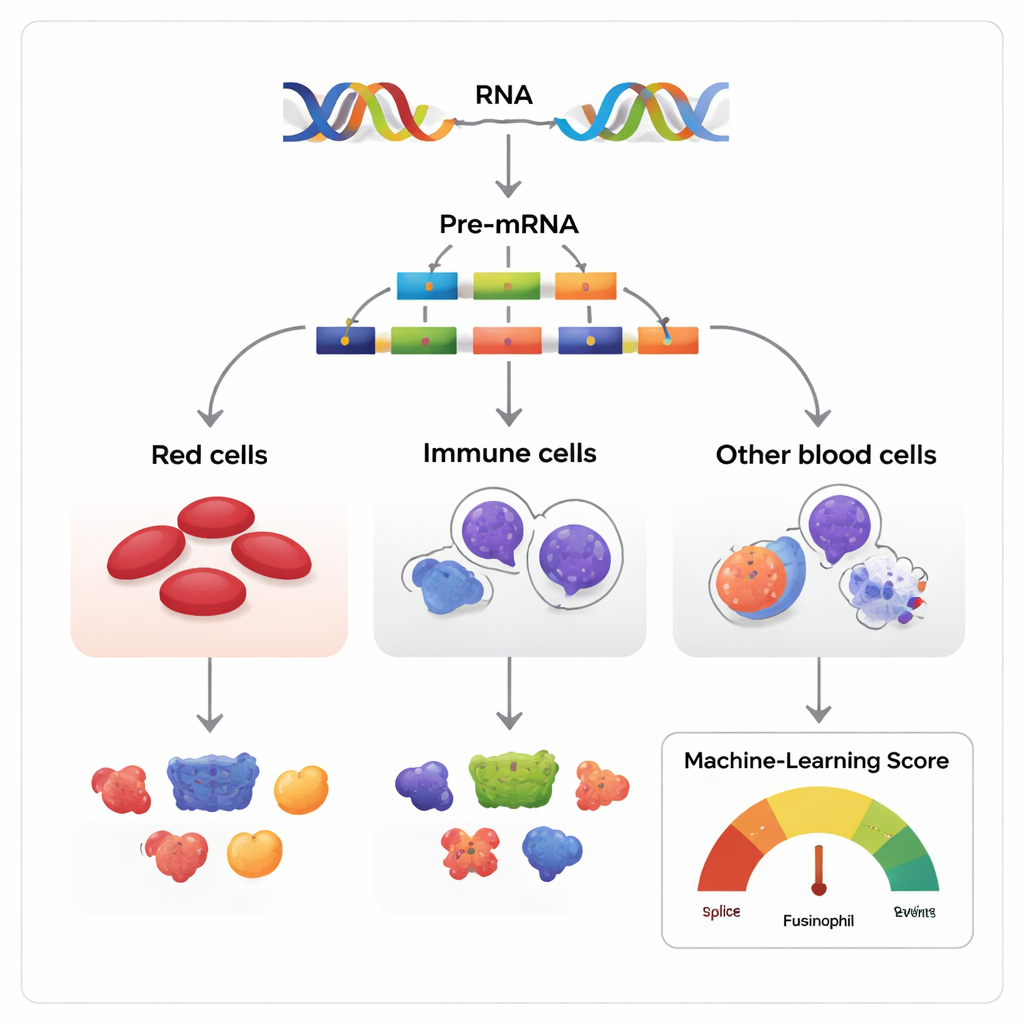
Molte versioni dallo stesso copione genetico
I geni vengono spesso descritti come progetti, ma in realtà assomigliano di più a copioni che possono essere riorganizzati. Quando un gene viene trascritto, la copia iniziale di RNA contiene segmenti chiamati esoni che possono essere mantenuti o saltati prima che il messaggio finale venga tradotto in proteina. Gli autori hanno esaminato questo processo, noto come salto di esoni, nei tessuti che formano il sangue in esseri umani, topi e diversi altri vertebrati. Hanno assemblato oltre 270 dataset di RNA che insieme seguono cellule staminali e progenitrici ematiche mentre maturano in tre famiglie principali: cellule eritroidi produttrici di globuli rossi, cellule mieloidi difensive contro le infezioni e cellule linfoidi produttrici di anticorpi.
Classificare quali cambiamenti di splicing contano davvero
Poiché la maggior parte dei geni multi-esonici può essere splicingata in molti modi, la sfida centrale è distinguere le variazioni innocue da quelle che influenzano realmente il destino cellulare. I ricercatori hanno costruito un modello di apprendimento automatico, chiamato Functional AS Score (FAScore), per affrontare questo problema. Per ogni evento di salto di esone, il modello considera 19 elementi informativi, come l’ampiezza del cambiamento d’uso durante lo sviluppo cellulare, quanto è conservato il DNA circostante tra le specie, se altera domini proteici noti e se contiene siti per modifiche chimiche della proteina. L’algoritmo, addestrato con una strategia positive–unlabeled e con un classificatore random forest, restituisce un punteggio tra 0 e 1 che indica quanto è probabile che un dato evento di splicing abbia un impatto funzionale.
Individuare interruttori conservati e specifici della linea
Applicando FAScore a decine di migliaia di eventi di salto di esoni, il team li ha classificati in gruppi probabili funzionali, non funzionali o incerti. Gli eventi previsti come funzionali si trovavano più spesso in regioni proteiche importanti per le interazioni, in sequenze evolutivamente conservate e in segmenti che ospitano etichette chimiche come fosforilazione o SUMOilazione. Molti di questi eventi erano inoltre attivi solo in specifiche linee ematiche o durante la formazione fetale del sangue, suggerendo che agiscono come interruttori finemente regolati in finestre di sviluppo particolari. Lo studio ha inoltre mostrato che alcuni degli eventi di splicing più antichi — quelli condivisi tra i vertebrati per centinaia di milioni di anni — sono particolarmente probabili di essere funzionali, rispecchiando come i geni più vecchi tendano a svolgere ruoli biologici centrali.
Prova sperimentale: modulare gli esiti delle cellule del sangue
Per verificare le predizioni del modello, gli autori hanno scelto diversi esoni con punteggi elevati in geni attivi nelle varie linee ematiche e hanno rimosso quegli esoni nelle cellule staminali e progenitrici del sangue dei topi usando CRISPR. I risultati hanno confermato le aspettative del modello: rimuovere certi esoni nei geni KLF6 e SSBP3 ha compromesso la formazione di colonie mieloidi senza danneggiare la produzione di globuli rossi, mentre eliminare esoni in EPB41L1 e TBC1D23 ha alterato la formazione di colonie eritroidi. In particolare, saltare l’esone 15 di TBC1D23 ha ridotto la produzione di precursori dei globuli rossi in topi e zebrafish, portando a un minor numero di globuli rossi circolanti e a livelli di emoglobina più bassi, pur risparmiando in gran parte i globuli bianchi.
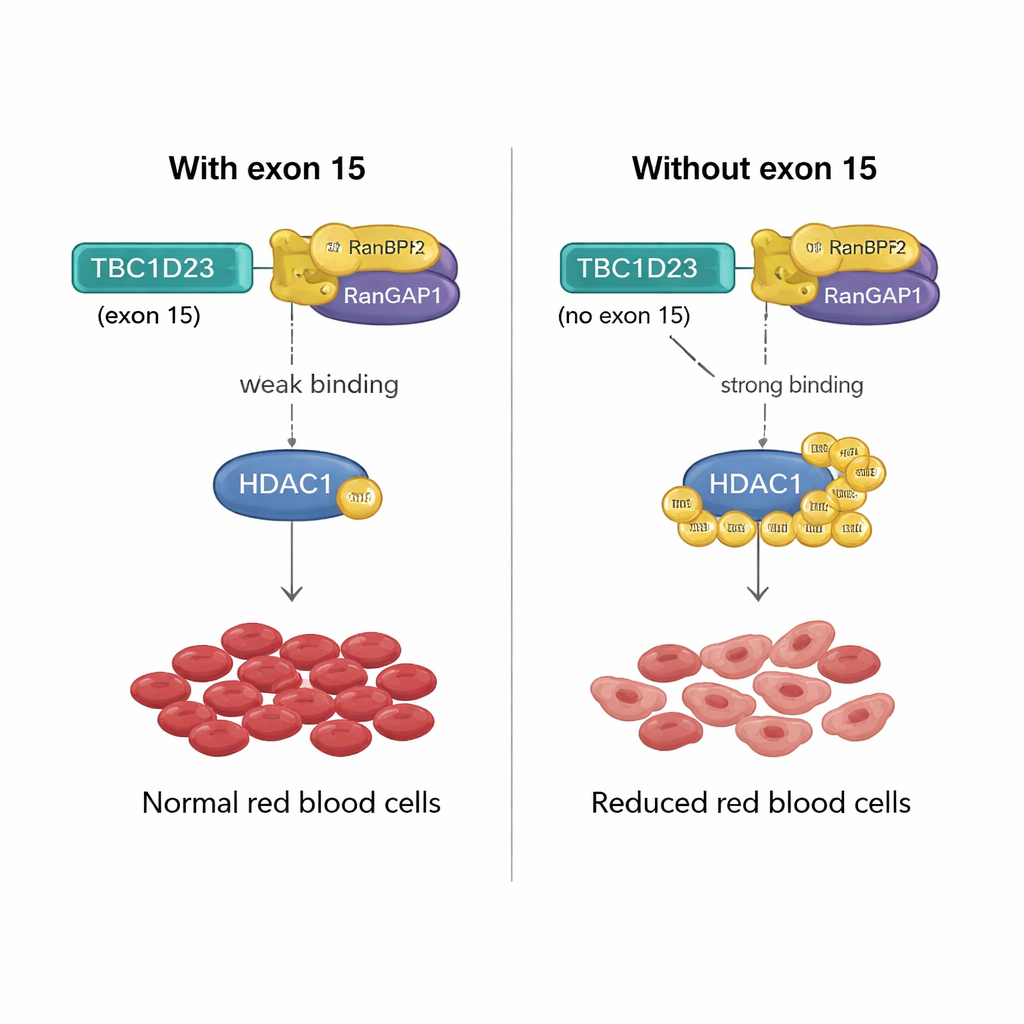
Una leva molecolare per la produzione di globuli rossi
Come può una porzione di 15 amminoacidi codificata dall’esone 15 di TBC1D23 avere un effetto tanto marcato? Il team ha scoperto che l’inclusione di questo esone indebolisce il legame di TBC1D23 con una coppia proteica chiamata RANBP2/RANGAP1, che collabora per attaccare etichette SUMO ad altre proteine. Senza l’esone 15, TBC1D23 si lega più fortemente a questa coppia, aumentando la SUMOilazione di un enzima chiave, HDAC1. Questo incremento delle etichettature modifica l’attività di molti fattori di trascrizione — regolatori principali dell’espressione genica — alterando i programmi genici necessari per la corretta maturazione dei globuli rossi. Quando i ricercatori hanno ingegnerizzato una versione di HDAC1 che non può essere SUMOilata in due posizioni cruciali, questa ha ripristinato la formazione dei globuli rossi nelle cellule prive dell’esone 15 di TBC1D23, confermando che questa etichettatura chimica è il passaggio critico.
Perché questo è importante per la salute e le terapie future
Per un non specialista, il messaggio di questo lavoro è che non tutte le modifiche genetiche sono equivalenti: a volte la differenza tra sangue sano e anemia dipende dal fatto che un minuscolo segmento di un gene venga mantenuto o saltato nel messaggio finale. Combinando grandi dataset di RNA con un sistema di punteggio sofisticato, lo studio fornisce una mappa per individuare quali varianti di splicing sono più propense a influenzare la scelta del destino da parte delle cellule staminali. Questo approccio non solo approfondisce la nostra comprensione di come le cellule del sangue si formano in salute e malattia, ma offre anche una strategia generale per identificare eventi di splicing importanti in altri organi, potenzialmente guidando future terapie geniche e trattamenti di precisione.
Citazione: Hu, X., Wang, J., Chen, L. et al. The functional landscape of alternative splicing in hematopoietic lineage commitment. Nat Commun 17, 2047 (2026). https://doi.org/10.1038/s41467-026-68811-8
Parole chiave: splicing alternativo, ematopoiesi, apprendimento automatico, globuli rossi, regolazione genica