Clear Sky Science · it
Base strutturale della regolazione trascrizionale da parte del regolatore della divisione cellulare MraZ in Mycoplasma genitalium
Come un batterio minuscolo controlla quando dividersi
Ogni cellula vivente deve decidere quando separarsi in due, e quella decisione può fare la differenza tra una crescita sana e un’infezione incontrollata. Questo studio esplora uno dei batteri più semplici noti, Mycoplasma genitalium, per rivelare a livello atomico come una singola proteina, chiamata MraZ, si ancora al DNA e accende o spegne geni chiave per la divisione cellulare. Comprendendo questo sistema di controllo minimalista, gli scienziati sperano di individuare regole generali della crescita batterica che un giorno potrebbero ispirare nuovi tipi di antibiotici o cellule sintetiche “minimali”.
Una cellula ridotta all’essenziale con grandi lezioni
Mycoplasma genitalium è famosa per il suo genoma esiguo: solo una frazione del DNA presente in batteri comuni come E. coli. Questa piccola dimensione la rende un modello potente per capire quali geni e sistemi di controllo sono davvero essenziali per la vita. Molti batteri mantengono i geni per la divisione cellulare e la parete cellulare raggruppati in un blocco chiamato cluster dcw. Nei micoplasmi privi di parete, la maggior parte di quei geni è scomparsa, ma ne rimane una manciata, incluso mraZ in testa al cluster. MraZ agisce come un vigile del traffico, controllando l’attività dei geni vicini, che a loro volta influenzano come e quando la cellula si divide.
Un motivo ripetuto nel DNA che funge da interruttore di controllo
Immediatamente a monte del gene mraZ, i ricercatori hanno trovato un tratto di DNA altamente conservato che funge da stazione di aggancio per la proteina MraZ. Questa regione contiene quattro brevi segmenti ripetuti, o “box”, che presentano una sequenza quasi identica in molte specie di batteri. Mutando con attenzione uno, due o più di questi box e misurando quanto saldamente MraZ riuscisse ancora a legare il DNA, il gruppo ha dimostrato che la proteina lega in modo cooperativo: ogni box contribuisce a rafforzare la presa complessiva. Esperimenti con reporter fluorescenti hanno confermato che più i box venivano disturbati, meno efficacemente MraZ riusciva a reprimere l’attività genica, sottolineando la loro importanza come pannello di controllo finemente regolato. 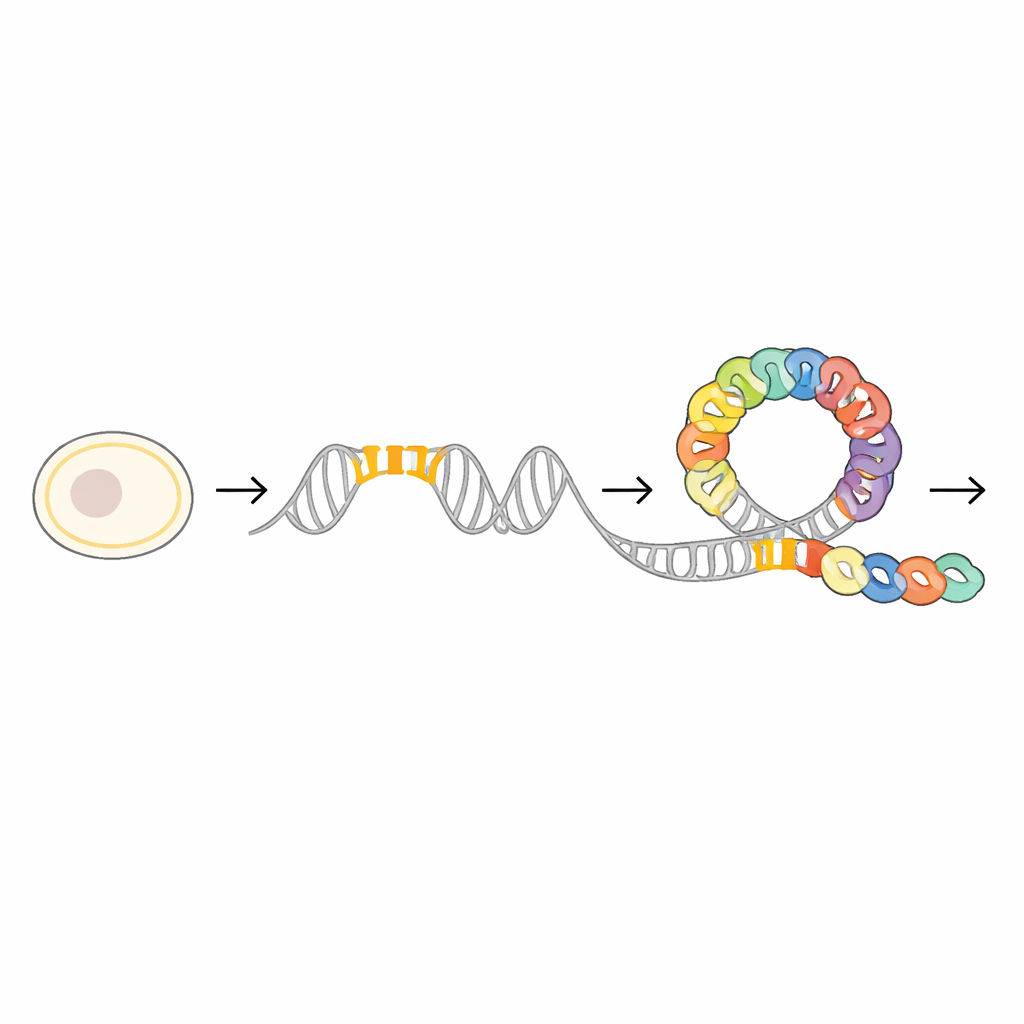
Una proteina ad anello che si apre per abbracciare il DNA
Per vedere come funziona questo pannello di controllo a livello atomico, gli scienziati hanno usato crio-microscopia elettronica e cristallografia a raggi X per risolvere diverse strutture tridimensionali di MraZ da sola e legata al DNA. Da sola, la molecola di MraZ si unisce in assemblaggi ad anello composti da otto o nove subunità identiche. Questi anelli hanno una superficie distintiva a forma di “culla” formata da una piccola struttura a foglietto beta, diversa dalle eliche a spirale spesso osservate nelle proteine leganti il DNA. Quando MraZ incontra il segmento di DNA con i quattro box, l’anello non si limita a posarsi sull’elica; si flette e si riorganizza in modo che quattro delle sue subunità si allineino lungo il DNA, ognuna adagiando un box nella scanalatura maggiore.
Punti di contatto chiave che leggono il codice del DNA
Le strutture ad alta risoluzione hanno rivelato che ogni subunità a contatto con il DNA usa tre catene laterali cariche positivamente—punti specifici sulla superficie proteica—per leggere la sequenza del DNA. Queste “dita” chimiche si inseriscono nella scanalatura della doppia elica e formano legami idrogeno precisi con coppie di basi particolari nei box conservati. Quando i ricercatori sostituivano una qualsivoglia di queste tre residue, MraZ perdeva in gran parte la capacità di legare il DNA e di spegnere il gene reporter di prova. Contatti aggiuntivi con lo scheletro zucchero-fosfato del DNA aiutano a stabilizzare il complesso ma sono meno specifici per la sequenza. Insieme, questi risultati mostrano come MraZ combini una testa di lettura altamente specializzata con un corpo multi-subunità flessibile per riconoscere la sua regione bersaglio. 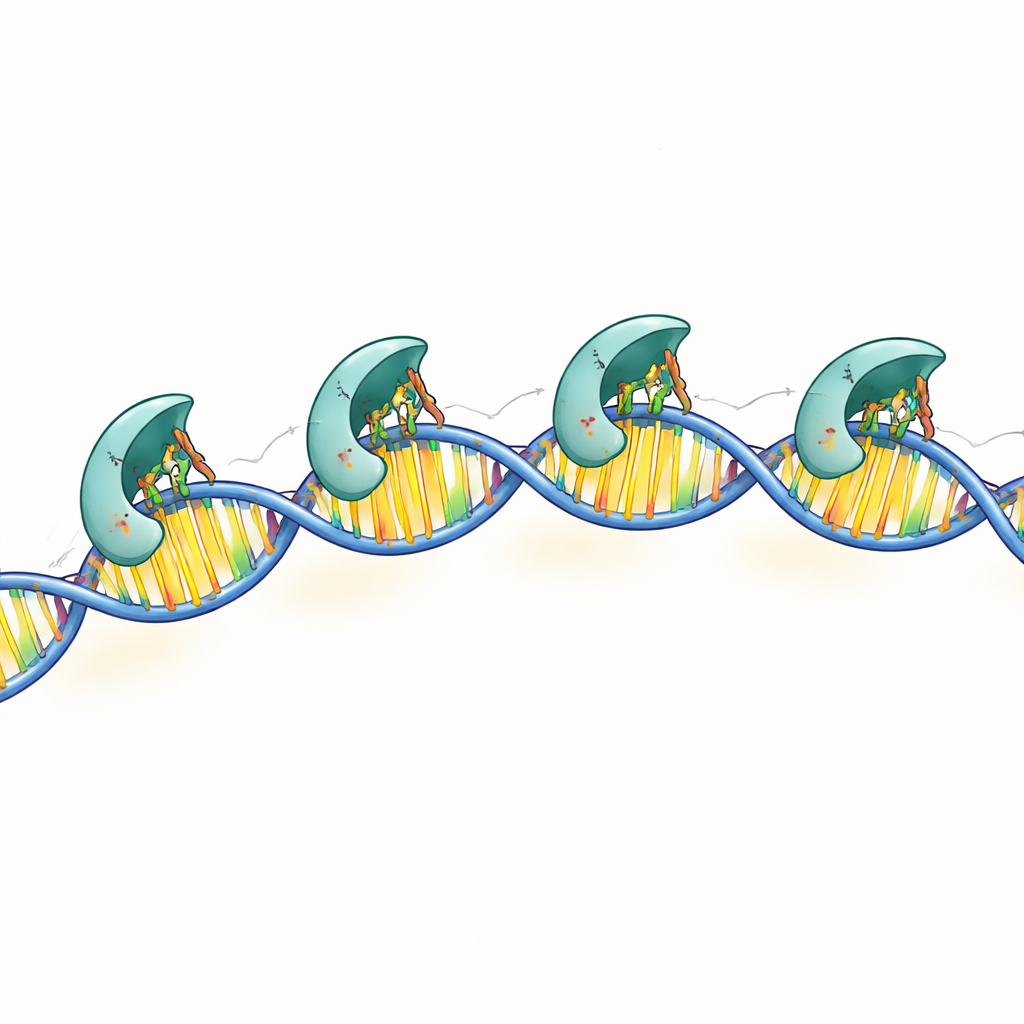
Oligomeri che modulano la forza del controllo
Poiché MraZ forma anelli e altre strutture multi-unità, il gruppo si è chiesto se questo raggruppamento sia necessario per il legame al DNA o semplicemente lo affini. Ingegnerizzando una versione di MraZ che non poteva più assemblarsi in anelli, hanno scoperto che la proteina continuava a legare la sequenza a quattro box, ma con affinità ridotta. Questa forma monomerica dava particolare difficoltà quando veniva alterata la distanza tra i box, suggerendo che l’oligomero completo aiuti a collegare e ad allineare box distanti, aumentando la concentrazione locale di motivi di legame lungo il DNA. Gli autori propongono un modello dinamico in cui MraZ oscilla tra un anello chiuso e una forma aperta impegnata sul DNA, usando il suo stato di assemblaggio come manopola per regolare quanto saldamente serra il promotore.
Cosa significa per i batteri e oltre
In termini semplici, questo lavoro spiega come una piccola proteina in un batterio minimale afferri un motivo ripetuto sul DNA e lo usi come interruttore maestro per i geni della divisione cellulare. La combinazione di una testa di lettura a forma di culla e di un corpo ad anello flessibile permette a MraZ di riconoscere il suo bersaglio con alta precisione pur rimanendo adattabile a diversi arrangiamenti del DNA. Poiché proteine e motivi di DNA simili appaiono in molti batteri, il meccanismo qui descritto è probabilmente una strategia condivisa per coordinare crescita e divisione. Le intuizioni tratte da questo sistema ridotto potrebbero aiutare i ricercatori a progettare circuiti genetici semplificati in cellule sintetiche e, nel lungo periodo, contribuire a nuovi modi per interrompere la crescita batterica nelle malattie.
Citazione: Sánchez-Alba, L., Varejão, N., Durand, A. et al. Structural basis for transcriptional regulation by the cell division regulator MraZ in Mycoplasma genitalium. Nat Commun 17, 2132 (2026). https://doi.org/10.1038/s41467-026-68809-2
Parole chiave: divisione cellulare batterica, interazione DNA–proteina, regolazione trascrizionale, crio-microscopia elettronica, Mycoplasma genitalium