Clear Sky Science · it
Traiettorie cellulari e trascrizionali della specificazione del destino neurale nell’anemone di mare rivelano due modalità di neurogenesi adulta
Come una creatura marina semplice continua a produrre nuove cellule cerebrali
La maggior parte degli animali, compresi gli esseri umani, produce la maggior parte dei neuroni nelle prime fasi della vita e poi sostanzialmente smette. Tuttavia, alcuni organismi apparentemente semplici, come gli anemoni di mare, continuano ad aggiungere nuovi neuroni per tutto l’età adulta. Questo studio esplora come l’anemone stella (Nematostella vectensis) rinnovi e rimodelli costantemente il suo sistema nervoso diffuso, rivelando strategie che potrebbero richiamare soluzioni antiche per la crescita e la riparazione del cervello.
Un corpo che cresce necessita di una rete nervosa che cresce
Gli anemoni di mare non hanno un cervello; hanno invece una rete nervosa a maglia diffusa distribuita nella parete corporea. Quando questi animali crescono o si riducono in base alla disponibilità di cibo, la loro rete nervosa deve scalare verso l’alto o verso il basso per adeguarsi. Usando una proteina fluorescente sensibile alla luce come “timestamp”, gli autori hanno marcato i neuroni esistenti in giovani adulti e poi hanno osservato le cellule neoformate che comparivano nella settimana successiva. Hanno trovato numerosi nuovi neuroni sparsi lungo l’asse corporeo, non confinati a una zona di crescita speciale. Queste cellule giovani sono apparse sia dal lato rivolto verso la bocca sia dall’estremità opposta dell’animale, indicando che la neurogenesi adulta è spazialmente diffusa e continua.
Tracciare l’origine delle nuove cellule nervose
Per scoprire da dove provengono queste nuove cellule, i ricercatori hanno combinato imaging in vivo con sequenziamento dell’RNA a singola cellula, una tecnica che legge quali geni sono attivi in migliaia di singole cellule. Si sono concentrati su cellule che portano reporter fluorescenti controllati da tre geni chiave: FoxL2, SoxC ed Elav. FoxL2 segnala un ampio pool di cellule progenitrici multipotenti in divisione; SoxC si attiva brevemente quando le cellule iniziano a specializzarsi; ed Elav è fortemente espresso nei neuroni peptidergici, che comunicano principalmente tramite piccoli peptidi segnalatori. Il gruppo ha mostrato che una popolazione di progenitori FoxL2-positivi e Piwi1-positivi si comporta come cellule staminali: si auto-rinnova mentre genera continuamente discendenti diversi, tra cui neuroni, cellule urticanti chiamate cnidociti e cellule secretorie. SoxC ed Elav, al contrario, si accendono solo quando le cellule lasciano questo pool progenitore e si impegnano in particolari destini neurali.
Due percorsi diversi verso i neuroni adulti
Allineando i tempi dei reporter con il profilo di espressione genica di ogni cellula, lo studio ha individuato due rotte distinte fino a cellule neurali mature. I neuroni peptidergici seguono un percorso diretto: derivano da progenitori che già possiedono un profilo molecolare «impegnato peptidergico» e poi si differenziano rapidamente in una varietà di sottotipi neuronali. Nuovi membri di ciascun sottotipo compaiono in proporzione a quanto quel sottotipo è già comune, suggerendo che il sistema mantiene una mescolanza equilibrata di tipi neuronali piuttosto che favorirne alcuni in particolare. In questa linea, non esiste una serie chiara di stazioni intermedie; al contrario, sottotipi neuronali strettamente correlati emergono in parallelo da progenitori in condizioni simili. 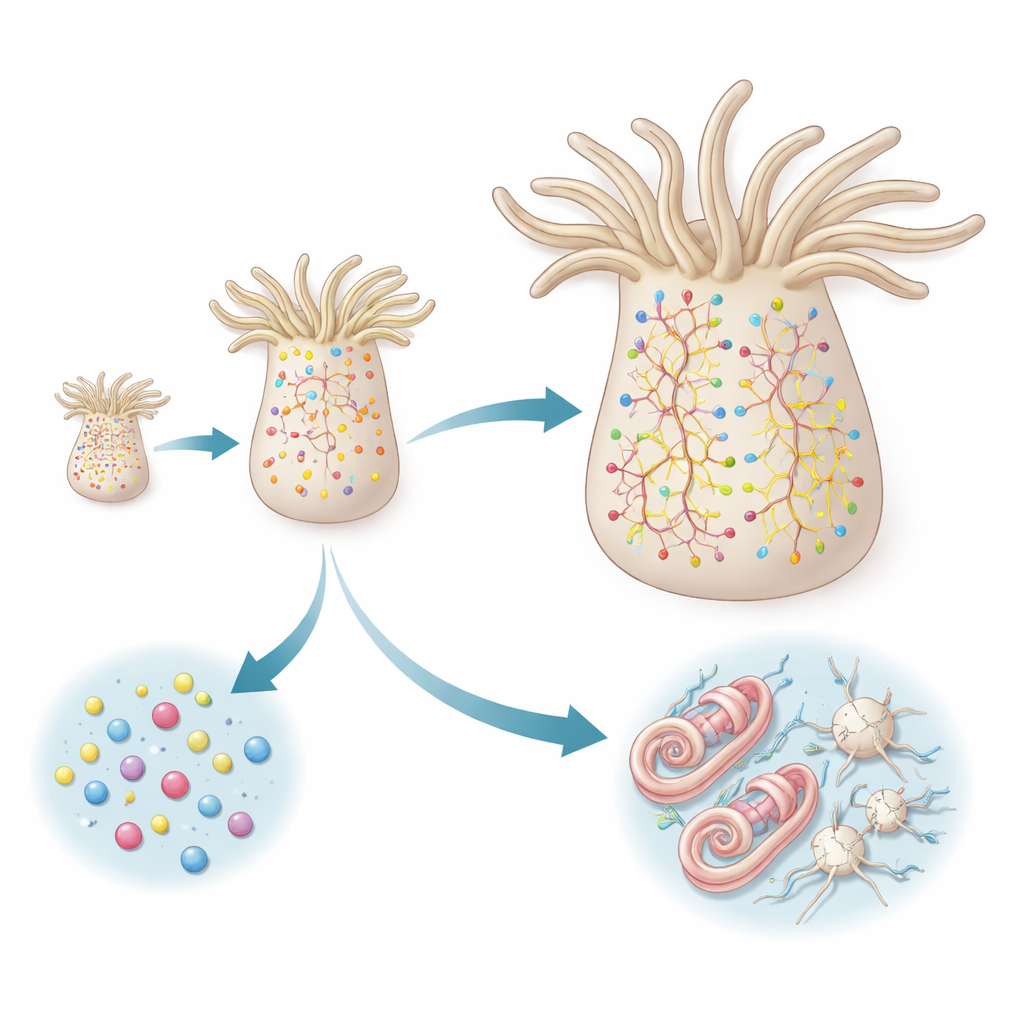
Il caso speciale delle cellule urticanti
I cnidociti, le cellule urticanti uniche dei cnidari, seguono un percorso più graduale. Passano prima attraverso una fase di «costruzione della capsula», durante la quale costruiscono i loro organelli pressurizzati caratteristici in grado di lanciare un arpione microscopico. Questa fase si basa su un insieme specifico di geni regolatori e proteine strutturali che sono per lo più assenti in altri tipi cellulari. Solo dopo il completamento di questo programma intermedio i cnidociti attivano un secondo programma più convenzionale di tipo neurale, aggiungendo canali ionici e altri componenti necessari per la segnalazione elettrica. Dati genetici provenienti da mutanti che si arrestano nella fase iniziale rafforzano questo modello in due fasi: bloccare la transizione impedisce la comparsa delle successive caratteristiche neurali. 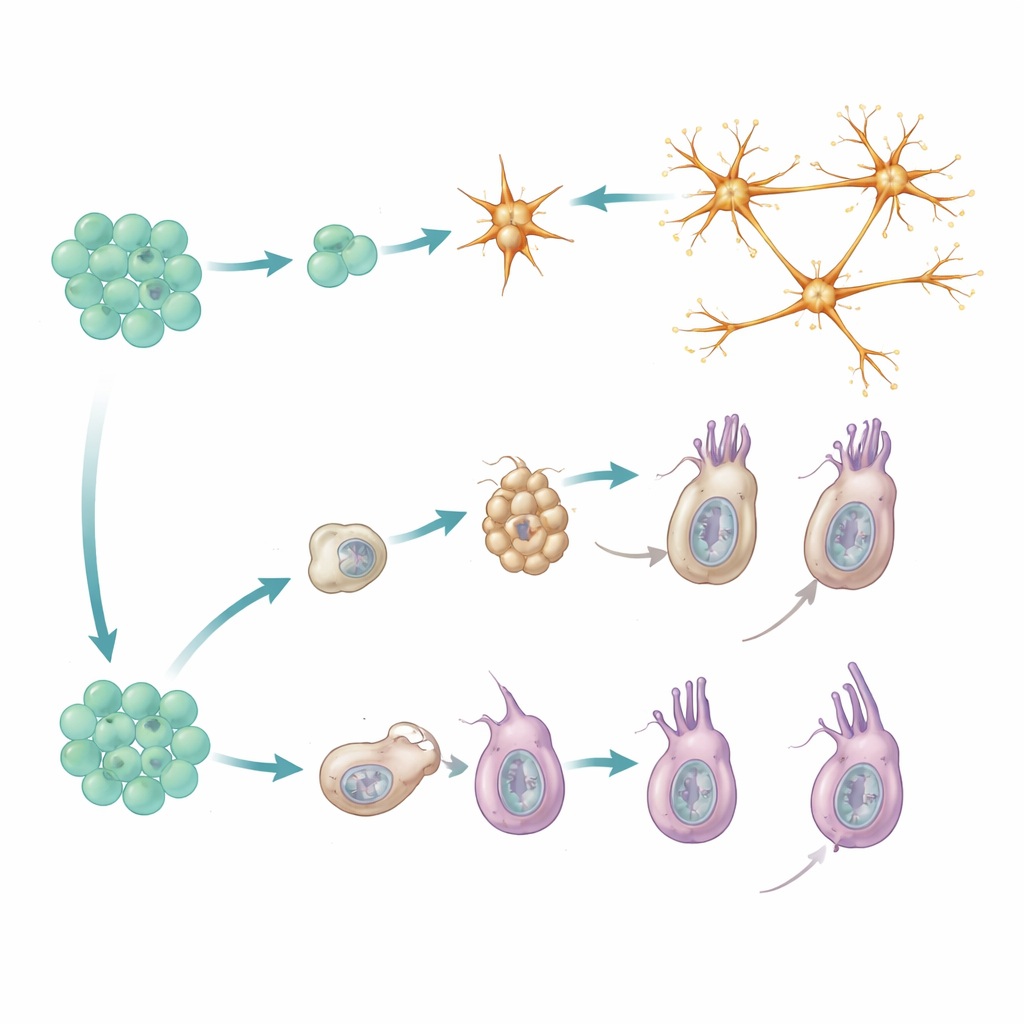
Regole condivise e radici antiche
Nonostante i percorsi differenti, neuroni peptidergici e cnidociti fanno affidamento su famiglie sovrapposte di geni regolatori per consolidare la loro identità. Caratteristiche neurali ampie sono associate a fattori di trascrizione bHLH e bZIP, mentre l’identità fine di ciascun sottotipo neuronale è specificata da combinazioni uniche di geni homeodomain e zinc-finger — un «codice» che ricorda come i tipi neuronali sono definiti in animali più complessi, compresi vermi e vertebrati. Gli autori sostengono che queste strategie modulari — progenitori di tipo staminale, attività transitoria di SoxC durante l’impegno e codici di homeodomain che definiscono i sottotipi — possano rappresentare principi profondamente conservati della neurogenesi. Negli anemoni, supportano il rinnovamento e la scalatura della rete nervosa per tutta la vita; in altri animali, meccanismi correlati potrebbero sostenere sia la neurogenesi adulta limitata sia le straordinarie capacità rigenerative osservate in alcune linee evolutive.
Citazione: Plessier, F., Marlow, H. Cellular and transcriptional trajectories of neural fate specification in sea anemone uncover two modes of adult neurogenesis. Nat Commun 17, 2611 (2026). https://doi.org/10.1038/s41467-026-68802-9
Parole chiave: neurogenesi adulta, anemone di mare, cellule progenitrici neurali, cnidociti, trascrittomica a singola cellula