Clear Sky Science · it
Consegna di coacervati peptidici per formare hub di interazione stabili nelle cellule
Costruire nuovi “postazioni di lavoro” all’interno delle cellule
Le nostre cellule sono piene di piccoli spazi di lavoro dove avvengono attività importanti—come la produzione di energia o le risposte allo stress. Col tempo, o in presenza di malattie, queste postazioni naturali possono indebolirsi. Questo studio esplora un modo per aggiungere nuovi “hub di interazione” nelle cellule vive usando semplici goccioline sintetiche create in laboratorio a partire da brevi peptidi. Questi hub sintetici possono catturare proteine specifiche, concentrarle e persino contribuire alla loro eliminazione, suggerendo nuove strategie per terapie future e per l’ingegneria cellulare.
Perché le cellule hanno bisogno di spazi di lavoro su misura
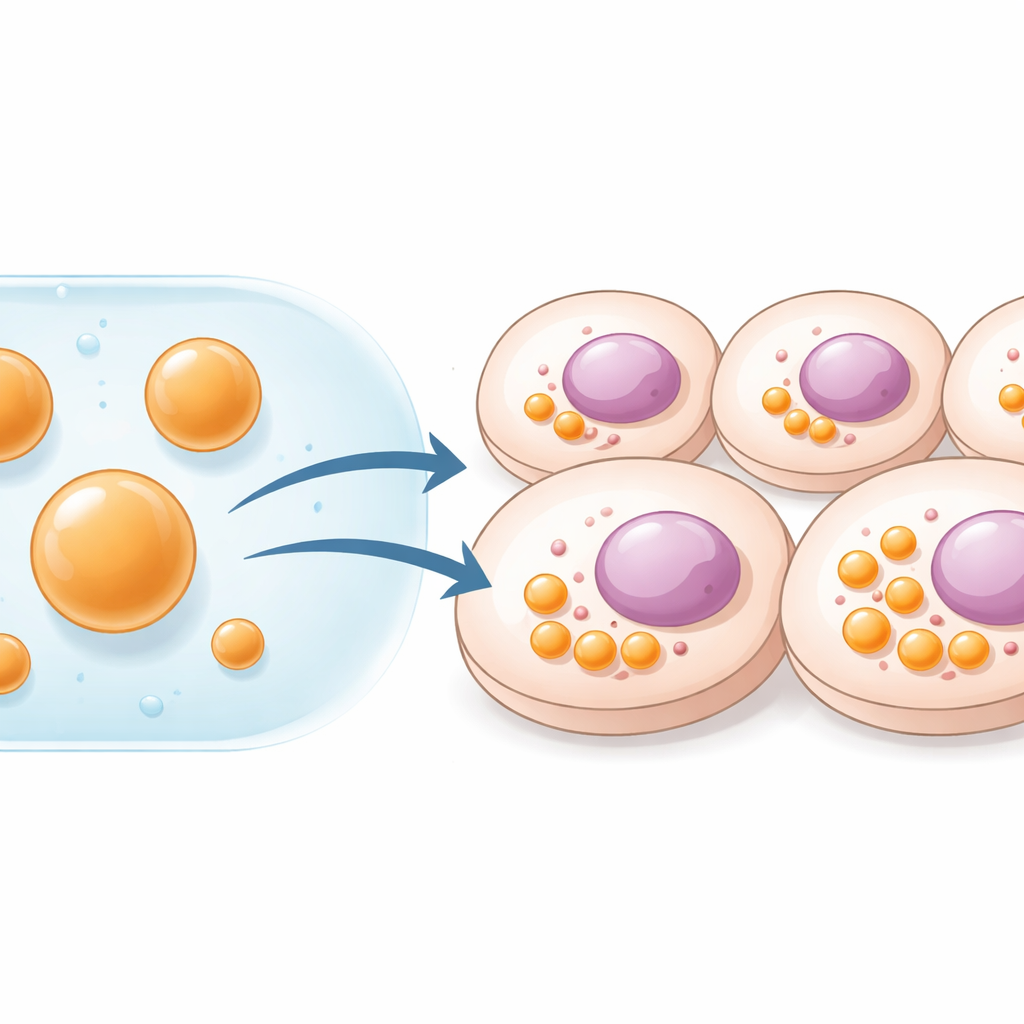
Le cellule mantengono l’ordine separando compiti diversi in compartimenti distinti. Alcuni sono racchiusi da membrane, come i mitocondri; altri sono strutture più morbide a forma di gocciola che si formano quando certe proteine e RNA si raggruppano. Questi condensati fluidi funzionano come centri di reazione che accelerano o spengono specifiche vie biochimiche. In precedenza i ricercatori avevano ingegnerizzato tali compartimenti inducendo le cellule a produrre proteine‑impalcatura speciali tramite geni inseriti. Pur essendo potente, quel metodo richiede la consegna del DNA e limita la quantità di materiale che la cellula può produrre. Gli autori di questo studio hanno cercato di bypassare del tutto il DNA e invece costruire compartimenti pronti all’uso fuori dalla cellula, per poi consegnarli direttamente come goccioline stabili di dimensione micrometrica.
Goccioline peptidiche che formano hub stabili
Il team ha lavorato con peptidi corti e disordinati noti come HBpep e con una variante redox‑sensibile, HBpep‑SA. In condizioni leggermente acide questi peptidi restano disciolti, ma quando il pH viene portato a valori vicini a quelli fisiologici—or quando la temperatura diminuisce—essi subiscono separazione di fase formando goccioline morbide e gel‑like di circa 1–5 micrometri. Regolando la concentrazione dei peptidi, i ricercatori hanno potuto controllare sia la dimensione che il numero delle goccioline. Con tecniche di fluorescenza hanno mostrato che le molecole peptidiche all’interno di queste goccioline si muovono lentamente, indice di uno stato gel che è sufficientemente robusto da resistere a diluizione e manipolazione. Quando aggiunte a colture di cellule tumorali umane, cellule di melanoma murino e cellule immunitarie primarie umane, le goccioline sono state internalizzate efficacemente e si sono accumulate nel citoplasma. Le goccioline più grandi, in particolare, sono rimaste intatte per almeno cinque giorni, agendo di fatto come organelli sintetici di lunga durata all’interno delle cellule vive.
Caricamento e miraggio degli hub
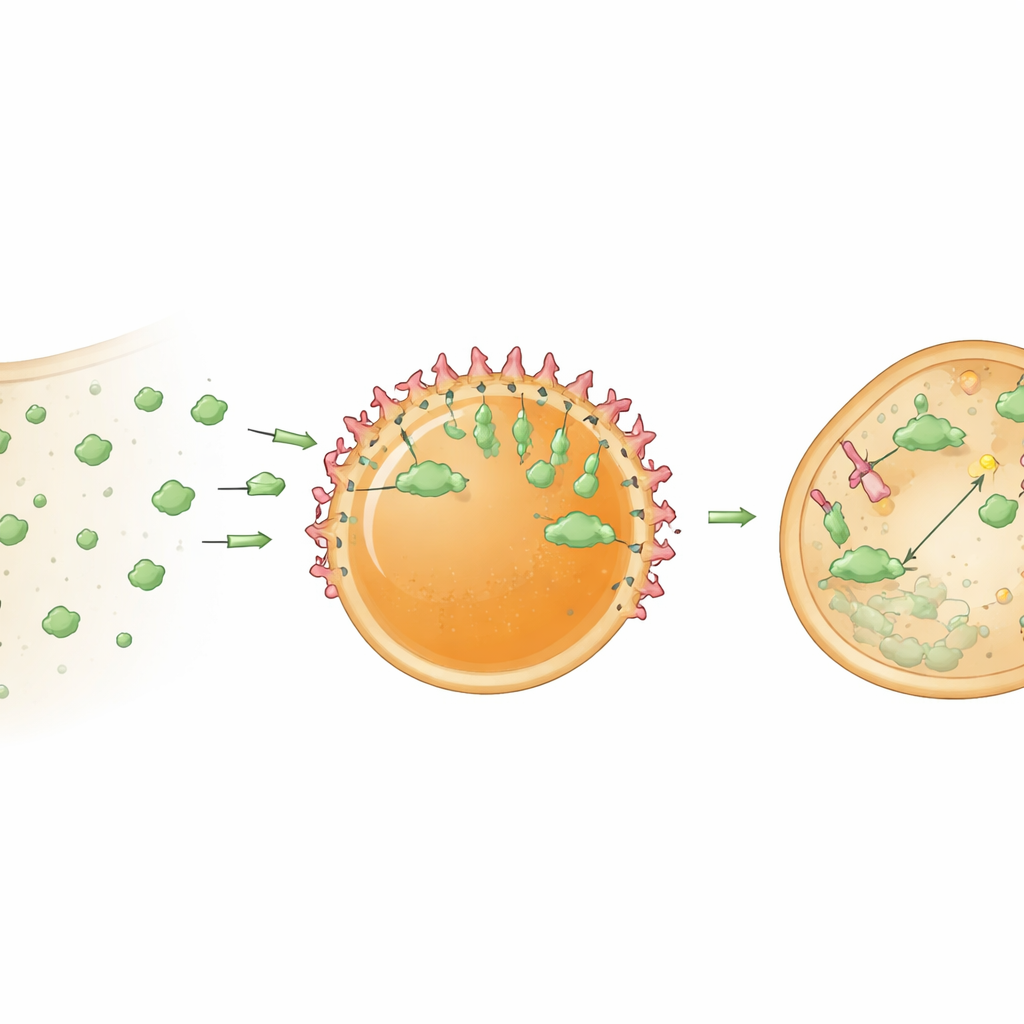
Perché questi hub siano utili devono poter trattenere e organizzare proteine cargo. I ricercatori hanno prima migliorato il caricamento fissando un breve tag derivato da HBpep a una proteina modello, la GFP. Questo tag ha favorito la partizione della GFP nelle goccioline e, fatto interessante, la sua concentrazione vicino alle superfici creando un’organizzazione a nucleo‑guscio. Successivamente hanno incorporato nanobodies—proteine compatte simili ad anticorpi che legano saldamente bersagli scelti—all’interno delle goccioline. Un nanobody che lega la GFP ha permesso agli hub di catturare selettivamente la GFP sia in provetta sia all’interno delle cellule. Poiché il gel peptidico è relativamente denso, inizialmente la maggior parte della GFP catturata si accumulava alla superficie della gocciolina. Ma quando la struttura interna è stata parzialmente allentata, o modificando le condizioni redox o favorendo la fuga delle goccioline dalle membrane endosomali che le circondano, la GFP ha cominciato anche a penetrare l’interno. Nelle cellule, coadiuvanti chimici che promuovono l’escape endosomale hanno aumentato notevolmente la frazione di hub in grado di reclutare con successo i loro bersagli.
Trasformare gli hub in trituratori di proteine
Gli autori hanno quindi aggiornato questi hub da trappole passive a centri di processamento attivi. Hanno caricato le goccioline con un bioPROTAC—una proteina di fusione che combina un nanobody legante il bersaglio con una parte di un adattatore enzimatico che segnala le proteine per la distruzione presso la macchina di smaltimento cellulare. Quando questi esempi di goccioline “degradosome” sono stati consegnati in cellule che esprimevano stabilmente la GFP, i livelli citosolici di GFP sono diminuiti di circa il 78 percento in un giorno. Gli hub di controllo contenenti solo il nanobody sequestravano la GFP ma non abbassavano in modo apprezzabile il suo livello complessivo, confermando che la forte diminuzione derivava dalla degradazione mirata piuttosto che dalla semplice cattura. I risultati suggeriscono che il clustering dei bioPROTAC all’interno di un microambiente concentrato li rende molto più potenti rispetto a quando sono dispersi liberamente nel citoplasma.
Cosa potrebbe significare per terapie future
In termini semplici, questo lavoro dimostra che gli scienziati possono fabbricare goccioline a base peptidica in provetta, caricarle con strumenti proteici personalizzati e poi consegnarle nelle cellule vive dove si comportano come nuovi organelli durevoli. Questi hub sintetici possono richiamare selettivamente proteine naturali e, se equipaggiati con macchine per la degradazione, possono rimuovere attivamente bersagli scelti dalla cellula. Poiché questa piattaforma evita di alterare i geni della cellula ed è modulare rispetto a ciò che può trasportare, apre la strada a terapie che ripristinano o riscrivono il comportamento cellulare—come la rimozione di proteine dannose o la riconfigurazione di segnali difettosi—semplicemente installando nuove “postazioni di lavoro” programmabili nelle nostre cellule.
Citazione: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
Parole chiave: organelle sintetiche, coacervati peptidici, consegna intracellulare, degradazione proteica, ingegneria cellulare