Clear Sky Science · it
Il taglio trans di CRISPR-Cas9 è ostacolato da un R-loop affiancato, da uno spacer allungato e da un dominio HNH inattivo
Perché contano i piccoli tagli al DNA
CRISPR-Cas9 è noto come un bisturi molecolare capace di recidere il DNA in punti scelti, ma questo strumento ha un secondo comportamento meno noto: una volta attivato, può anche sgranocchiare altri frammenti di materiale genetico nelle vicinanze. Capire quando questo taglio “collaterale” si accende o si spegne è cruciale per rendere più sicure le terapie di editing genico e più sensibili i test diagnostici. Questo studio analizza le caratteristiche fisiche del complesso Cas9–DNA–RNA che determinano se Cas9 esegue silenziosamente il taglio previsto o inizia anche a degradare filamenti semplici di DNA circostanti.
Come si avviano le forbici CRISPR
Per agire, Cas9 si lega a un breve pezzo di RNA guida che lo indirizza verso una sequenza di DNA corrispondente all'interno del genoma. Quando Cas9 trova il bersaglio, l'RNA guida si appaia con un filamento di DNA, costringendo le due eliche a separarsi e creando una regione ibrida DNA–RNA chiamata R-loop. Nel suo ruolo classico, Cas9 taglia poi entrambi i filamenti del DNA in quel punto. Ma lavori recenti hanno mostrato che una volta attivato in questo modo, il dominio di taglio RuvC di Cas9 può anche recidere DNA a singolo filamento non correlati, come tratti di poli(T), altrove nella soluzione. Gli autori hanno voluto capire quali esatte caratteristiche geometriche e strutturali del DNA bersaglio e dell'RNA guida rendono questa attività collaterale forte, debole o assente.
Target corti contro lunghi: dare spazio a Cas9 per muoversi
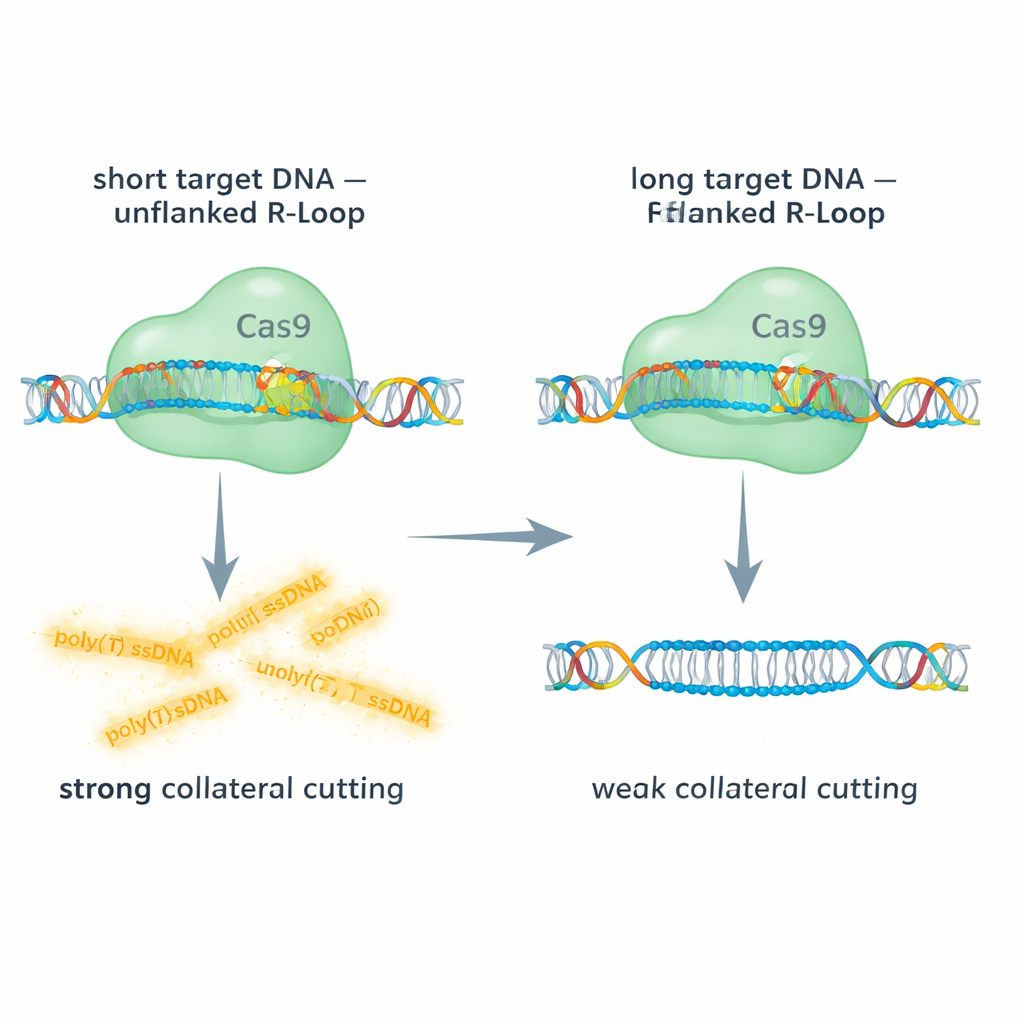
Il gruppo ha confrontato l'attività di Cas9 su bersagli di DNA a doppio filamento corti e lunghi, usando letture fluorescenti per seguire sia il taglio sul bersaglio sia il taglio collaterale di una sonda a singolo filamento. Con bersagli di DNA corti, l'R-loop all'estremità 5′ dell'RNA guida è “non affiancato” — non c'è DNA a doppio filamento che continui oltre la regione ibrida. In queste condizioni, Cas9 mostrò una forte attività collaterale sul DNA a singolo filamento. Al contrario, quando usarono segmenti di DNA più lunghi che lasciavano DNA a doppio filamento adiacente all'R-loop, il taglio collaterale diminuì drasticamente, talvolta di circa il 90%, pur verificandosi ancora il taglio principale sul bersaglio. Il targeting di DNA a singolo filamento lungo, che rimuove completamente l'R-loop, ripristinò in larga misura l'attività collaterale. Questi confronti rivelano che un 'cappuccio' a doppio filamento accanto all'R-loop irrigidisce il complesso e ostacola fisicamente l'accesso o la flessibilità necessaria al dominio RuvC di Cas9 per recidere altri filamenti.
Regolazione fine con la lunghezza della guida e i mismatch
I ricercatori hanno poi esplorato come l'RNA guida moduli questo comportamento. Hanno introdotto piccoli mismatch tra la guida e il DNA bersaglio e hanno seguito quanto bene Cas9 continuasse a tagliare. Il taglio principale sul bersaglio tollerava molti mismatch a singola base, ma il taglio collaterale era più fragile e dipendeva fortemente dalla posizione esatta del mismatch, sottolineandone la sensibilità. Successivamente hanno allungato sistematicamente lo spacer dell'RNA guida oltre i consueti 20 nucleotidi. Pur se Cas9 poteva ancora legare e tagliare il DNA bersaglio, l'attività collaterale diminuì quasi linearmente con l'aumentare della lunghezza dello spacer: aggiungere appena due basi riduceva l'attività collaterale di circa la metà, e quattro basi in più la riducevano ulteriormente. In test pratici con materiale genetico di SARS-CoV-2, solo gli ampliconi di DNA predisposti per produrre un R-loop non affiancato con una guida di lunghezza standard diedero un forte segnale collaterale, evidenziando come il disegno di primer e guide possa determinare il successo o il fallimento di saggi diagnostici basati su CRISPR.
Un dominio ausiliario essenziale dietro le quinte
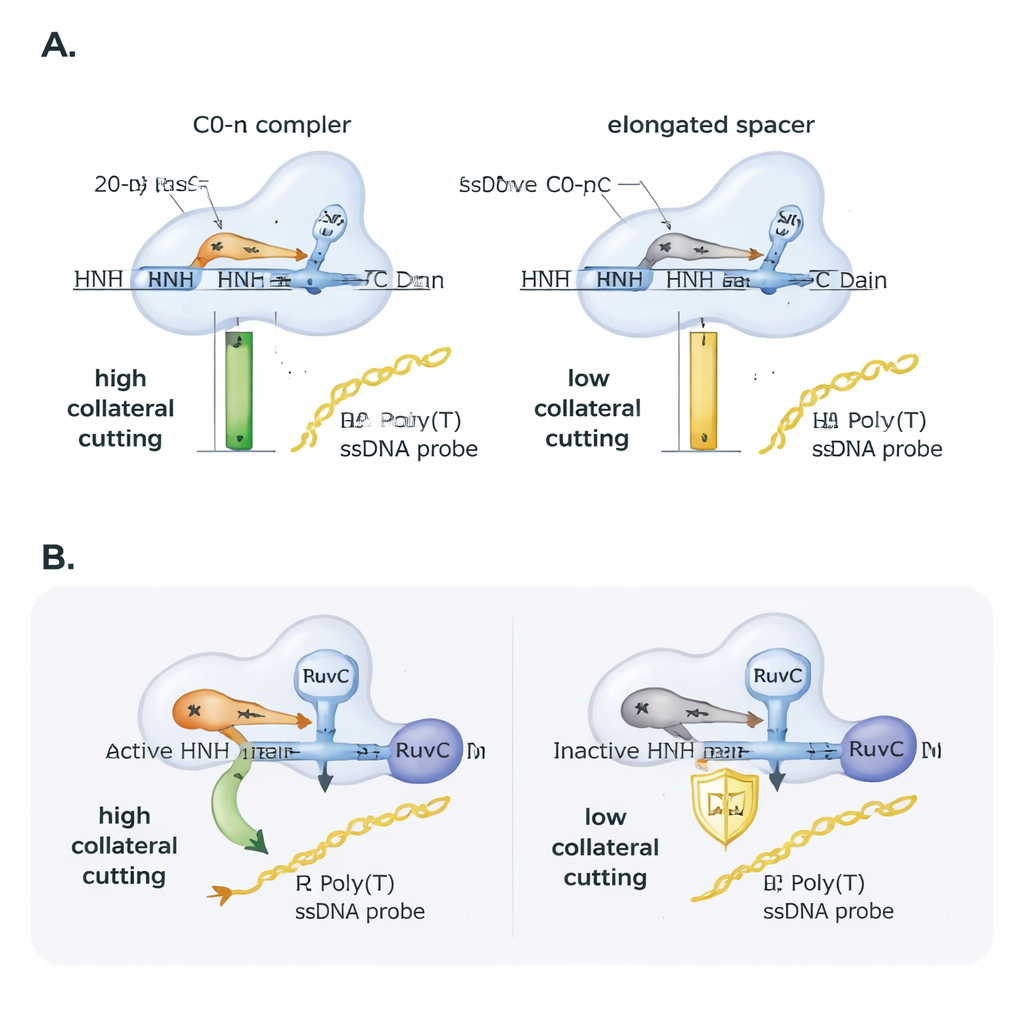
Cas9 possiede due domini di taglio, RuvC e HNH. Studi precedenti avevano collegato direttamente il taglio collaterale a RuvC, ma questo lavoro mostra che anche HNH è importante. Quando gli autori usarono una variante di Cas9 con il dominio HNH inattivo, l'attività collaterale crollò, pur mantenendosi il legame al bersaglio e il comportamento di nicking. Interessante, se fornirono a Cas9 un bersaglio di DNA già tagliato (nicked) su un filamento, la versione con HNH inattivo recuperò l'attività collaterale in modo simile all'enzima normale. Questo suggerisce che il ruolo di HNH è in parte meccanico: tagliando o ammorbidendo il filamento mirato, aiuta la proteina a stabilizzarsi in una conformazione che espone RuvC al DNA a singolo filamento nelle vicinanze. Analisi strutturali di modelli 3D esistenti supportano questa lettura, mostrando che R-loop non affiancati e guide di lunghezza standard permettono all'estremità 5′ dell'RNA di “appoggiarsi” su Cas9 e di posizionare favorevolmente le regioni catalitiche, mentre R-loop affiancati e guide allungate compattono la proteina e probabilmente schermano il sito RuvC dai filamenti estranei.
Cosa significa per gli strumenti futuri
Per i non specialisti, il messaggio principale è che il comportamento di Cas9 non è tutto-o-nulla: piccoli dettagli geometrici — quanto si estende il DNA, quanto è lunga la guida e se un dominio ausiliario può completare il suo taglio — decidono se l'enzima si limita al suo compito principale o degrada anche filamenti singoli vicini. Bersagli corti che lasciano l'R-loop non affiancato, guide standard di 20 basi e un dominio HNH attivo favoriscono un forte taglio collaterale; DNA fluttuante adiacente lungo, guide allungate o un dominio HNH inattivo lo sopprimono. Queste intuizioni forniscono ai ricercatori una manopola più precisa per modulare Cas9, aiutandoli a progettare sistemi di editing genico più sicuri che evitino danni collaterali indesiderati, oppure saggi diagnostici più potenti che sfruttino intenzionalmente questa attività collaterale per rilevare piccole quantità di materiale virale o genetico.
Citazione: Montagud-Martínez, R., Ruiz, R., Baldanta, S. et al. CRISPR-Cas9 trans-cleavage is hindered by a flanked R-loop, an elongated spacer, and an inactive HNH domain. Nat Commun 17, 1998 (2026). https://doi.org/10.1038/s41467-026-68789-3
Parole chiave: CRISPR-Cas9, taglio collaterale, R-loop, spacer dell'RNA guida, diagnostica degli acidi nucleici