Clear Sky Science · it
NatA si impegna in complessi multifattoriali all’uscita del tunnel polipeptidico ribosomale
Come le cellule perfezionano le proteine appena sintetizzate
Ogni secondo, le tue cellule producono migliaia di nuove proteine su minuscole macchine chiamate ribosomi. Man mano che la catena proteica emerge, deve essere rifinita, etichettata e ripiegata correttamente, altrimenti può comportarsi in modo anomalo e contribuire a malattie. Questo studio esamina uno dei sistemi di etichettatura chiave, una modificazione chiamata acetilazione N-terminale, e mostra come un complesso enzimatico centrale, NatA, collabori con diversi partner proprio nel punto in cui le nuove proteine escono dal ribosoma. Comprendere questa coreografia aiuta a spiegare come le cellule mantengano efficienti le loro “fabbriche” proteiche.
Il piccolo tag chimico che conta
La maggior parte delle proteine inizia la propria esistenza con lo stesso primo mattone, l’amminoacido metionina. Spesso questa metionina iniziale viene rimossa e sostituita con un piccolo gruppo chimico chiamato acetile. Questo tag, aggiunto all’estremità della proteina (la N-terminale), può influenzare la durata di vita della proteina, la sua localizzazione nella cellula e la sua funzione. Due tipi principali di enzimi stazionano all’uscita del tunnel ribosomale per gestire questo primo restyling: le metionina aminopeptidasi (MAP), che tagliano via la metionina iniziale, e le N-terminale acetiltransferasi (NAT), che aggiungono il gruppo acetile. Tra le NAT, NatA è il motore nelle cellule umane, potenzialmente in grado di modificare quasi il 40% di tutte le proteine. Poiché molte proteine vengono sintetizzate simultaneamente, la cellula deve organizzare questi enzimi in modo che il taglio e l’etichettatura avvengano rapidamente e nell’ordine corretto.
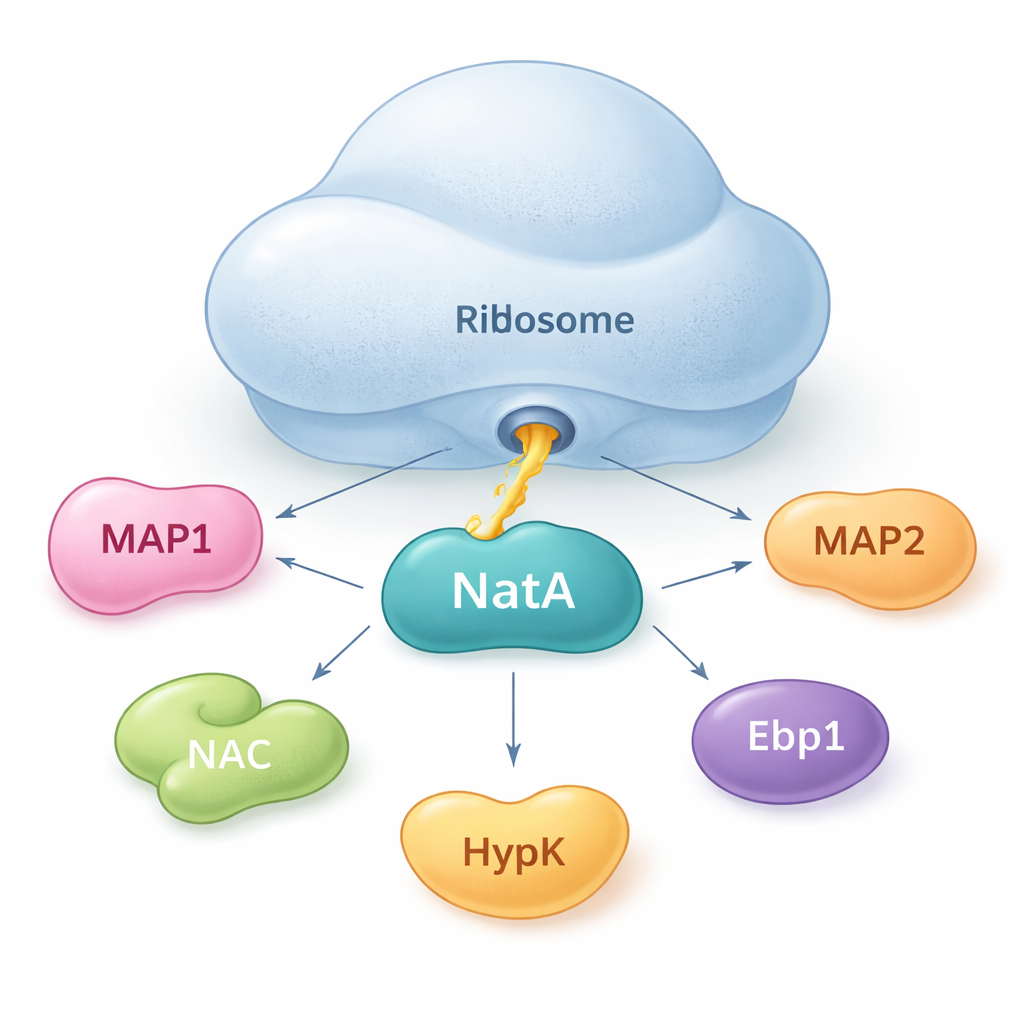
NatA come punto d’incontro per i collaboratori proteici
Gli autori dimostrano che NatA non agisce da sola. Piuttosto, si comporta come un hub che mette insieme molte proteine helper, sia sul ribosoma sia in soluzione libera. Utilizzando misure di legame sensibili in soluzione, hanno scoperto che NatA può formare complessi stabili con MAP1, il complesso associato alle polipeptidi nascenti (NAC), la proteina regolatoria HypK e un altro enzima, Naa50, anche in assenza del ribosoma. NAC può fare da ponte tra NatA e MAP1, permettendo che i passaggi di taglio e acetilazione siano collegati in un’unica assemblaggio. Tuttavia, HypK, che normalmente attenua l’attività di NatA, può impedire il legame di NAC. Ciò suggerisce che le cellule possano commutare NatA tra uno stato più attivo, collegato a NAC, e uno più restrittivo, legato a HypK, a seconda delle necessità.
Un secondo punto di ancoraggio proprio all’uscita del tunnel
Usando la crio–microscopia elettronica, una tecnica che immmagini molecole grandi a dettaglio quasi atomico, i ricercatori hanno scoperto che NatA può legarsi al ribosoma in due posizioni distinte. Un sito, già noto, si trova leggermente distante dall’uscita del tunnel. Il sito “prossimale” appena scoperto posiziona il nucleo catalitico di NatA molto vicino al punto in cui la catena proteica in crescita emerge, riducendo la distanza che la catena deve percorrere per essere modificata. È interessante che entrambe le posizioni possano essere occupate contemporaneamente, il che significa che due complessi NatA possono sedere sullo stesso ribosoma. La copia più distante agisce come impalcatura e ancoraggio, mentre la copia prossimale è idealmente collocata per etichettare le nuove proteine. Le due molecole di NatA si toccano inoltre tra loro, indicando che NatA può coordinare i propri duplicati in squadre multi-enzimatiche.
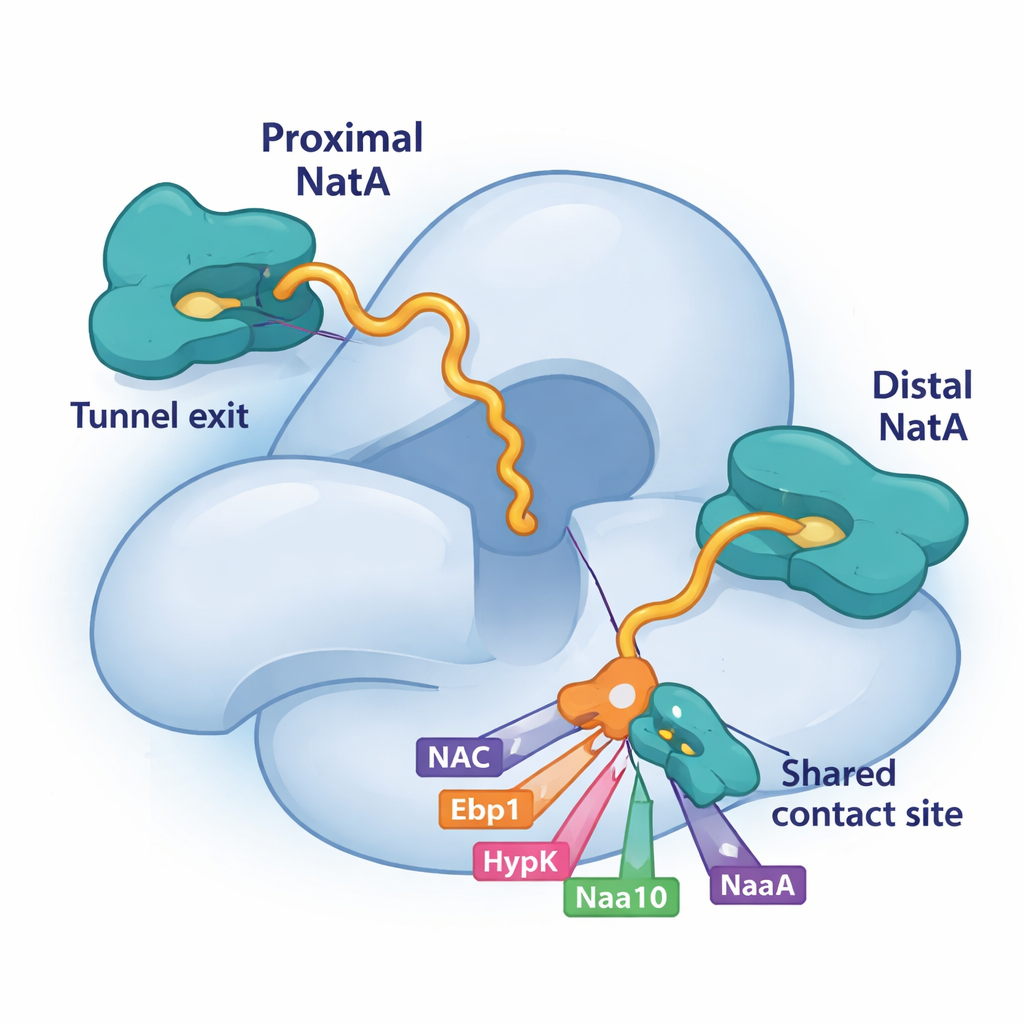
Concorrenza per un punto di atterraggio condiviso su NatA
Un elemento chiave di questo puzzle è una piccola fessura sulla subunità maggiore di NatA, Naa15. Lo studio mostra che quattro diversi fattori associati al ribosoma—NAC, HypK, Ebp1 e persino un tratto terminale della subunità catalitica di NatA, Naa10—usano eliche corte per aggrapparsi esattamente allo stesso punto su Naa15. Poiché tutti si affidano a questo punto di ancoraggio condiviso, devono competere per l’accesso. Quando HypK occupa il sito, non solo silenzia l’attività di NatA ma impedisce anche a NatA di associarsi a NAC o di formare dimeri NatA–NatA. Quando invece si legano NAC, la pseudo–enzima Ebp1 o Naa10 prossimale, essi possono rimodellare la posizione o le connessioni di NatA sul ribosoma. Questo legame competitivo offre alla cellula un modo flessibile per scegliere quali partner assemblare attorno a NatA in un dato momento.
Una pseudo-enzima come vigile del traffico molecolare
La proteina Ebp1 è particolarmente intrigante. Somiglia a una delle enzimi che rimuovono la metionina ma è priva di attività catalitica; è una “pseudo-enzima”. Lavori precedenti avevano mostrato che Ebp1 può posizionarsi sul ribosoma vicino all’uscita del tunnel e bloccare un lungo segmento di RNA. In questo studio, gli autori trovano che quando NatA si unisce al ribosoma, Ebp1 cambia posizione, rilascia l’RNA e invece usa la propria elica per occupare lo stesso sito di legame su Naa15 che NAC e HypK usano. Questo riassetto suggerisce che Ebp1 possa agire come segnaposto o organizzatore: può modellare l’ambiente locale dell’RNA e poi cedere il controllo a enzimi attivi come MAP e NatA, senza eseguire direttamente reazioni chimiche.
Perché questo controllo della folla molecolare è importante
Per un non specialista, i dettagli di eliche e siti di legame possono sembrare astratti, ma il messaggio è semplice: le cellule eseguono un sistema di controllo qualità altamente coreografato e a più passaggi proprio dove nascono le proteine. NatA si trova al centro di questo sistema, in grado di reclutare o rilasciare diversi partner a seconda di quali fattori ottengono accesso a una patch di ancoraggio cruciale e di quale sito ribosomale NatA occupa. Questa rete flessibile aiuta a garantire che il taglio e l’acetilazione avvengano con il giusto tempismo e ordine per migliaia di proteine diverse. Poiché errori nel processamento N-terminale sono collegati a disturbi dello sviluppo, neurodegenerazione e cancro, mappare come NatA e i suoi partner si assemblano fornisce ai ricercatori un progetto più chiaro per capire come sia controllata l’elaborazione proteica iniziale—e come potrebbe essere presa di mira quando va storta.
Citazione: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
Parole chiave: controllo qualità delle proteine, acetilazione N-terminale, uscita del tunnel ribosomale, complesso NatA, modificazione co-traduzionale