Clear Sky Science · it
La fucosiltransferasi vegetale FUT11 deforma l’accettore zuccherino per catalizzare tramite un intermedio ossocarbenio transitorio
Come le piante rifiniscono gli zuccheri sulle loro proteine
Le proteine nelle nostre cellule, e nelle piante, sono spesso decorate con catene complesse di zuccheri che funzionano come codici a barre, indirizzando il ripiegamento delle proteine, la loro durata e i partner con cui possono interagire. Questo studio è incentrato su un enzima vegetale chiamato FUT11 che aggiunge un piccolo zucchero, la fucosio, a queste catene. Svelando esattamente come FUT11 agisce a livello atomico, gli autori rivelano un trucco sorprendente: l’enzima piega brevemente il suo partner zuccherino fuori forma per favorire un passaggio chimico difficile. Comprendere questo processo è importante non solo per la biologia di base, ma anche per progettare farmaci prodotti in piante che evitino di scatenare risposte immunitarie indesiderate nell’uomo.
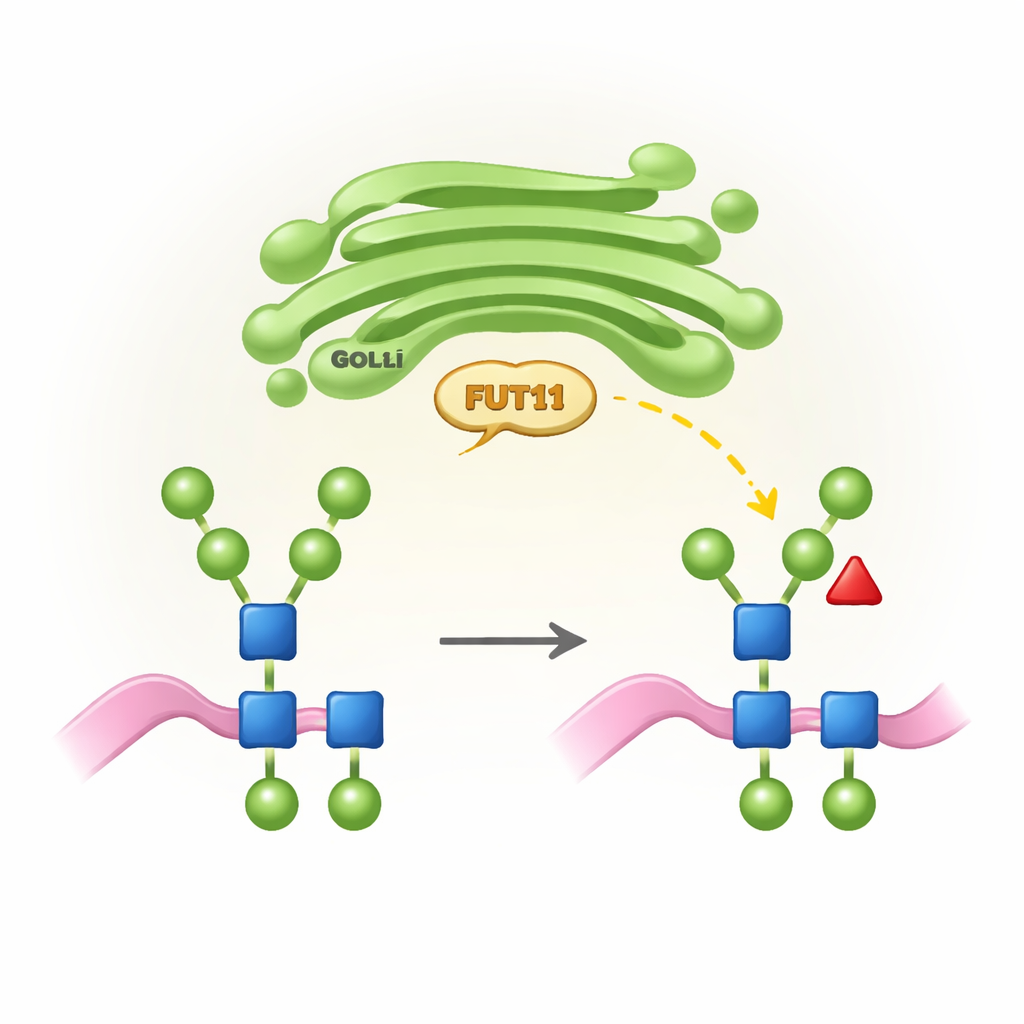
Marchette zuccherine specifiche delle piante e perché contano
Tutti gli organismi superiori usano un processo chiamato N-glicosilazione per legare catene di zuccheri (N-glicani) a punti specifici sulle proteine. Negli animali, queste catene vengono rimodellate nell’apparato di Golgi in strutture elaborate che spesso terminano con acidi sialici e portano una fucosio nel core in una posizione specifica. Le piante, invece, seguono una «regola di progetto» diversa: i loro N-glicani tipicamente non contengono acido sialico ma presentano una fucosio del core in un’altra posizione (indicata come β1,3) oltre a uno zucchero aggiuntivo, lo xiloso. Queste caratteristiche specifiche delle piante sono essenziali per una crescita e una fertilità normali, ma possono essere percepite come estranee dal sistema immunitario umano. FUT11 è uno degli enzimi chiave che installano questa fucosio del core, e la sua attività influenza sia lo sviluppo vegetale sia il modo in cui le proteine terapeutiche prodotte in piante saranno riconosciute nei nostri corpi.
Mappare dove FUT11 può agire sui rami zuccherini complessi
Per capire cosa riconosce FUT11, i ricercatori hanno testato l’enzima su un microarray con 144 diverse strutture di N-glicani. Hanno scoperto che FUT11 è piuttosto selettiva per un ramo dell’albero zuccherino — il cosiddetto braccio β1,3 — che deve portare un blocco costitutivo particolare (un N-acetilglucosamina terminale, o GlcNAc) affinché la reazione proceda. Allo stesso tempo, FUT11 tollera altre decorazioni: funziona ancora quando la mannosa centrale porta uno xiloso tipico delle piante, e persino quando un’altra fucosio è già stata aggiunta nella posizione tipica dei mammiferi nel core. Il ramo opposto (β1,6) è per lo più esposto al solvente e stabilisce solo deboli contatti con l’enzima, il che spiega perché FUT11 può gestire una vasta gamma di modifiche lì. Queste preferenze di legame aiutano a spiegare perché le piante producono un insieme caratteristico di strutture di N-glicani e mostrano come FUT11 potrebbe essere sfruttata o evitata nella glicoingegneria delle cellule vegetali per la biotecnologia.
Un disegno strutturale unico per afferrare e posizionare gli zuccheri
Usando la cristallografia a raggi X, il gruppo ha risolto la struttura tridimensionale di FUT11 legato al suo donatore zuccherino (GDP-fucosio) e a un accettore N-glicanico. L’enzima presenta un’architettura «GT-B» a due lobi: un lobo accoglie il GDP-fucosio, mentre un lobo accettore insolita mente elaborato, che include un sottodominio N-terminale specifico delle piante, avvolge l’N-glicano. Questo sottodominio aggiuntivo, collegato al resto dell’enzima tramite ponti disolfuro, ancora la parte centrale del glicano e aiuta a presentare l’unità reattiva GlcNAc verso il donatore. Mutare alcuni amminoacidi chiave ha confermato i loro ruoli: cambiare una singola glutammato (Glu158) ha eliminato l’attività, mentre alterare due residui vicini ha fortemente indebolito la fucosilazione in cellule umane ingegnerizzate. Questi risultati collegano istantanee strutturali alla funzione cellulare reale, mostrando esattamente quali parti della proteina sono indispensabili per il legame e la catalisi.
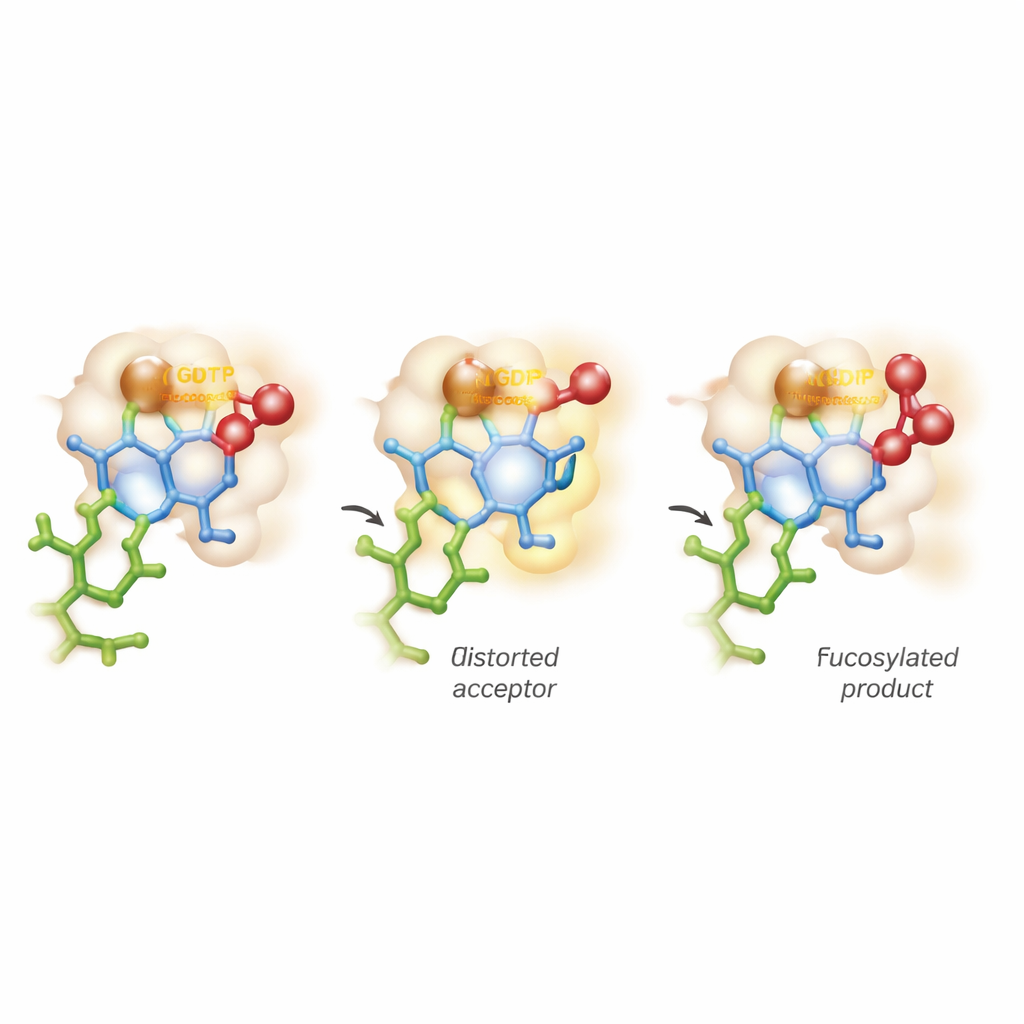
Piegare lo zucchero e camminare sulla linea tra due vie reattive
L’intuizione più sorprendente proviene da avanzate simulazioni al computer che combinano meccanica quantistica e dinamica molecolare. Le visioni tradizionali assumono che lo zucchero accettore mantenga la sua forma stabile a sedia mentre l’enzima attiva semplicemente il donatore. Qui, FUT11 si comporta in modo più aggressivo: interazioni guidate da Glu158 deformano temporaneamente l’anello più interno del GlcNAc in una forma incavata meno confortevole. In questa postura tesa, il gruppo ossidrilico critico è perfettamente allineato per attaccare il donatore di fucosio. I calcoli rivelano che mentre il legame chimico con il GDP si rompe, compare uno stato a vita breve, caricato positivamente, «simile a un ossocarbenio» sullzucchero, prima che il nuovo legame con l’accettore sia completamente formato. Ciò significa che la reazione non rientra nitidamente nelle categorie SN1 o SN2 dei manuali, ma procede lungo un continuum, in modo asincrono e quasi graduale.
Flessibilità nascosta ed echi evolutivi
Confrontando FUT11 con un enzima umano correlato, FUT9, gli autori hanno scoperto che l’enzima vegetale può anche, seppur debolmente, modificare un altro tipo di motivo zuccherino (LacNAc) per generare una struttura nota come Lewis X. Questa attività secondaria probabilmente non è biologicamente rilevante nelle piante, dove Lewis X non è normalmente presente, ma evidenzia come scheletri proteici simili possano essere riadattati nell’evoluzione per agire su contesti zuccherini differenti. Lo studio suggerisce che FUT11 e i suoi parenti condividono un quadro modulare per il riconoscimento degli N-glicani, con sottili aggiustamenti che spostano la specificità tra i core vegetali e le antenne animali.
Perché questo trucco di piegare lo zucchero conta per la scienza e la medicina
Nel complesso, il lavoro mostra che FUT11 fa più che avvicinare due partner zuccherini: deforma attivamente lo zucchero accettore in una posa reattiva e incanala la chimica attraverso un intermedio carico e fugace. Per il lettore non specialista, ciò significa che lo zucchero sulla proteina non è un sito di ancoraggio rigido ma un partecipante flessibile che l’enzima modella secondo le proprie necessità. Questa nuova visione della «catalisi conformazionale» aiuta a spiegare come gli enzimi ottengano velocità e selettività e offre un progetto per riprogettare le vie di glicosilazione. In termini pratici, conoscere esattamente come FUT11 riconosce e modifica gli N-glicani vegetali può guidare l’ingegnerizzazione di colture e sistemi di produzione vegetale per minimizzare i motivi zuccherini che scatenano il sistema immunitario umano, o per creare glicoproteine su misura con proprietà biologiche specifiche.
Citazione: Taleb, V., Sanz-Martínez, I., Serna, S. et al. Plant fucosyltransferase FUT11 distorts the sugar acceptor to catalyze via a transient oxocarbenium intermediate mechanism. Nat Commun 17, 1960 (2026). https://doi.org/10.1038/s41467-026-68786-6
Parole chiave: glicosilazione vegetale, fucosiltransferasi FUT11, N-glicani, meccanismo enzimatico, glicoingegneria