Clear Sky Science · it
Base strutturale e implicazioni patologiche del complesso core ERAD dimero OS9-SEL1L-HRD1
La squadra di pulizia cellulare sotto il microscopio
All’interno di ciascuna delle nostre cellule, una fabbrica affollata trasforma le istruzioni genetiche in proteine funzionanti. Come in qualsiasi fabbrica, possono verificarsi errori. Quando le proteine si ripiegano in modo errato, possono intasare il sistema e contribuire a malattie. Questo studio si concentra su una delle principali macchine di controllo qualità della cellula — il complesso SEL1L‑HRD1 — per rivelarne la struttura 3D dettagliata e mostrare come piccole variazioni genetiche possano compromettere questo meccanismo e potenzialmente condurre a patologie umane.
Un nastro trasportatore nascosto nella cellula
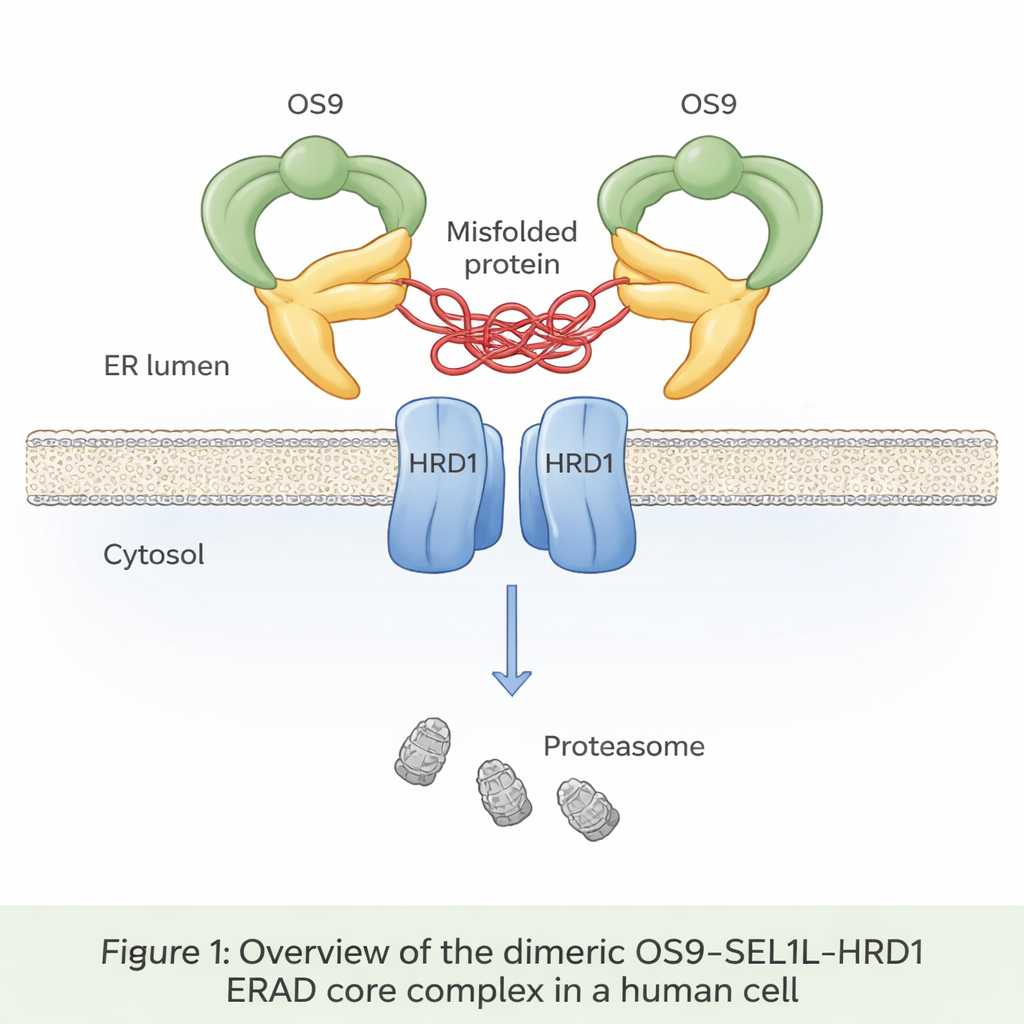
Fino a un terzo di tutte le proteine appena sintetizzate entra in un compartimento chiamato reticolo endoplasmatico, o RE, dove vengono ripiegate e controllate. Le proteine mal ripiegate vengono normalmente riconosciute, estratte dal RE e distrutte in un processo noto come degradazione associata al reticolo endoplasmatico (ER‑associated degradation, ERAD). Al centro di una delle principali vie ERAD si trova un trittico di proteine: OS9, SEL1L e HRD1. OS9 funge da sensore per le proteine difettose con marcatori zuccherini; SEL1L agisce da impalcatura; e HRD1 marca le proteine destinate alla distruzione con piccole etichette di ubiquitina che le indirizzano ai sistemi di smaltimento della cellula, i proteasomi. Fino ad ora, tuttavia, nessuno aveva osservato in dettaglio atomico come questi tre elementi si assemblino nelle cellule umane.
Rivelare la forma della macchina centrale
Gli autori hanno utilizzato la crio‑microscopia elettronica, una tecnica che imagina molecole congelate istantaneamente a risoluzione prossima all’atomo, per visualizzare il complesso OS9‑SEL1L‑HRD1 purificato da cellule umane. Hanno scoperto che si organizza in un dimero — essenzialmente due copie identiche unite tra loro — piuttosto che rimanere unità singole. Sul lato del lume del RE (l’interno del RE), due molecole di OS9 e due di SEL1L si assemblano in un anello simile a una chela di granchio con un’apertura centrale che sembra progettata per afferrare le proteine mal ripiegate. All’interno della membrana, due molecole di HRD1 si accoppiano per formare un canale condiviso. Questa disposizione posiziona la “chela” direttamente sopra la porta di HRD1, creando un percorso continuo perché le proteine mal ripiegate passino dal lume del RE, attraverso la membrana, verso la degradazione nel citosol.
Come piccole modifiche rompono un grande sistema
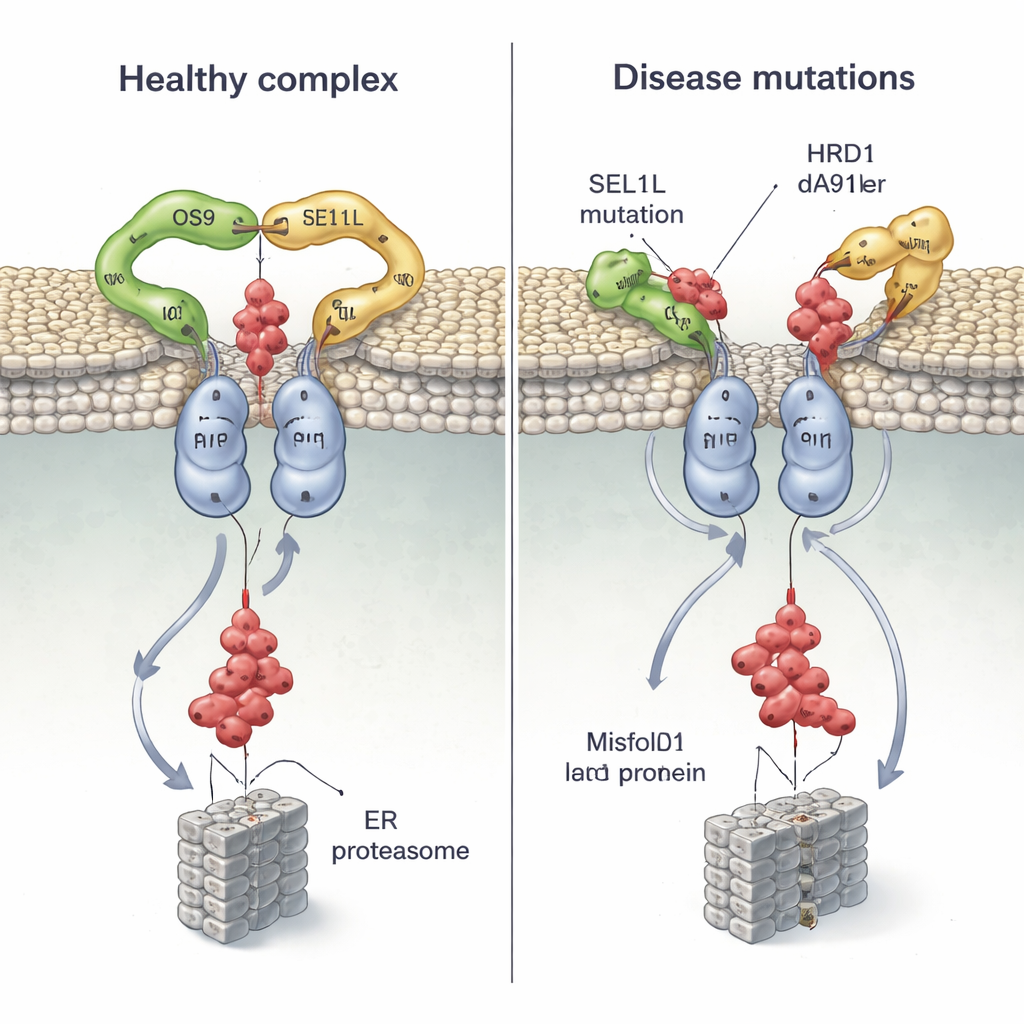
Poiché sono state trovate mutazioni in SEL1L e HRD1 in pazienti con gravi disturbi neuroevolutivi e altre patologie, il gruppo ha mappato diverse varianti associate a malattia sulla loro struttura e ha testato il loro comportamento nelle cellule. Due mutazioni di SEL1L, G585D e S658P, si trovano proprio nei punti di contatto rispettivamente con OS9 e HRD1. Negli esperimenti cellulari, G585D ha quasi abolito la capacità di SEL1L di legarsi a OS9, mentre S658P ha notevolmente indebolito la sua interazione con HRD1; la combinazione di entrambe le mutazioni ha di fatto rotto il complesso core, pur lasciando intatti altri partner. Di conseguenza, le cellule hanno faticato a marcare e eliminare un precursore ormonale mal ripiegato, permettendo alle proteine difettose di persistere.
Una mutazione patologica nel canale di membrana
La struttura mostra anche che il segmento transmembrana 3 di HRD1 è l’interfaccia chiave dove due molecole di HRD1 si incontrano per formare il canale. I ricercatori hanno introdotto “maniglie” di cisteina in posizioni specifiche e usato crosslinking chimico per confermare che queste regioni entrano in stretto contatto nelle cellule viventi, dimostrando che HRD1 si dimerizza realmente in vivo. Quando hanno perturbato un singolo residuo altamente conservato (T93) a questa interfaccia, il dimero si è disgregato e l’attività ERAD è crollata, anche se il complesso continuava ad assemblarsi con OS9 e SEL1L. Hanno poi esaminato una variante recentemente scoperta in un paziente, HRD1 A91D, trovata in un bambino con problemi cardiaci e polmonari. Questa alterazione, anch’essa nell’interfaccia di dimerizzazione, ha ridotto la dimerizzazione di HRD1 di circa la metà e ha compromesso gravemente lo smaltimento delle proteine mal ripiegate, ancora una volta senza alterare l’interazione complessiva con i partner.
Una nuova prospettiva sul controllo qualità delle proteine e sulle malattie
Combinando biologia strutturale e test su cellule, questo lavoro mostra che il complesso OS9‑SEL1L‑HRD1 opera come una macchina accoppiata e dimerica: un catturatore a forma di chela collegato a un canale condiviso che convoglia le proteine difettose fuori dal RE. Le mutazioni che allentano la presa della chela o destabilizzano la coppia HRD1 non si limitano a modificare l’efficienza — possono effettivamente inceppare il sistema, permettendo l’accumulo di proteine danneggiate che contribuiscono alle malattie umane. Per i non specialisti, il messaggio chiave è che anche cambiamenti di una singola lettera nel nostro DNA possono deformare sottilmente la forma di macchine cellulari essenziali, con conseguenze diffuse per lo sviluppo cerebrale, l’immunità e la funzione degli organi.
Citazione: Lin, L.L., Maldosevic, E., Zhou, L.E. et al. Structural basis and pathological implications of the dimeric OS9-SEL1L-HRD1 ERAD Core Complex. Nat Commun 17, 2064 (2026). https://doi.org/10.1038/s41467-026-68777-7
Parole chiave: controllo di qualità delle proteine, reticolo endoplasmatico, ERAD, complesso SEL1L-HRD1, ripiegamento proteico errato