Clear Sky Science · it
Profilo delle delezioni di esoni a singola cellula rivela eventi di splicing che modellano l’espressione genica e la dinamica dello stato cellulare
Come piccole modifiche all’RNA possono cambiare il comportamento cellulare
Le nostre cellule leggono e assemblano costantemente istruzioni RNA per decidere quali proteine produrre e come rispondere allo stress, crescere o dividersi. Questo studio mostra che modificare porzioni molto piccole di quei messaggi RNA — singoli segmenti chiamati esoni — può rimodellare in modo significativo l’attività genica e perfino alterare il modo in cui le cellule progrediscono nel ciclo cellulare. Il lavoro presenta uno strumento potente che consente agli scienziati di analizzare contemporaneamente molte di queste piccole scelte sull’RNA, cellula per cellula, aprendo nuove strade per comprendere le malattie e individuare bersagli farmacologici.
Ritagliare parole selezionate dal copione genetico
I geni sono scritti come lunghe porzioni di DNA, ma le cellule non li leggono in modo lineare. Invece, tagliano e incollano insieme blocchi più piccoli, chiamati esoni, per costruire un messaggio di RNA. Scegliendo quali esoni mantenere, le cellule possono produrre versioni proteiche multiple a partire da un singolo gene, proprio come realizzare diversi montaggi di un film dallo stesso girato. Molte malattie, compresi il cancro e l’autismo, sono correlate a errori in questo processo, eppure per la maggior parte delle scelte di esoni non sappiamo ancora cosa comportino effettivamente. Gli autori hanno affrontato questa lacuna costruendo un sistema su larga scala che può rimuovere esoni specifici da molti geni e poi osservare, in migliaia di singole cellule contemporaneamente, come queste modifiche influenzino il circuito interno della cellula.
Un “motore di ricerca” a singola cellula per la funzione degli esoni
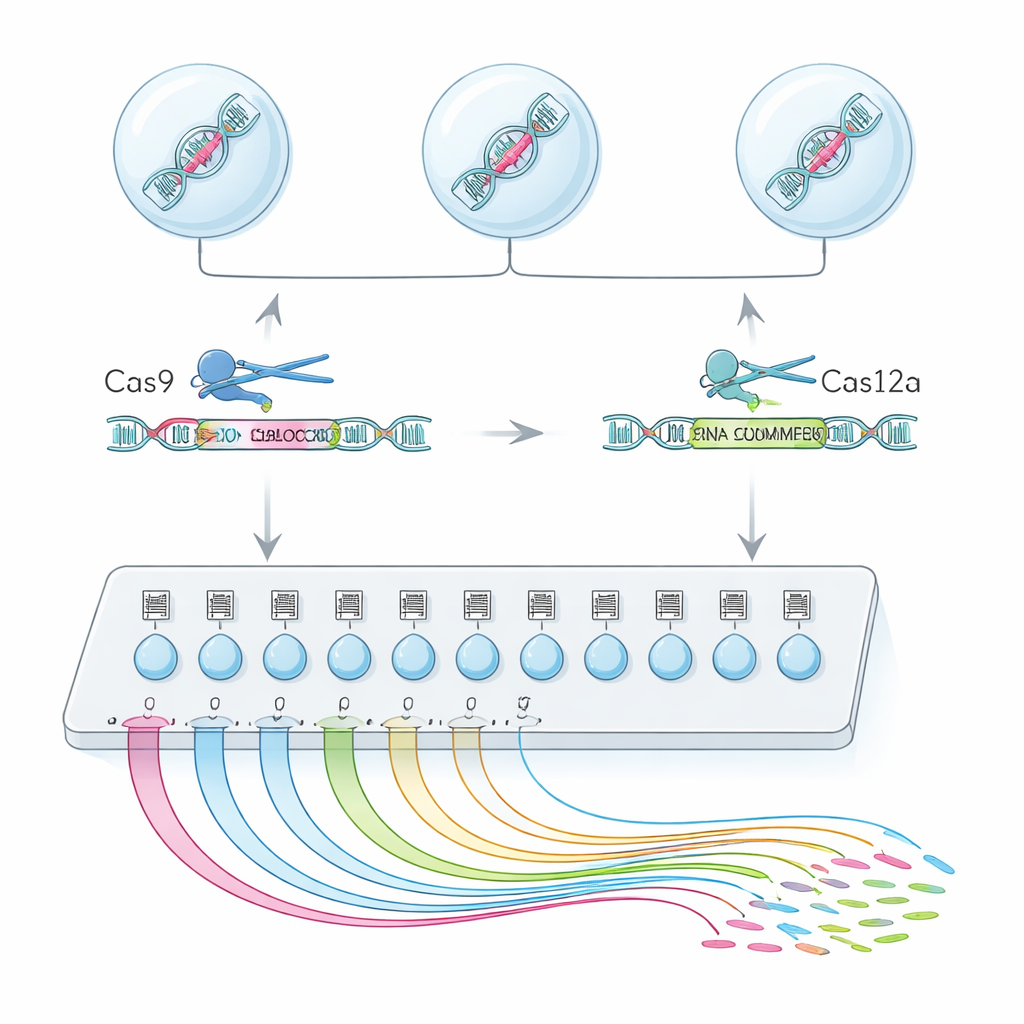
Per ottenere questo risultato, il team ha combinato due enzimi di editing del genoma, Cas9 e Cas12a, in una piattaforma ibrida chiamata CHyMErA. Ciascun enzima è guidato verso il DNA da brevi “indirizzi” di RNA. Direzionando i due enzimi per tagliare immediatamente prima e subito dopo un esone scelto, è possibile eliminare con precisione quel segmento lasciando intatto il resto del gene. Il nuovo metodo, scCHyMErA-Seq, collega questo taglio preciso alla tecnologia di sequenziamento dell’RNA a singola cellula. L’RNA di ciascuna cellula viene catturato in una goccia insieme a un barcode e alle guide RNA che specificano quale esone è stato rimosso. Il sequenziamento rivela così, per decine di migliaia di cellule, sia la modifica ricevuta da ciascuna cellula sia il modello dettagliato di geni attivati o disattivati.
Progettare lo strumento per vedere entrambe le lame delle forbici
Una sfida cruciale è stata rilevare in modo affidabile le guide di Cas12a insieme a quelle di Cas9 nello stesso esperimento a singola cellula. I progetti iniziali o non riuscivano a catturare le guide Cas12a oppure compromettevano l’efficienza dell’editing. I ricercatori hanno risolto il problema riprogettando con cura la sequenza dell’impugnatura di Cas12a per rimuovere tratti che interrompevano prematuramente la trascrizione, aggiungendo un piccolo elemento RNA stabilizzante e inserendo un passaggio di amplificazione mirata. Questi aggiustamenti hanno aumentato la capacità di rilevare entrambe le guide in circa il 90% delle cellule, mantenendo al contempo robuste delezioni di esoni. Con questa configurazione ottimizzata, gli autori hanno analizzato 224 esoni alternativi in 161 geni umani, profilando oltre 200.000 cellule singole di alta qualità.
Scoprire esoni che controllano programmi genici e cicli cellulari
Confrontando l’attività genica delle cellule modificate con i controlli, quasi la metà degli esoni testati ha provocato cambiamenti sostanziali in centinaia di altri geni. Gli esoni di geni coinvolti nell’elaborazione dell’RNA e nella trascrizione tendevano a raggrupparsi, producendo impronte di espressione simili e rivelando percorsi biologici condivisi, come la sintesi dei ribosomi o il decadimento dell’RNA. In alcuni casi, la rimozione di un singolo esone aveva un effetto chiaro e interpretabile: l’eliminazione di un esone nei geni TAF5 o LSM11 ha compromesso l’elaborazione corretta degli RNA degli istoni, portando a un accumulo insolito di messaggi istonici poliadenilati. Il set di dati ha inoltre evidenziato dozzine di esoni la cui perdita alterava la distribuzione delle cellule nelle diverse fasi del ciclo cellulare, collegando eventi specifici di splicing a decisioni su quando una cellula si arresta, copia il proprio DNA o si prepara a dividersi.
Un caso di studio: un esone che regola un master regulator
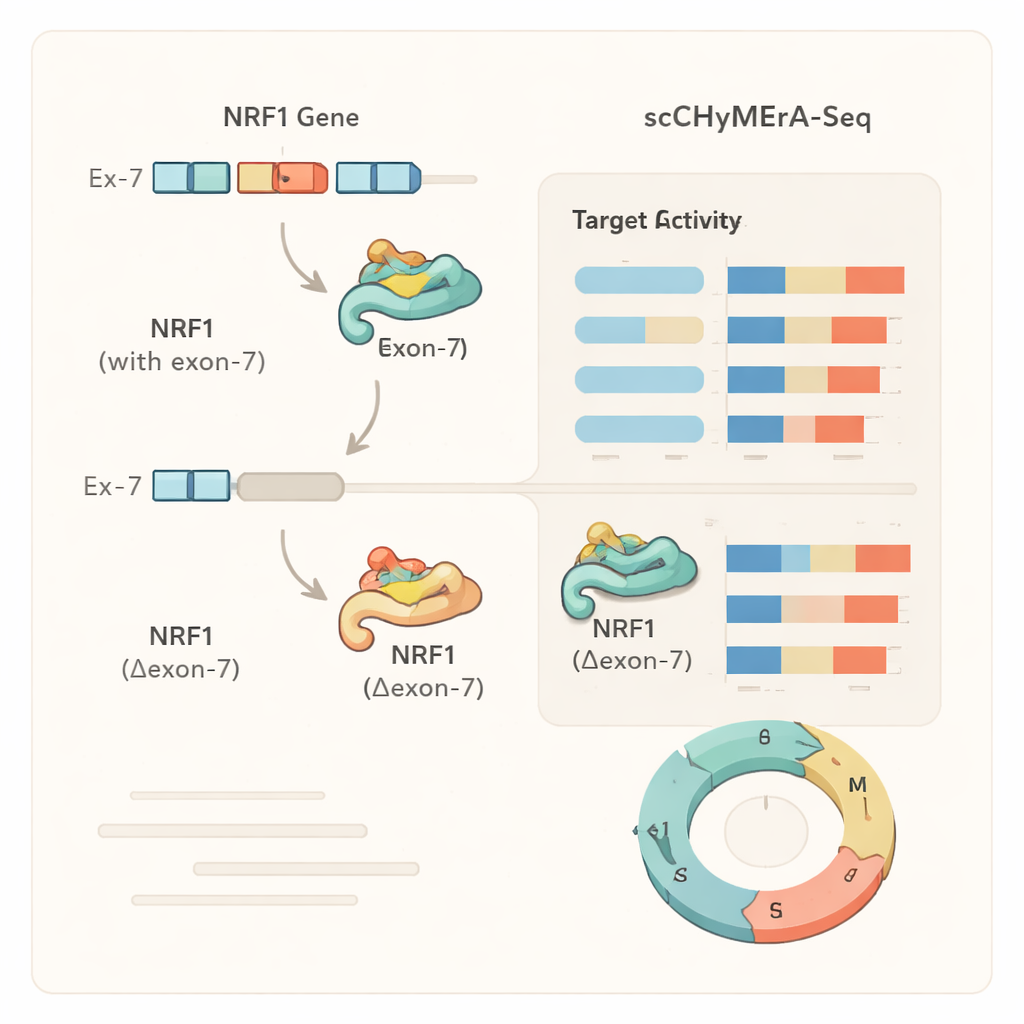
Un esempio notevole è stato l’esone 7 nel gene NRF1, un fattore di trascrizione che controlla molti geni coinvolti nella produzione di energia cellulare. Questo esone si sovrappone parzialmente alla regione di legame al DNA di NRF1. Quando l’esone 7 è stato eliminato, centinaia di geni controllati da NRF1 hanno modificato la loro attività, e esperimenti dettagliati hanno mostrato che la proteina NRF1 accorciata legava molto meno efficacemente i suoi promotori bersaglio nel genoma. Gli autori hanno inoltre identificato un regolatore dello splicing specifico, SRSF3, che favorisce l’inclusione di questo esone, rivelando una catena che va da un fattore di splicing, attraverso la scelta di un esone in NRF1, a cambiamenti ampi nei programmi genici e nel metabolismo cellulare. Analisi analoghe hanno mostrato che per alcuni geni la delezione di un esone imitava un knockout genico completo, mentre per altri produceva una modifica più fine e dipendente dallo stato cellulare, suggerendo che gli esoni alternativi possono modulare sottilmente il comportamento delle proteine invece di limitarsi ad attivarle o disattivarle.
Perché questo è importante per la salute e le terapie future
Per un non specialista, il messaggio chiave è che le cellule si affidano all’inclusione o allo skipping di segmenti RNA molto brevi per regolare il funzionamento dei geni, e che questi aggiustamenti fini possono modificare tratti importanti come il modo in cui le cellule si dividono o rispondono allo stress. La piattaforma scCHyMErA-Seq funziona come un test in laboratorio ad alto rendimento per queste scelte di splicing, individuando quali esoni hanno un reale impatto funzionale e come rimodellano gli stati cellulari. Poiché molti tumori e disturbi neurologici coinvolgono esoni mal splicati o fattori di trascrizione alterati, questo approccio potrebbe aiutare a prioritizzare quali varianti di splicing bersagliare con futuri farmaci o terapie basate su RNA, e fornire una mappa per comprendere come piccole modifiche nel copione genetico possano riverberare in grandi cambiamenti del comportamento cellulare.
Citazione: Kumari, B., Damodaran, A.P., Guiblet, W.M. et al. Single-cell exon deletion profiling reveals splicing events that shape gene expression and cell state dynamics. Nat Commun 17, 1218 (2026). https://doi.org/10.1038/s41467-026-68774-w
Parole chiave: splicing alternativo, sequenziamento dell’RNA a singola cellula, screening CRISPR, regolazione genica, ciclo cellulare